mRNA HIV疫苗安全的,可将感染风险降低79%
在一项新的研究中,来自美国国家过敏与传染病研究所(NIAID)的研究人员指出一种基于mRNA的实验性HIV疫苗--与两种高效的COVID-19 mRNA疫苗所用的平台技术相同--在小鼠和非人灵长类动物身上显示出了希望。他们的研究结果表明,这种新型疫苗是安全的,并能引发针对一种类似于HIV的病毒(即SHIV)的抗体和细胞免疫反应。与未接种这种疫苗的恒河猴相比,在接种初始疫苗(priming vaccine)以及此后多次接种加强疫苗的恒河猴每次接触猿-人类免疫缺陷病毒(simian-human immunodeficiency virus, SHIV)后的感染风险下降了79%。相关研究结果于2021年12月9日在线发表在Nature Medicine期刊上,论文标题为“A multiclade env–gag VLP mRNA vaccine elicits tier-2 HIV-1-neutralizing antibodies and reduces the risk of heterologous SHIV infection in macaques”。论文通讯作者为NIAID免疫调节实验室的Paolo Lusso博士。
论文共同作者、NIAID主任Anthony S. Fauci博士说,“尽管全球研究界进行了近四十年的努力,但预防HIV感染的有效疫苗仍然是一个难以实现的目标。这种实验性mRNA疫苗结合了几个特点,可能会克服其他实验性HIV疫苗的缺点,因此代表了一种有希望的方法。”
这种实验性疫苗的工作原理与COVID-19 mRNA疫苗类似。不过,该疫苗并不携带SARS-COV-2冠状病毒刺突蛋白的mRNA指令,而是提供制造两种关键HIV蛋白---Env和Gag---的编码指令。接种这种疫苗的动物中的肌肉细胞将这两种蛋白组装起来,产生病毒样颗粒(virus-like particle, VLP),其表面上有许多Env的拷贝。虽然这些VLP因缺乏HIV的完整遗传密码而不能引起感染或疾病,但是它们在刺激适当的免疫反应方面与完整的传染性HIV相匹配。
这些作者报告说,在对小鼠的研究中,两次注射这种形成VLP的mRNA疫苗在所有动物中诱发了中和抗体。由mRNA指令在小鼠体内产生的Env蛋白与完整HIV病毒中的Env蛋白非常相似,这是对之前的实验性HIV疫苗的一种改进。Lusso博士说,“在每个VLP表面上展示多个Env拷贝的HIV包膜蛋白是我们平台的特殊功能之一,它密切模拟自然感染,并可能在激发所需的免疫反应方面发挥了作用。”
这些作者随后在恒河猴身上测试了这种实验性mRNA疫苗:Env-Gag VLP mRNA疫苗。这种疫苗方案的细节在不同的疫苗接种动物亚群中有所不同,但都涉及到用经过修改的疫苗来激发免疫系统,以优化抗体的产生:在初始疫苗接种后,在一年内进行多次加强疫苗接种。加强疫苗包含来自两种HIV亚型的Gag mRNA和Env mRNA,这两种HIV亚型与初始疫苗中使用的一种HIV亚型不同。他们使用多种病毒变体来优先激活靶向Env中更保守的“相同”区域---广泛中和抗体的结合靶标---而不是靶向每种病毒毒株中不同的更多可变区域的抗体产生。
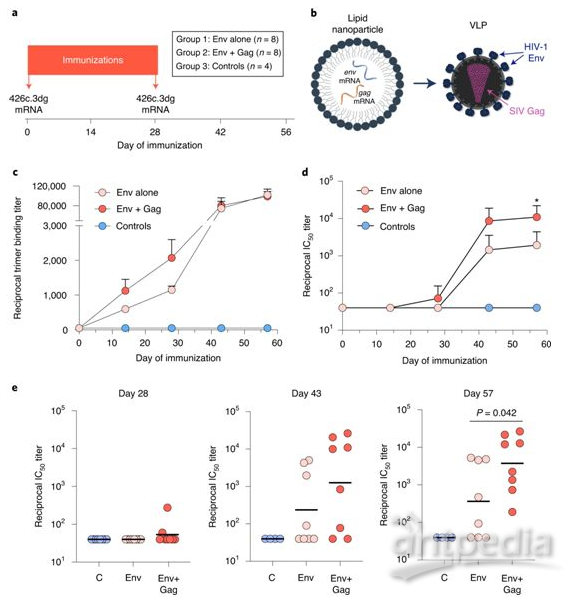
env-gag mRNA疫苗在小鼠中的免疫原性和效力
尽管递送的mRNA剂量很高,但是这种疫苗的耐受性很好,只在恒河猴中产生了轻微的、暂时的不良反应,如食欲不振。到第58周时,所有接种疫苗的恒河猴都产生了针对12种不同HIV病毒毒株中大多数毒株的可测量水平的中和抗体。除了诱导中和抗体产生外,这种mRNA疫苗还诱导了强劲的辅助性T细胞反应。
从第60周开始,接受疫苗接种的恒河猴(测试组)和未接受疫苗接种的恒河猴(对照组)每周通过直肠粘膜暴露于SHIV。由于非人灵长类动物对HIV-1不敏感,这些作者在实验中使用嵌合SHIV,因为这种病毒能够在恒河猴体内复制。经过13次每周一次的接种,七只接受疫苗接种的恒河猴中的两只仍然没有被感染。剩下的接受疫苗接种的恒河猴的感染总体上有所延迟,平均在8周后发生。相比之下,未接受疫苗接种的恒河猴平均在三周后就会被感染。
Lusso博士说,“我们如今正在完善我们的疫苗方案,以提高所产生的VLP的质量和数量。这可能会进一步提高疫苗的效力,从而降低产生强大免疫反应所需的初始疫苗接种和加强疫苗的接种次数。如果确认安全有效,我们计划在健康的成人志愿者中进行这种疫苗平台的1期临床试验。”







