固相萃取技术
液液分配(LLE)有许多局限性,例如需要大量不互溶溶剂;样品处理步骤复杂;样品回收率和精密度不理想;处理过程中乳液的形成,和溶剂蒸发时产生的样品损失等等。
固相萃取(SPE)主要用于样品分析前的净化或浓缩富集。与传统的液-液萃取相比,由于其采用了高效、高选择性的固定相,能显著减少溶剂用量,简化样品预处理过程,同时所需费用也有所减少,一般来说,固相萃取所需时间为液-液萃取的1/12,费用为液液分配的1/5。
固相萃取能用于气相色谱、液相色谱、红外光谱、质谱、核磁、紫外和原子吸收等各种分析方法的样品预处理。正因为固相萃取柱独特的性能,自70年代问世以来,其全球需求量迅速增长。
总的来讲,固相萃取法改进了样本制备技术:
(1)可批量进行;(2)节省时间;(3)减少溶剂使用和废物产生;(4)多种键合固定相选择性;(5)可富集痕量分析物;(6)可消除乳化现象;(7)易于自动化;(8)回收率高、重现性好。
一个固相萃取柱由三部分组成:(l)柱管;(2)烧结垫;(3)固定相。
柱管由血清级的聚丙烯制成,一般做成注射器形状。一些厂家也提供玻璃的柱管。柱管下端有一突出的头,此头的尺寸已标准化,可用于各种不同的固相萃取多管真空装置。
烧结垫除能固定固定相外,也能起一些过滤作用。聚乙烯是常见的烧结垫材料,对于特殊要求也可采用特氟隆或不锈钢片。
固定相是固相萃取柱中最重要的部分。最常见的固相萃取固定相是键合的硅胶材料。一般采用孔径60A不规则形状的40u硅胶微粒作为原材料,然后将各种官能团键合上去。也有一些非硅胶基质的固定相被广泛应用。
其一般操作步骤是:液态或溶解后的固态样品倒入活化过的固相萃取柱,然后利用抽真空、加压或离心等方式使样品进入固定相。为了同时处理多个样品,往往需要一个固相萃取柱多管真空装置。一般来说,固相萃取柱将保留所需要的组分和类似的其他组分,并尽量减少不需要的样品组分的保留。
弱保留组分的样品可用一溶剂冲洗掉,然后用另一溶剂把感兴趣的分析物从固定相上洗脱下来。另外,也可让感兴趣的组分(分析物)直接通过固定相而不被保留,同时大部分干扰物质被保留在固定相上,从而得到分离。在多数情况下,使分析物得到保留更有利于样品净化。
固相萃取柱类型
1、 键合相技术(固相分配柱技术)
2、 固相吸附柱技术
在细的、分散的载体(或固定相)表面涂有一层与流动相互不相溶的固定液或化学键合相,当液体流动相流经固定相时,由于有很大的界面,使分析物和提取物在两相间按分配系数分配。
分析物与提取物的分离能力取决于:
1、两相间极性的差异。
2、物质在两相间的亲和力和溶解度。
固定相:涂渍在惰性载体上的液体或化学键合在载体上的各种有机基团。
流动相:与固定相互不相溶的液体。流动相中的样品组分在两相间进行平衡分配,由于样品组分在两相中的相对溶解度不同,以不同的速度流出色谱柱而得到分离。
选择适宜的固定相和流动相,可对非常广泛样品类型进行分离。
目前常用的多为化学键合固定相,是利用化反应的方法,通过化学键把不同极性化合物键合到载体表面。先将硅胶进行酸洗、中和、干燥活化,使其表面保持自由硅醇基,如酯化键合,又如聚合键合固定相:

R为十八烷基(-C18),辛烷基(-C8),苯基(C6)或C2等,采用极性强的溶剂做流动相,如水、甲醇、乙腈等。R也可以是CN、苯基等基团,采用极性弱的溶剂为流动相。
正相色谱与反相色谱的区别可用下表来说明:

固定相的分离选择性决定于可被保留组分的保留强度;所以固定相的选择将取决于分析物质和样品溶剂的性质。
分析物的极性与固定相极性非常相似时,可得到分析物的最佳保留,两者极性越相似保留越好,所以要尽量选择极性相似的固定相。正相固定相如CN、Si、NH2 都是极性的,用来保留(萃取)极性物质。而C18、C8、C2、PH等都是反相固定相,用来保留(萃取)非极性分析物。当分析物极性适中时,正、反相固定相都可使用。
固定相的选择还受样品溶剂强度的制约,弱溶剂会增强分析物在吸咐剂上的保留,样品溶剂强度相对该固定相应该较弱。
对于正相和反相来说,组分在固定相上的保留或洗脱直接与溶剂极性有关,溶剂的极性决定溶剂的强度。在洗脱被保留组分时,强溶剂的用量比弱溶剂小。对于正相固定相,溶剂强度随其极性增加而增加。对于反相固定相,溶剂强度随其非极性增加而增加。常用的溶剂有水、甲醇、异丙醇和乙腈,有时也用丙酮和二氯甲烷。
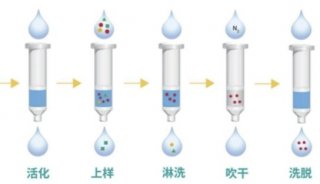
固相萃取的四个步骤
1、柱子预处理conditioning(固定相活化)(Column solvation/pre-equilibration)
活化的目的是创造一个与样品溶剂相容的环境并去除柱内所有杂质。通常需要两种溶剂来完成上述任务,第一个溶剂(初溶剂)用于净化固定相,另一个溶剂(终溶剂)用于建立一个合适的固定相环境使样品分析物得到适当的保留。每一活化溶剂用量约为1~2ml/100mg固定相。
终溶剂不应强于样品溶剂,若使用太强的溶剂,将降低回收率。通常采用一个弱于样品溶液的溶剂不会有什么问题。值得注意的是,在活化的过程中和结束时,固定相都不能抽干,因为这将导致填料床出现裂缝,从而得到低的回收率和重现性,样品也没得到应有的净化。如果在活化步骤中出现干裂,所有活化步骤都得重复。
2、上样load sample(Apply sample)
上样步骤指样品加入到固相萃取柱并迫使样品溶剂通过固定相的过程,这时分析物和一批样品干扰物保留在固定相上。
为了保留分析物,溶解样品的溶剂必须较弱。如果溶剂太强,分析物将不被保留,结果回收率将会很低,这一现象叫穿漏(breakthrough)。尽可能使用最弱的样品溶剂,可以使溶质得到最强的保留或者说最窄的谱带。只要不出现穿漏,允许采用大体积的上样量(0.5~1L)。
有时候固体样品必须用一个很强的溶剂进行萃取,这样的萃取液是不能直接上样的。所以萃取液要用一个弱溶剂稀释以得到一个合适的溶剂总强度进行上样。例如一个土壤样品,采用50%甲醇萃取,得到2ml萃取液,用8ml水稀释,得到10%的甲醇溶液,这样就可以直接上反相固相萃取柱而不存在穿漏问题。
3、淋洗Rinse(Interference elution)
分析物得到保留后,通常需要淋洗固定相以洗掉不需要的样品组分,淋洗溶剂的洗脱强度是略强于或等于上样溶剂。淋洗溶剂必须尽量地弱以洗调尽量多的干扰组分,但不能强到可以洗脱任何一个分析物的程度。溶剂体积可为0.5~0.8ml/100mg 固定相。
淋洗时不宜使用太强溶剂,太强溶剂会将强保留杂质洗下来。使用太弱溶剂,会使淋洗体积加大。可改为强、弱溶剂混用;但混用或前后使用的溶剂必须互溶。
4、洗脱Analyte Elution
淋洗过后,将分析物从固定相上洗脱,洗脱溶剂用量一般为0.5~0.8ml/100mg固定相。而溶剂必须进行认真选择,溶剂太强,一些更强保留的不必要组分将被洗出来;溶剂太弱.就需要更多的洗脱液来洗出。
-
仪器推荐

-
仪器推荐

-
仪器推荐

-
仪器推荐

-
仪器推荐

-
会议会展

-
企业风采

-
企业风采

-
会议会展