FLT3抑制剂Vanflyta在日本获全球首批,在美国遭FDA拒绝批准
日本药企第一三共制药(Daiichi Sankyo)近日宣布,该公司已收到美国食品和药物管理局(FDA)的一封完整回应函(CRL),该CRL是关于靶向抗癌药quizartinib治疗复发性/难治性FLT3-ITD急性髓性白血病(AML)成人患者的新药申请(NDA)。

值得一提的是,就在本周,quizartinib(品牌名Vanflyta)获得日本卫生劳动福利部(MHLW)批准治疗复发或难治性FLT3-ITD AML成人患者,这也是该药在全球范围内的首个监管批准。目前,该药也正在接受欧洲药品管理局(EMA)的加速评估。
在美国监管方面,今年4月份,FDA将NDA审查时间延长了3个月,至2019年8月25日。根据当时发布的声明,FDA需要时间来审查第一三共提交的与FDA要求相关的额外数据。
第一三共肿瘤学研发执行副总裁兼全球主管Antoine Yver表示:“公司正在评估CRL,之后将决定在美国监管方面采取的下一步行动。”
在美国,quizartinib的NDA,是基于关键性III期临床研究QuANTUM-R的数据,该研究是评估一种FLT3抑制剂作为口服单药疗法相对化疗治疗复发性/难治性FLT3-ITD AML患者显著延长总生存期的首个随机III期研究。在该研究中,与挽救性化疗相比,quizartinib口服单药疗法使死亡风险显著降低24%(HR=0.76,p=0.0177,95%CI:0.58-0.98)、总生存期显著延长(中位OS:6.2个月[双边检验95%CI:5.3-7.2] vs 4.7个月[双边检验95%CI:4.0-5.5]);quizartinib治疗组估计的1年生存率为27%,挽救性化疗组为20%。
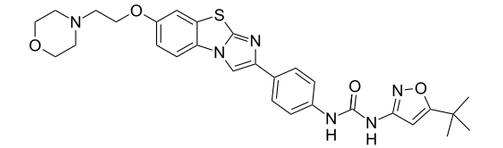
quizartinib分子结构式(图片来源:Wikipedia)
quizartinib属于第二代FLT3抑制剂,该药是一种口服小分子受体酪氨酸激酶抑制剂,选择性靶向抑制FLT3。在美国,quizartinib已获FDA授予治疗复发性/难治性FLT3-ITD AML成人患者的突破性药物资格、治疗复发性/难治性AML的快速通道地位。此外,quizartinib在美国、欧盟均被授予了治疗AML的孤儿药资格,在日本被授予了治疗FLT3突变AML的孤儿药资格。
AML是一种侵袭性血液和骨髓癌症,导致患者体内功能失常的癌变白细胞不受控制地增生和积累,并影响正常血细胞的生成。FLT3基因突变是AML最常见的基因异常改变之一,其中FLT3-ITD是最常见的FLT3突变,影响约1/4的AML患者。FLT3-ITD是白血病高负担、预后差并对AML患者疾病管理有显著影响的一种驱动突变。与未携带FLT3-ITD突变的AML患者相比,FLT3-ITD AML患者总体预后更差,包括复发率增加、复发后死亡风险增加、造血干细胞移植后复发的可能性更高。
原文出处:Daiichi Sankyo Provides Update on FDA Review of Quizartinib for the Treatment of Patients with Relapsed/Refractory FLT3-ITD AML
-
企业风采

-
焦点事件

-
企业风采

-
产品技术

-
项目成果
-
产品技术