Cell子刊:蛋白通道的转运新解
加州理工学院的化学家首次成功模拟了一个蛋白通道的生物学功能,即允许特定蛋白通过细胞膜的过程。以往原子级别的动态模拟一般只达到纳秒水平,而他们成功进行了一分钟的原子动态模拟,详细展示了Sec易位子的作用机制。化学助理教授Thomas Miller及其研究生Bin Zhang将这项成果发表在Cell旗下的Cell Reports杂志上。
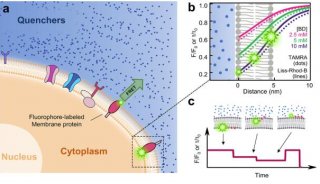
Sec 易位子是细胞膜中的通道,能够识别并转运新合成的蛋白。细胞膜不允许包括水分子在内的任何分子随意出入,因此核糖体合成的蛋白需要通过蛋白通道进行运输,从而到达正确位点执行执行蛋白功能。Sec易位子这样的通道就相当于看门人,一旦Sec易位子决定蛋白可以通过,它就会开启,允许蛋白整合到膜上或者分泌到细胞外。
是什么决定了穿过易位子蛋白的命运,科学家们意见不一。有研究显示,蛋白氨基酸序列与水的亲和力是决定性的,蛋白转运是一个平衡态过程。也有研究认为,蛋白插入通道的频率很重要,动力学影响才是关键。
“有人认同平衡机制,认为蛋白序列是决定性的。也有人提出动力学影响是关键,”Miller说,“而我们的研究显示,这两者都在起作用。”
2010年和今年早些时候,Miller和Zhang就曾在美国国家科学院院刊PNAS等杂志上发表文章,描述了他们对Sec易位子的原子模拟。不过当时他们模拟了该系统的所有原子,而且模拟时长最多只能达到百万分之一秒。
而现在,研究者们在前期研究的基础上明确了易位子的关键组分,计算了蛋白通过时各组分所需的能量。由此,他们建立了只包括重要组分的简化模型,将模拟时长增加到了一分钟。研究人员反复运行这一简化模型,逐步更改其中的变量(包括蛋白氨基酸序列、所带电荷、插入易位子的频率、尾部长度等等),并仔细分析了蛋白通过通道时的情况。
“研究显示,平衡态和动力学一同控制着这一过程,只不过我们只有在观察全局时才能够明确这一点”,Miller说。研究人员还利用新模型进行了长蛋白的模拟,与短蛋白不同,长蛋白很明显受到上述两种机制的影响。
-
科技前沿
-
科技前沿
-
项目成果