PCR技术 PCR技术的应用
一滴残留在裙子上的精液使得美国总统Bill Clinton不得不坦承他与白宫实习生有不正当的关系。因为他知道现在的生物科技就连一个精子也能被用来做为证据。这种将极微量的生物标本化为可供鉴定的现代技术正是PCR(Polymerase chain reaction)--聚合酶链式反应具有的特色之一。这也是分子生物医学令人震撼的一例。
何谓PCR
简单的说,PCR就是利用DNA聚合酶对特定基因做体外或试管内 (In Vitro) 的大量合成。基本上它是利用DNA聚合酶进行专一性的连锁复制.目前常用的技术,可以将一段基因复制为原来的一百亿至一千亿倍。
PCR的要素
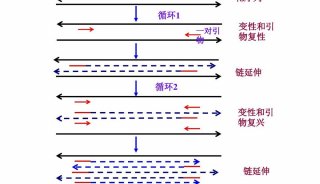
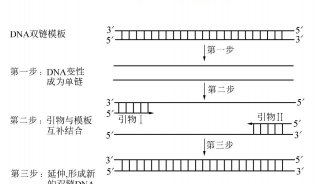
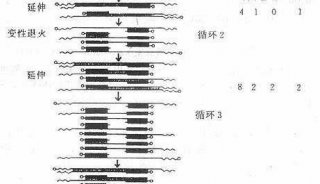
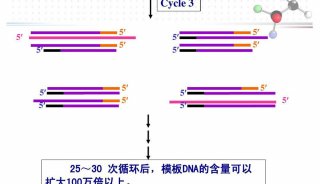
基本的PCR须具备1.要被复制的DNA模板 (Template) 2.界定复制范围两端的引物(Primers). 3.DNA聚合酶 (Taq. Polymearse) 4.合成的原料及水。PCR的反应包括三个主要步骤,分别是1). Denaturation 2). Annealing of primers, and 3). Extension of primers。 所谓 Denaturing乃是将DNA加热变性, 将双股的DNA加热后转为单股DNA以做为复制的模板. 而Annealing 则是令 Primers于一定的温度下附着于模板DNA两端。 最后在DNA聚合酶 (e.g. Taq-polymerase) 的作用下进行引物的延长 (Extension of primers)及另一股的合成。
PCR 的问题,无疑是绝大多数学生物的人都关心的问题。今天我们把相关内容整理出来,与大家共同讨论,希望对大家能有所帮助。 一、引物设计所谓“工欲善其事,必先利其器”,这年头手工设计引物的人似乎不多,还是用软件方便些,防止你一不小心看走眼,丢一个碱基,同时计算起来也方便。设计软件有很多,既可以在线设计(如Primer3 http://frodo.wi.mit.edu/cgi-bin/primer3/primer3_www.cgi),也可以用Primer5、Oligo6.65 等等。1. 引物设计的原则细心地进行引物设计是PCR 中最重要的一步。理想的引物对只同目的序列两侧的单一序列而非其他序列退火。设计糟糕的引物可能会同时扩增其他的非目的序列。下面的指导描述了一个可以增加特异性的引物所具有的令人满意的特点:1)典型的引物18 到24 个核苷长。引物需要足够长,保证序列独特性,并降低序列存在于非目的序列位点的可能性。但是长度大于24 核苷的引物并不意味着更高的特异性。较长的序列可能会与错误配对序列杂交,降低了特异性,而且比短序列杂交慢,从而降低了产量。2)选择GC 含量为40%到60%或GC 含量与模板GC 含量接近的引物。3)设计5'端和中间区为G 或C 的引物。这会增加引物的稳定性和引物同目的序列杂交的稳定性。4)避免引物对3'末端存在互补序列,这会形成引物二聚体,抑制扩增。在用软件设计时大家常常会疑惑,究竟? G 不能低于多少?这里有个数据: ? G 为0~-2时,PCR 产率可达100%, ? G=-6 时,为40%.5)避免3'末端富含GC。设计引物时保证在最后5 个核苷中含有3 个A 或T。6)避免3'末端的错误配对。3'端核苷需要同模板退火以供聚合酶催化延伸。3’最好以G或C 结尾,防止AT 的松散结合引起错配。7)避免存在可能会产生内部二级结构如发夹结构的序列,这会破坏引物退火稳定性。8)引物的一个重要参数是熔解温度(Tm)。这是当50%的引物和互补序列表现为双链DNA 分子时的温度。两引物的Tm 值相差不应大于5℃。计算Tm 有几种公式。第一个公式(Wallace 规则):Tm = 4℃(g + C) +2℃(a + T),这来源于高盐溶液中的杂交,适用于小于15-20个碱基的引物,也适用于手工设计时的简单计算。第二个公式(Baldino 算法)适用于计算14-70个核苷酸在≤0.4mol\L 的阳离子溶液中的Tm, 也可用于扩增产物的Tm 计算.Tm=81.5+16.6*lg[K+]+0.41(%[G+C])-(675/n)。以上两种算法都是基于碱基组成而不是碱基排列而计算的,事实上相同碱基组成的引物Tm 可能差异不小:GGGAA 和GAGAG 的Tm 是不一样的,所以确定引物Tm 最可信的方法是近邻分析法。这种方法从序列一级结构和相邻碱基的特性预测引物的杂交稳定性。大部分计算机程序如Primer5 等均使用近邻分析法。9)当在引物5’端添加酶切位点时要考虑:a)该目的序列内部不得含有相同的酶切位点,在引物发出后才发现错误的事情本人就干过,在论坛上也能看到这样的粗心人。这样的错误会给将来的克隆造成麻烦。b)如果打算PCR 后直接酶切,不要忘了在酶切位点的外侧再加上保护碱基,不同的酶对于保护碱基的要求是不同的。如果不设计保护碱基,则多半要用TA 克隆的方式连接到质粒上,这时要注意Taq 酶的选择,这一点在后面再聊。若想在目的序列上附加上并不存在的序列,如限制位点和启动子序列,可以加入到引物5'端而不影响特异性。当计算引物Tm 值时并不包括这些序列,但是应该对其进行互补性和内部二级结构的检测。10)有时候,对于引物设计仅了解有限的序列信息。比如,如果仅知道氨基酸序列,可以设计兼并引物。兼并引物是指代表编码单个氨基酸所有不同碱基可能性的不同序列的混合物。为了增加特异性,可以参考密码子使用表,根据不同生物的碱基使用偏好,减少兼并性。次黄嘌呤可以同所有的碱基配对,降低引物的退火温度。特别要注意的是:不要在引物的3'端使用兼并碱基,因为3'端最后3 个碱基的退火足以在错误位点起始PCR。使用较高的引物浓度(1µM 到3µM),因为许多兼并混合物中的引物不是特异性针对目的模板。说了半天了,想起来还得提醒大家一句:千万别搞错了引物的位置!这句话似乎多余。看了上面的图吧,如果要扩增目的序列为“ATG…………TGA”的片段,则引物分别为“ATG……”和“TCA……”仔细琢磨一下,特别是5’端再接上酶切位点可别搞错了!合成错了一条可就是50 块钱,到时候挨老板批的时候别怪我没提醒你哦:)设计好了引物就要让公司合成,这时候别忘了谈价格:)现在竞争很厉害,价格已经挺便宜了,注意两个参数:一个是OD 值,如果公司说1OD 能比2OD 优惠,那通常1OD 足够了。第二是纯度,是HPLC 的还是OPC 的,事先要说好,建议看看这里(唉,不是我给他们做广告,只是他们的说明书写得真不错):http://www.takara.com.cn/product/cs/c_3.htm#1引物设计方面还有很多话题可说,比如如何利用引物搭桥将两个片段通过PCR 而不是酶连接起来、如果要设计引物表达蛋白时注意“N 端规则”。 二、PCR 成分引用《分子克隆3》提供的PCR 标准反应条件:模板1pg-1μg引物1μmol/LDNA 聚合酶1-5 单位Mg2+ 1.5mmol/LdNTPs 200μmol/LKCl 50 mmol/L1. 模板模板可是PCR 的关键,模板的质量是PCR 成功的先决条件,巧妇难为无米之炊嘛!怎样得到模板,这可是一个大问题,仅仅一个提取基因组DNA 就有很多的名堂,这会是我们后面专辑的内容,这里不多说啦,有问题来论坛讨论吧。P 不出东西的时候不妨先考虑:模板有没有问题?(DNA 样品中发现有多种污染物会抑制PCR。一些在标准基因组DNA 制备中使用的试剂,如SDS,在浓度低至0.01%时就会抑制扩增反应。)所需的最佳模板量取决于基因组的大小。你的目的片段在基因组中占多少?至少要保证模板中含有一个单拷贝吧!100ng 到1µg 的人类基因组DNA,相当于3×104 到3×105 个分子。所以对于单拷贝基因,这需要0.1μg 的人基因组DNA,10ng的酵母DNA,1ng 的大肠杆菌DNA.扩增多拷贝序列时,用量更少.灵敏的PCR 可从一个细胞,一根头发,一个孢子或一个精子提取的DNA中分析目的序列.模板量过多则可能增加非特异性产物.DNA中的杂质也会影响PCR的效率。2. 引物引物以干粉形式运输。最好用TE 重溶引物,使其最终浓度为100µM。TE 比去离子水好,因为水的pH 经常偏酸,会引起寡核苷的水解。当然,如果担心TE 对于PCR 的影响,不妨用ddH2O。引物的稳定性依赖于储存条件。应将干粉和溶解的引物储存在-20℃。以大于10µM 浓度溶于TE 的引物在-20℃可以稳定保存6 个月,但在室温(15℃到30℃)仅能保存不到1 周。干粉引物可以在-20℃保存至少1 年,在室温(15℃到30℃)最多可以保存2 个月。注意:溶解之前先离心一下,防止一开盖就飞了。引物的浓度会影响特异性。最佳的引物浓度一般在0.1 到0.5µM。较高的引物浓度会导致非特异性产物扩增。通常跟着引物来的说明书会告诉你,关于寡核苷酸的计算可以看看这里:http://www.takara.com.cn/product/fl/i_1.htm3. 聚合酶的选择这可是有讲究,咱论坛里有个专题讨论这个问题。主要考虑两个方面:用途——对保真度的要求高不高?成本——高保真的酶总是会贵一些的。综合考虑一下找个平衡点吧,当然啦,该花钱的时候可不能省。Taq DNA聚合酶被看做是低保真度的聚合酶,因为其缺少3'到5'外切核酸酶(校正)活性。使用带有3'到5'外切核酸酶活性的热稳定聚合酶可以提高保真度。但是这些聚合酶的产量比Taq DNA聚合酶低。在很多公司的手册中有对各种酶特性的描述,大家不妨比较一下。提醒一点:高保真酶除了我所知的Merck的Easy-A 以外,都不会在3’端加A尾巴(因为其3’-5’外切酶活性),所以做TA克隆的时候需要一点小诀窍——扩增完了再加普通Taq去加个A。另外还有个方法:将Taq DNA聚合酶同带有3'到5'外切核酸酶活性第二种聚合酶混合在一起可以获得比单独Taq DNA聚合酶高的保真度,并可以得到高产量及扩增长模板。4. Mg2+浓度镁离子影响PCR的多个方面,如DNA聚合酶的活性,这会影响产量;再如引物退火,这会影响特异性。dNTP和模板同镁离子结合,降低了酶活性所需要的游离镁离子的量。最佳的镁离子浓度对于不同的引物对和模板都不同,但是包含200µM dNTP的典型PCR起始浓度是1.5mM(注意:对实时定量PCR,使用3到5mM带有荧光探针的镁离子溶液)。在多数情况下,较高的游离镁离子浓度可以增加产量,但也会增加非特异性扩增,降低忠实性(当然,也有相反的报道)。为了确定最佳浓度, 可以用0.1-5mmol/L的递增浓度的Mg2+ 进行预备实验,选出最适的Mg2+浓度。在PCR反应混合物中, 应尽量减少有高浓度的带负电荷的基团, 例如磷酸基团或EDTA等可能影响Mg2+ 离子浓度的物质,以保证最适Mg2+ 浓度。5. dNTPs高浓度的dNTPs会对扩增反应起抑制作用。将每种dNTP的浓度从200µM降低到25-50µM可以使扩增产物获得满意的产率。6. KCl标准浓度为50 mmol/L, 对于较短片段可将其提高到70-100 mmol/L. 三、PCR 反应参数1. 变性:在第一轮循环前,在94℃下变性5-10min 非常重要,它可使模板DNA 完全解链,然后加入Taq DNA聚合酶(hot start),这样可减少聚合酶在低温下仍有活性从而延伸非特异性配对的引物与模板复合物所造成的错误。变性不完全,往往使PCR 失败,因为未变性完全的DNA 双链会很快复性,减少DNA 产量.一般变性温度与时间为94℃ 1min。在变性温度下,双链DNA 解链只需几秒钟即可完全,所耗时间主要是为使反应体系完全达到适当的温度。对于富含GC 的序列,可适当提高变性温度.但变性温度过高或时间过长都会导致酶活性的损失。2. 退火:这是PCR 的一个关键参数。在理想状态下,退火温度足够低,以保证引物同目的序列有效退火,同时还要足够高,以减少非特异性结合。合理的退火温度从55℃到70℃。退火温度一般设定比引物的Tm 低5℃, 当产物中包含有影响实验的非可异性扩增带时,以2℃为增量,逐步提高退火温度。较高的退火温度会减少引物二聚体和非特异性产物的形成。如果两个引物Tm 不同,将退火温度设定为比最低的Tm 低5℃。或者为了提高特异性,可以在根据较高Tm 设计的退火温度先进行5 个循环,然后在根据较低Tm 设计的退火温度进行剩余的循环。这使得在较为严紧的条件下可以获得目的模板的部分拷贝。退火温度越高,所得产物的特异性越高。有些反应甚至可将退火与延伸两步合并,只用两种温度(例如用60℃和94℃)完成整个扩增循环, 既省时间又提高了特异性。退火一般仅需数秒钟即可完成,反应中所需时间主要是为使整个反应体系达到合适的温度。3. 延伸:延伸反应通常为72℃,接近于Taq DNA 聚合酶的最适反应温度75℃.实际上,引物延伸在退火时即已开始,因为Taq DNA 聚合酶的作用温度范围可从20℃-85℃.延伸反应时间的长短取决于目的序列的长度和浓度.在一般反应体系中,Taq DNA聚合酶每分钟约可合成1kb 长的DNA。延伸时间过长会导致产物非特异性增加.但对很低浓度的目的序列, 则可适当增加延伸反应的时间。一般在扩增反应完成后,都需要一步较长时间(10-30min)的延伸反应,以获得尽可能完整的产物, 这对以后进行克隆或测序反应尤为重要。4. 循环次数: 当其它参数确定之后, 循环次数主要取决于DNA 浓度。一般而言25-30轮循环已经足够。循环次数过多,会使PCR 产物中非特异性产物大量增加。通常经25-30 轮循环扩增后, 反应中Taq DNA 聚合酶已经不足, 如果此时产物量仍不够, 需要进一步扩增,可将扩增的DNA 样品稀释103-105倍作为模板, 重新加入各种反应底物进行扩增, 这样经60 轮循环后, 扩增水平可达109-1010。扩增产物的量还与扩增效率有关,扩增产物的量可用下列公式表示:C=Co(1+P)n 。其中:C 为扩增产物量,C0 为起始DNA 量, P 为增效率, n 为循环次数。在扩增后期,由于产物积累,使原来呈指数扩增的反应变成平坦的曲线,产物不再随循环数而明显上升,这称为平台效应。平台期会使原先由于错配而产生的低浓度非特异性产物继续大量扩增,达到较高水平。因此,应适当调节循环次数,在平台期前结束反应,减少非特异性产物。 四、提高PCR 扩增特异性1. 递减PCR(TouchDown PCR)递减PCR 通过在PCR 的前几个循环使用严紧的退火条件提高特异性。循环设在比估算的Tm 高大约5℃的退火温度下开始,然后每个循环降低1℃到2℃(当然,也可以每几个循环降1-2℃),直到退火温度低于Tm 5℃。特异性最高的目的模板会被优先扩增,这些产物在随后的循环中继续扩增占据优势。递减PCR 对于那些不了解引物和目的模板同源性程度的方法更为有用,如AFLP® DNA 指纹分析。2. 热启动热启动PCR 是除了好的引物设计之外,提高PCR 特异性最重要的方法之一。尽管TaqDNA 聚合酶的最佳延伸温度在72℃,聚合酶在室温仍然有活性。因此,在进行PCR 反应配制过程中,以及在热循环刚开始,保温温度低于退火温度时会产生非特异性的产物。这些非特异性产物一旦形成,就会被有效扩增。在用于引物设计的位点因为遗传元件的定位而受限时,如定点突变、表达克隆或用于DNA 工程的遗传元件的构建和操作,热启动PCR 尤为有效。并且,热启动在很大程度上防止引物二聚的发生。限制Taq DNA 聚合酶活性的常用方法是在冰上配制PCR 反应液,并将其置于预热的PCR 仪。这种方法简单便宜,但并不能完成抑制酶的活性,因此并不能完全消除非特异性产物的扩增。热启动通过抑制一种基本成分延迟DNA 合成,直到PCR 仪达到变性温度。包括延缓加入Taq DNA 聚合酶在内的大部分手工热启动方法十分烦琐,尤其是对高通量应用。其他的热启动方法使用蜡防护层将一种基本成分,入镁离子或酶,包裹起来,或者将反应成分,如模板和缓冲液,物理地隔离开。在热循环时,因蜡熔化而把各种成分释放出来并混合在一起。象手动热启动方法一样,蜡防护层法比较烦琐,易于污染,不适用于于高通量应用。3. 促进PCR 的添加剂退火温度,引物设计和镁离子浓度的优化足以对大多数模板进行高特异性的扩增,但是,某些模板,包括高GC 含量的模板,需要其他的措施。影响DNA 熔解温度的添加剂提供了提高产物特异性和产量的另外一种方法。为获得最好的结果需要模板的完全变性。另外,二级结构会阻止引物结合和酶的延伸。PCR 添加剂,包括甲酰胺,DMSO,甘油,甜菜碱以及PCRx Enhancer Solution 可以增强扩增。它们可能的机理是降低熔解温度,从而有助于引物退火并辅助DNA 聚合酶延伸通过二级结构区。PCRx Solution 还有其他优点。在同PlatinumTaq DNA 聚合酶和Platinum Pfx DNA 聚合酶一起使用时,仅需很少的镁离子优化。这样,将Platinum 技术同添加剂结合,增强了特异性,同时减少了第三种方法-镁离子优化的依赖。为获得最佳结果,应优化添加剂的浓度,尤其是会抑制Taq DNA 聚合酶的DMSO,甲酰胺和甘油。4. 巢式PCR使用巢式引物进行连续多轮扩增可以提高特异性和灵敏度。第一轮是15 到20 个循环的标准扩增。将一小部分起始扩增产物稀释100 到1000 倍加入到第二轮扩增中进行15 到20个循环。或者,也可以通过凝胶纯化将起始扩增产物进行大小选择。在第二轮扩增中使用一套巢式引物,其可以同第一套引物内侧的靶序列结合。巢式PCR 的使用降低了扩增多个靶位点的可能性,因为同两套引物都互补的靶序列很少。而使用同样的引物对进行总数相同的循环(30 到40)会扩增非特异性靶位点。巢式PCR 可以增加有限量靶序列(如稀有mRNA)的灵敏度,并且提高了困难PCR(如5' RACE)的特异性。 五、PCR 产物测序对于PCR 产物的测序有两个方式:1. DNA 直接测序: 指直接分析不经分离的PCR 扩增产物,如果各个位点上碱基序列都是一致的,则所得信号是确定的,否则,在那些有相异碱基的位点出现模糊信号, 如果模板在多数情况下被正确扩增,则少数的突变将被掩盖,这是结果显示的是模板的序列.但是,当扩增的前几轮即出现错误扩增并被后续的循环积累,这时就不再反映模板的状况.2. PCR 产物经克隆后测序: 这是对单克隆测序,其结果是反映单一扩增产物的序列,结果是确定的. 六、PCR 污染与对策PCR 反应的最大特点是具有较大扩增能力与极高的灵敏性,但令人头痛的问题是易污染,极其微量的污染即可造成假阳性的产生.1、污染原因(一)标本间交叉污染:标本污染主要有收集标本的容器被污染,或标本放置时,由于密封不严溢于容器外,或容器外粘有标本而造成相互间交叉污染;标本核酸模板在提取过程中,由于吸样枪污染导致标本间污染;有些微生物标本尤其是病毒可随气溶胶或形成气溶胶而扩散,导致彼此间的污染.(二)PCR 试剂的污染:主要是由于在PCR 试剂配制过程中,由于加样枪、容器、双蒸水及其它溶液被PCR 核酸模板污染.(三)PCR 扩增产物污染.这是PCR 反应中最主要最常见的污染问题.因为PCR 产物拷贝量大(一般为1013 拷贝/ml),远远高于PCR 检测数个拷贝的极限,所以极微量的PCR 产物污染,就可造成假阳就可形成假阳性.还有一种容易忽视,最可能造成PCR 产物污染的形式是气溶胶污染;在空气与液体面摩擦时就可形成气溶胶,在操作时比较剧烈地摇动反应管,开盖时、吸样时及污染进样枪的反复吸样都可形成气溶胶而污染.据计算一个气溶胶颗粒可含48000 拷贝,因而由其造成的污染是一个值得特别重视的问题.(四)实验室中克隆质粒的污染:在分子生物学实验室及某些用克隆质粒做阳性对照的检验室,这个问题也比较常见.因为克隆质粒在单位容积内含量相当高,另外在纯化过程中需用较多的用具及试剂,而且在活细胞内的质粒,由于活细胞的生长繁殖的简便性及具有很强的生命力.其污染可能性也很大.2、污染的监测一个好的实验室,要时刻注意污染的监测,考虑有无污染是什么原因造成的污染,以便采取措施,防止和消除污染.对照试验:1)阳性对照:在建立PCR 反应实验室及一般的检验单位都应设有PCR 阳性对照,它是PCR 反应是否成功、产物条带位置及大小是否合乎理论要求的一个重要的参考标志.阳性对照要选择扩增度中等、重复性好,经各种鉴定是该产物的标本,如以重组质粒为阳性对照,其含量宜低不宜高(100 个拷贝以下).但阳性对照尤其是重组质粒及高浓度阳性标本,其对检测或扩增样品污染的可能性很大.因而当某一PCR 试剂经自己使用稳定,检验人员心中有数时,在以后的实验中可免设阳性对照.2)阴性对照:每次PCR 实验务必做阴性对照.它包括①标本对照:被检的标本是血清就用鉴定后的正常血清作对照;被检的标本是组织细胞就用相应的组织细胞作对照.②试剂对照:在PCR 试剂中不加模板DNA 或RNA,进行PCR 扩增,以监测试剂是否污染.3)重复性试验4)选择不同区域的引物进行PCR 扩增
3、防止污染的方法(一)合理分隔实验室:将样品的处理、配制PCR 反应液、PCR 循环扩增及PCR 产物的鉴定等步骤分区或分室进行,特别注意样本处理及PCR 产物的鉴定应与其它步骤严格分开.最好能划分①标本处理区;②PCR 反应液制备区;③PCR 循环扩增区;④PCR 产物鉴定区. 其实验用品及吸样枪应专用.实验前应将实验室用紫外线消毒以破坏残留的DNA 或RNA.(二)吸样枪:吸样枪污染是一个值得注意的问题.由于操作时不慎将样品或模板核酸吸入枪内或粘上枪头是一个严重的污染源,因而加样或吸取模板核酸时要十分小心,吸样要慢,吸样时尽量一次性完成,忌多次抽吸,以免交叉污染或产生气溶胶污染.(三)预混和分装PCR 试剂:所有的PCR 试剂都应小量分装,如有可能,PCR 反应液应预先配制好,然后小量分装,-20℃保存.以减少重复加样次数,避免污染机会.另外,PCR 试剂,PCR 反应液应与样品及PCR 产物分开保存,不应放于同一冰盒或同一冰箱.(四)防止操作人员污染,使用一次性手套、吸头、小离心管应一次性使用.(五)设立适当的阳性对照和阴性对照,阳性对照以能出现扩增条带的最低量的标准病原体核酸为宜,并注意交叉污染的可能性,每次反应都应有一管不加模板的试剂对照及相应不含有被扩增核酸的样品作阴性对照.(六)减少PCR 循环次数,只要PCR 产物达到检测水平就适可而止.(七)选择质量好的Eppendorf 管,以避免样本外溢及外来核酸的进入,打开离心管前应先离心,将管壁及管盖上的液体甩至管底部.开管动作要轻,以防管内液体溅出.4、PCR 污染解决对策(这是从另一篇文章总结而来,与前面的部分略有重复,大家随便看看吧)PCR 检测微量感染因子时,一定要注意产物残留污染的问题。 一. 污染的预防进行PCR 操作时,操作人员应该严格遵守一些操作规程,最大程度地降低可能出现的PCR 污染或杜绝污染的出现。(一)划分操作区:目前,普通PCR 尚不能做到单人单管,实现完全闭管操作,但无论是否能够达到单人单管,均要求实验操作在三个不同的区域内进行,PCR 的前处理和后处理要在不同的隔离区内进行:1. 标本处理区,包括扩增摸板的制备;2. PCR 扩增区,包括反应液的配制和PCR 扩增;3. 产物分析区,凝胶电泳分析,产物拍照及重组克隆的制备。各工作区要有一定的隔离,操作器材专用,要有一定的方向性。如:标本制备→PCR扩增? 产物分析? 产物处理。切记:产物分析区的产物及器材不要拿到其他两个工作区。(二)分装试剂:PCR 扩增所需要的试剂均应在装有紫外灯的超净工作台或负压工作台配制和分装。所有的加样器和吸头需固定放于其中,不能用来吸取扩增后的DNA 和其他来源的DNA:1.PCR 用水应为高压的双蒸水;2.引物和dNTP 用高压的双蒸水在无PCR 扩增产物区配制;3.引物和dNTP 应分装储存,分装时应标明时间,以备发生污染时查找原因。(三) 实验操作注意事项尽管扩增序列的残留污染大部分是假阳性反应的原因,样品间的交叉污染也是原因之一。因此,不仅要在进行扩增反应是谨慎认真,在样品的收集、抽提和扩增的所有环节都应该注意:1. 戴一次性手套,若不小心溅上反应液,立即更换手套;2. 使用一次性吸头,严禁与PCR 产物分析室的吸头混用,吸头不要长时间暴露于空气中,避免气溶胶的污染;3. 避免反应液飞溅,打开反应管时为避免此种情况,开盖前稍离心收集液体于管底。若不小心溅到手套或桌面上,应立刻更换手套并用稀酸擦拭桌面;4. 操作多份样品时,制备反应混合液,先将dNTP、缓冲液、引物和酶混合好,然后分装,这样即可以减少操作,避免污染,又可以增加反应的精确度;5. 最后加入反应模板,加入后盖紧反应管;6. 操作时设立阴阳性对照和空白对照,即可验证PCR 反应的可靠性,又可以协助判断扩增系统的可信性;7. 尽可能用可替换或可高压处理的加样器,由于加样器最容易受产物气溶胶或标本DNA 的污染,最好使用可替换或高压处理的加样器。如没有这种特殊的加样器,至少PCR操作过程中加样器应该专用,不能交叉使用,尤其是PCR 产物分析所用加样器不能拿到其它两个区;8. 重复实验,验证结果,慎下结论。 二. 追踪污染源如果不慎发生污染情况,应从下面几条出发,逐一分析,排除污染。(一)设立阴阳性对照:有利于监测反应体系各成分的污染情况。选择阳性对照时,应选择扩增弱,且重复性好的样品,因强阳性对照可产生大量不必要的扩增序列,反而可能成为潜在的污染源。如果以含靶序列的重组质粒为对照,100 个拷贝之内的靶序列就足以产生阳性扩增。阴性对照的选择亦要慎重,因为PCR 敏感性极高,可以从其它方法(Sourthern 印迹或点杂交等)检测阴性的标本中检测出极微量的靶分子。此外,每次扩增均应包括PCR 体系中各试剂的时机对照,即包括PCR 反应所需的全部成分,而不加模板DNA,这对监测试剂中PCR 产物残留污染是非常有益的。如果扩增结果中试剂对照为阳性结果,就是某一种或数种试剂被污染了。此时,要全部更换一批新的试剂进行扩增,扩增时设立不同的反应管,每一管含有一种被检测试剂,在检出污染试剂后,应马上处理。(二)环境污染:在排除试剂污染的可能性外,更换试剂后,若不久又发现试剂被污染了,如果预防措施比较严密,则考虑可能为环境污染。环境污染中常见的污染源主要有:1. 模板提取时真空抽干装置;2. 凝胶电泳加样器;3. 电泳装置;4. 紫外分析仪;5. 切胶用刀或手术刀片;6. 离心机;7. 冰箱门把手,冷冻架,门把手或实验台面等;此时可用擦拭实验来查找可疑污染源。1)用无菌水浸泡过的灭菌棉签擦拭可疑污染源;2)0.1ml 去离子水浸泡;3)取5ml 做PCR 实验;4)电泳检测结果。8. 气溶胶。如果经过上述追踪实验,仍不能查找到确切污染源,则污染可能是由空气中PCR 产物的气溶胶造成的,此时就应该更换实验场所,若条件不允许,则重新设计新的引物(与原引物无相关性)。 三.污染处理(一)环境污染1. 稀酸处理法:对可疑器具用1mol/L 盐酸擦拭或浸泡,使残余DNA 脱嘌呤;2. 紫外照射(UV)法:紫外波长(nm)一般选择254/300nm,照射30min 即可。需要注意的是,选择UV 作为消除残留PCR 产物污染时,要考虑PCR 产物的长度与产物序列中碱基的分布,UV 照射仅对500bp 以上长片段有效,对短片段效果不大。UV 照射时,PCR产物中嘧啶碱基会形成二聚体,这些二聚体可使延伸终止,但并不是DNA 链中所有嘧啶均能形成二聚体,且UV 照射还可使二聚体断裂。形成二聚体的程度取决于UV 波长,嘧啶二聚体的类型及与二聚体位点相邻核苷酸的序列。在受照射的长DNA 链上,形成二聚体缺陷的数量少于0.065/碱基,其他非二聚体的光照损伤(如环丁烷型嘧啶复合体,胸腺嘧啶乙二醇,DNA 链间与链内的交联和DNA 断裂等)均可终止Taq DNA 聚合酶的延伸。这些位点的数量与二聚体位点相当。如果这些位点( 0.13/碱基)在DNA 分子上随机分布,一个500bp片段的DNA 分子链上将有32 处损伤位点,那么,105个这样的分子中每个分子中会至少有一处损伤。相反,如果100bp 的片段,每条链上仅有6 处损伤,105个拷贝分子中将有许多分子没有任何损伤。这就是UV 照射有一定的片段长度限制的原因。 (二)反应液污染可采用下列方法之一处理:1. DNase I 法:PCR 混合液(未加模板和Taq 聚合酶)加入0.5U DNase I,室温反应30min 后加热灭活,然后加入模板和Taq 聚合酶进行正常PCR 扩增。该方法的优点是不需要知道污染DNA 的序列;2. 内切酶法:选择识别4 个碱基的内切酶(如Msp I 和Taq I 等),可同时选择几种,以克服用一种酶只能识别特定序列的缺陷,室温作用1h 后加热灭活进行PCR;3. 紫外照射法:未加模板和Taq 聚合酶的PCR 混合液进行紫外照射,注意事项与方法同上述UV 照射法;4. g 射线辐射法:1.5kGy 的辐射可完全破坏0.1ng 基因组DNA,2.0 kGy 可破坏104 拷贝的质粒分子,4.0 kGy 仍不影响PCR,但高于此限度会使PCR 扩增效率下降。引物可受照射而不影响PCR,g 射线是通过水的离子化产生自由基来破坏DNA 的。 (三)尿嘧啶糖苷酶(UNG)法由于UV 照射的去污染作用对500bp 以下的片段效果不好,而临床用于检测的PCR 扩增片段通常为300bp 左右,因此UNG 的预防作用日益受到重视和肯定。1. 原理:在PCR 产物或引物中用dU 代替dT。这种dU 化的PCR 产物与UNG 一起孵育,因UDG 可裂解尿嘧啶碱基和糖磷酸骨架间的N-糖基键,可除去dU 而阻止TaqDNA 聚合酶的延伸,从而失去被再扩增的能力。UNG 对不含dU 的模板无任何影响。UNG 可从单或双链DNA 中消除尿嘧啶,而对RNA 中的尿嘧啶和单一尿嘧啶分子则无任何作用。2. dUTP 法:用dUTP 代替dTTP,使产物中掺入大量dU。在再次进行PCR 扩增前,用UNG 处理PCR 混合液即可消除PCR 产物的残留污染。由于UNG 在PCR 循环中的变性一步便可被灭活,因此不会影响含dU 的新的PCR 产物。3. dU 引物法:合成引物时以dU 代dT,这样PCR 产物中仅5ˊ端带dU。UNG 处理后,引物失去了结合位点而不能扩增。对长片段(1-2kb 以上)的扩增用dUTP 法效率较用dTTP低,而用dU 法就可克服这一缺点。dU 引物最好将dU 设计在3ˊ端或近ˊ端。该法仅能用于引物以外试剂的处理。4. 优点:可以去除任何来源的污染;UNG 处理可以和PCR 扩增在同一个反应管内进行;由于扩增产物中有大量dU 存在,可彻底消除污染源。5. 需注意的是掺入dUTP 的DNA不应对产物的任何操作有影响,在进行PCR 产物克隆时,应该转化UNG-(UNG 缺陷)大肠杆菌受体菌,否则转化产物会被受体菌UNG 消化掉。 (四) 固相捕获法用于去除标本中污染的核酸和杂质,原理如下:1)用一生物素标记的单链RNA 探针与待扩核酸杂交,杂交区域是非扩增区;2)用包被链霉亲和素的固相载体来捕获带有生物素探针的杂交核酸,通过漂洗可去除污染的扩增产物和杂质;3)洗脱靶分子后用特异引物扩增非RNA 探针杂交区域。第2)步的漂洗后可用PCR 检测以确定标本是否被扩增产物或重组质粒污染。 (五)RS-PCR 法(RNA-specific PCR)也称为链特异性PCR,主要指用于RNA 模板的特异性PCR 法,该法可明显降低假阳性而不影响PCR 的敏感性。其关键在于设计引物,逆转录引物的3ˊ端(A 区)有2 0 个核苷酸左右为模板的特异性互不序列,5ˊ端2 0 个核苷酸(C 区)为附加修饰碱基。与mRNA逆转录后,经超速离心使cDNA 与多余引物分开,再用和第二引物(C)以第一链cDNA为模板合成第二链cDNA,以后的PCR 循环中用逆转录引物的B 区和引物C 进行扩增加尾cDNA,而污染的DNA 或质粒DNA 才不会被扩增。 (六)抗污染引物法该对引物扩增时通过病毒DNA克隆如入质粒的位点。这一区域只存在完整的原病毒中,在重组质粒中,这一区域分成两个区域与克隆位点被。如果重组质粒污染了标本,也不能扩增出任何条带,即使出现了扩增带,其大小也与预期的不同。只有原病毒DNA 才能被引物扩增,因此只要出现预期大小的扩增带就可以证明标本是阳性的,该法试用于环状靶分子系列。 附录: 各种碱基符号在设计简并引物或测序时你可能会碰到这样的符号来表示碱基,到时候不要不知道哦:B = C or G or TD = A or G or TH = A or C or TK = G or TM = A or CN = A or C or G or TR = A or GS = C or GV = A or C or GW = A or TY = C or T