肿瘤克隆的临床应用价值
前列腺癌患者在临床上的表现可谓千差万别,有很多前列腺肿瘤可能好几十年都不会有任何进展,可是有一些前列腺肿瘤的恶化程度却又非常快,在几个月之内就会出现远处转移,甚至致人死亡。流行病学资料也越来越明显,在美国,平均每6个成年男性中就会有1人在一生中被诊断出患有前列腺癌,每年每33名前列腺癌患者中就会有1人因病死亡。前列腺癌患者死亡的主要原因就是癌细胞转移,而我们目前的治疗手段还无法阻止前列腺癌细胞的转移。自从Charles Huggins在70多年前发明了去雄性激素疗法(androgen deprivation therapy)之后,该方案一直是临床上治疗前列腺癌转移患者的首选疗法。通过该方法可以使依赖雄性激素的肿瘤细胞凋亡、坏死。几乎所有的前列腺癌转移患者经过阉割手术(castration)或第一代抗雄性激素药物(antiandrogens)治疗之后病情都会有所好转,但是他们最终都无一例外地会复发、死亡,这主要是因为还存在不依赖雄性激素的肿瘤细胞(castration-resistant prostate cancer, CRPC)。正是因为前列腺癌在组织结构和基因组学方面都存在如此巨大的异质性(heterogeneity),所以才给我们的临床治疗带来了上述这些麻烦。
寻找耐药根源
要了解前列腺癌转移,一个最根本的问题就是要明确在诊断之初是否就存在多个在基因组学层面存在差异的不同肿瘤病灶,它们今后会同时发生转移,导致患者死亡;亦或是在诊断之初就只存在一个占据绝对优势的肿瘤克隆,而且该克隆在整个疾病的发展演变过程中会一直处于优势地位。本期《科学 转化医学》(Science Translational Medicine)杂志将向您介绍Carreira等人最新的工作进展,他们对前列腺癌患者进行了连续的病理活检检查,通过这种方法来跟踪肿瘤克隆的遗传演进过程,同时对患者整个病程过程(直至疾病晚期)进行动态监测。他们在寻找转移癌常见染色体缺失(chromosomal deletions)的过程中发现了多个互相独立的克隆,这些肿瘤克隆在肿瘤组织和外周循环中都有发现。考虑到循环基因组物质有可能来自体内多个转移灶,所以对这些DNA进行监测更加能够反映雄性激素受体(androgen receptor, AR)信号通路的动态变化情况。如图1所示,这种雄性激素受体信号通路就是导致治疗失败的主要原因。
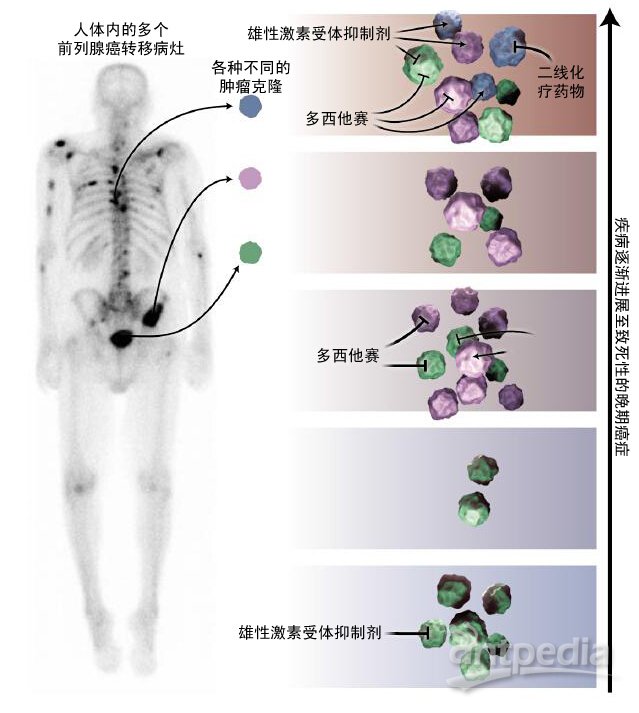
图1:对肿瘤转移克隆进行连续检测能够指导体内存在CRPC细胞(不依赖雄性激素的肿瘤细胞)前列腺癌患者的临床治疗。上图形象的展示了前列腺癌转移患者体内发生的具体情况,如图所示,有多个转移灶肿瘤细胞克隆都会进入到人体的循环系统当中。随着疾病的进展,慢慢发展到致死性的CRPC期,这些肿瘤克隆也都是导致患者产生耐药性的根本原因。对这些肿瘤克隆进行遗传学分析能够指导临床医生在恰当的时间选择使用最合适的药物,包括abiraterone 和enzalutamide等抗雄性激素药物,泼尼松(prednisone)、化疗药物多西他赛,以及多西他赛与enzalutamide联用或二线化疗药物cabazitaxel等。
对于存在CRPC细胞的前列腺癌患者而言,AR一直都是决定治疗效果的关键因素。这也是我们长久以来一直在试图解决的一个问题。在CRPC细胞上过表达AR可以促使细胞对抗雄性激素药物耐药。受体发生的杂乱的突变也使得配体结合结构域(ligand-binding domain, LBD)的结合能力有了很大的“灵活性”,所以肾上腺雄激素(adrenal androgens)和enzalutamide、abiraterone等抗雄性激素药物都能够使AR活化。另外一些研究证据表明,缺少LBD的各种 AR截短体(truncated AR splice variants, AR-Vs),以及糖皮质激素受体(glucocorticoid receptor, GR)都能够“躲过”AR阻断药物,所以在抗雄性激素药物治疗耐药的前列腺癌患者时,这些受体也都是非常好的潜在作用靶点。研究还发现,在出现抗雄性激素治疗失败之后才开始出现AR大量扩增或突变的情况,这说明的确是抗雄性激素治疗促使肿瘤细胞发生了基因组学层面的适应性改变,继续维持了AR信号通路的活性,所以才会出现耐药的情况。
解决耐药问题所面临的挑战
那么对前列腺癌的预后具有如此重要影响作用的肿瘤异质性与异常的雄性激素轴(androgen axis)之间又是如何发生相互作用,以及跟踪肿瘤克隆对于耐药性预测的价值又有多大呢?Carreira等人的工作为我们提供了答案——对晚期前列腺癌患者进行连续循环DNA监测有助于寻找更佳的治疗时机,决定合适的停药时间,在继续使用抗雄性激素药物和糖皮质激素类药物反而对病人有害时及时停药。以往开展的寻找致命前列腺癌克隆的工作瞄准的都是源于转移灶的单个的克隆。Carreira等人开展的工作则为我们提供了另外一种与此截然相反,但是又非常有意思的思路,而且他们的工作必将改变晚期前列腺癌患者的临床管理模式。Carreira等人以取自前列腺转移癌患者血液和肿瘤组织的样品为研究材料,在 21q22、8p21和10q23这3个位点上发现了完全不同,而且存在动态变化特征的基因组缺失现象,这说明存在多个不同的肿瘤克隆,而且这些克隆都是对患者致命的。通过证明在CRPC的演进过程中,循环肿瘤克隆的异质性存在动态改变的情况,Carreira等人的工作表明,我们过去一直低估了循环肿瘤细胞的数量,而这对于设计循环DNA测序策略是一个非常大的风险,因为这会忽略携带非常见基因组突变的肿瘤克隆(图1)。该工作还让我们意识到,出现AR 突变与治疗失败和患者对抗雄性激素疗法治疗反应的临床演变过程之间在时间上的关系。
如果肿瘤多克隆现象是导致enzalutamide和 abiraterone配合糖皮质激素类药物治疗失败的唯一原因,那么这是否也能够推广到抗微管蛋白的化疗药物(microtubuletargeting chemotherapy,这类药物往往会在抗雄性激素药物使用之前使用,或者与抗雄性激素药物联合使用)上,帮助我们进一步解析争论已久的,认为前列腺癌细胞对这两类药物所存在的交叉耐药现象的作用机制呢?因此,要解决肿瘤细胞耐药的问题,克隆出这种促使肿瘤细胞转移的异常突变变成了问题的关键,同时也表明,需要对循环肿瘤DNA进行全面的克隆,来帮助我们针对CRPC患者设计出更好的化疗及抗雄性激素治疗方案。比如,针对能够提高糖皮质激素类药物敏感性的AR-L702H突变开展研究就有可能为我们提供非常重要的信息和线索,让我们能够更好地将糖皮质激素类药物与enzalutamide联用。而且这也能够为使用abiraterone或enzalutamide与强的松(prednisone)联用方案的患者研究交叉耐药(cross -resistance)现象提供分子基础资料,也可以为使用抗雄性激素药物和多西他赛(docetaxel,是一种抗有丝分裂的化疗药)联用方案的患者研究交叉耐药现象提供分子基础资料,同时也有望能够预测这些治疗方案的预后情况。不过有一个问题值得我们考虑,即只对一个区域的CRPC细胞进行活检可能不太能够准确地反映体内整个转移病灶的整体异质性情况。另外,肿瘤细胞DNA进入人体循环系统的机制也还没有被彻底了解清楚,但是如图1所示,循环系统中的肿瘤DNA肯定是来自体内多个不同转移病灶的。
目前的工作还不太能够分辨我们观察到的克隆异质性究竟是源自原本从最开始就不同的各种肿瘤亚克隆细胞,还是因为随着疾病的发展,从最初的同一个因为体细胞的随机突变而产生的肿瘤克隆慢慢演变出了这么多种不同的亚克隆。我们还应该对这些前列腺肿瘤克隆进行连续的、动态的监测,了解其分子学变化情况,从中找出对肿瘤转移和致命性具有绝对影响意义的克隆,只有这样才能够明确该患者体内癌症的突变特点,然后据此找出最敏感的治疗药物,制定出最合适的治疗方案。科研人员已经开发出了多种经过人工遗传学改造过的实验小鼠,这些小鼠体内都带有一种独特的、与肿瘤复发相关的遗传变异,比如染色体数量减少、缺失(chromosomal losses)、染色体增多(chromosomal gains)、染色体重排(chromosomal rearrangements)、抑癌基因突变(mutations of tumor suppressor genes)或癌基因突变(mutations of oncogenes)等。通过对这些实验小鼠开展的临床前研究将有助于我们发现在前列腺癌的进展和转移过程中,肿瘤微环境(tumor microenvironment)对各种不同的、可以当作药物治疗靶点的癌变事件的影响和促进作用。搞清楚致命性转移克隆的原始来源也非常重要,因为这能够帮助我们了解肿瘤的演进历程,了解肿瘤细胞基因组改变(比如AR突变或PTEN缺失等)的先后顺序,在整个治疗过程中开展监测,随时掌握肿瘤细胞的变动情况,以免在出现耐药性之后继续使用已耐药药物。
转化医学的影响和意义
Carreira 等人开展的这项工作对于临床工作的意义在于,能够在基因组学水平上为临床治疗失败,以及产生耐药性找到原因,不仅能够为enzalutamide和 abiraterone等针对雄性激素的药物找到治疗失败的原因,同时也能够为化疗药物和糖皮质激素类药物的治疗失败找到原因。根据这些分子作用机制,我们能够设计出一套全新的患者管理模式,不论是使用能够激活AR突变体的抗微管蛋白的化疗药物,还是能够激活GR的糖皮质激素类药物,都可以根据对肿瘤 DNA的动态监测结果,在合适的时机选择最合适的药物,对患者进行最恰当、治疗效果最好的治疗。如图1所示,这种根据病程进展来选择治疗方案的策略会取得更好的治疗效果,比如在疾病晚期使用紫杉烷等化疗药物的效果就更好。这也提示我们,前列腺癌会随着病情的进展而不断发生演进,而这个过程很有可能如 Carreira等人发现的那样,是由多个不同的肿瘤克隆所导致的。由于并非在所有的进展期肿瘤克隆中都能够发现雄性激素受体发生遗传学改变,所以目前还不能肯定,这种对循环肿瘤DNA进行连续监测的方法是否适用于所有已经发生转移的前列腺癌患者。不过无论如何,该研究还是以非常明确的证据向我们表明,对转移克隆进行连续的、精确的、灵敏的监测才能够找到比AR更加致命的基因组学突变。
为了充分了解这些科学研究在临床上的应用价值,我们首先需要知道,目前的抗雄性激素治疗已经让存在CRPC细胞的前列腺癌转移患者的平均生存期达到了17个月。PREVAIL研究是针对在起始化疗药物治疗之前已经使用过enzalutamide治疗的前列腺癌转移患者开展的一项临床研究项目,该研究也发现,即便患者最终的预后非常差,但是抗癌治疗也取得了持续的效果。通过克隆测序研究发现,对于使用enzalutamide和糖皮质激素治疗的前列腺癌转移患者,继续治疗并不能阻止这些患者体内的肿瘤细胞继续突变,产生能够激活AR的特异性突变,所以继续治疗的意义不大。这种对某些肿瘤克隆产生的治疗选择压力(selection pressure)也为解决CRPC患者耐药问题的个性化治疗提供了空间。如果要了解前列腺癌在从疾病最初发的阶段,直到病情逐渐进展、转移、患者死亡的全过程中肿瘤的整体演进情况,就需要对原发灶、相应的转移灶、后续的多次循环肿瘤细胞样品进行基因组学和病理学方面的检测,并且需要对大量的人群,在他们如图1所示使用抗雄性激素药物和化疗药物(包括二线化疗药物)的同时开展上述这些工作。
前列腺癌属于死亡率最高的癌症之一。充分利用这些赋予转移肿瘤细胞“永生”能力的遗传突变,可以阻止疾病的发展,了解治疗的反应,延长患者的生命,提高患者的生活质量。对这些致命的转移肿瘤克隆开展严密的动态监视,就能够为治疗失败找到最好的解决之道。
-
焦点事件