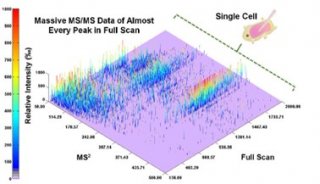
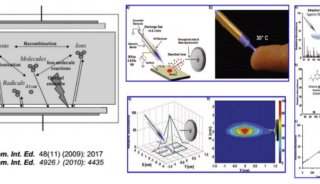
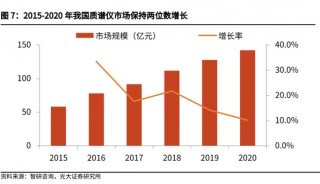
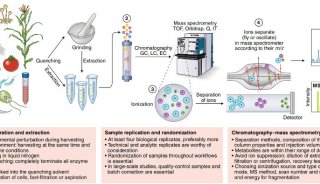
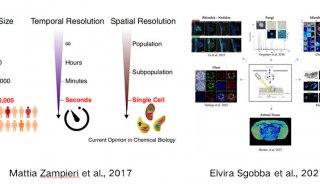
采用MassWorks对青霉素G新的微量代谢产物进行确证
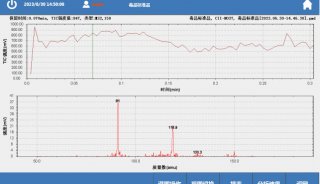
浙江大学用户与台湾中兴大学再次合作,在Rapid Commun. Mass Spectrom上发表文章《 Identification of new minor metabolites of penicillin G in human serum by multiple-stage tandem mass spectrometry》,采用MassWorks在四极杆质谱上测定了青霉素G的8种新代谢产物的精确质量数,并对血浆中微量代谢物进行了确证。
多级质谱确证人血清中青霉素G新的微量代谢产物
Hsin-Pin Ho1, Ren-Jye Lee1, Chung-Yu Chen1, Soo-Ray Wang2, Zu-Guang Li1,3 and Maw-Rong Lee1*
1 Department of Chemistry, National Chung Hsing University, Taichung 40227, Taiwan, R.O.C.
2 Department of Interncel Medicine, Chung Shan Medical University and Chung Shan Medical University Hospital,
Taichung 40201, Taiwan, R.O.C.
3 College of Chemical Engineering and Materials Science, Zhejiang University of Technology, Hangzhou 310014 Zhejiang, P.R. China
摘要:液相色谱质谱和液相色谱串联质谱法常被用于药物代谢物的研究。虽然这两种方法已经解决了代谢物鉴定及结构表征的分析,但是仍然是比较耗时的。本文中,一种新的多级串联质谱方法用于人血清中青霉素G的微量代谢产物-一种β-内酰胺抗生素的鉴定及结构表征的分析。青霉素G的七种微量代谢产物包括5种I相代谢产物和2种II相代谢产物通过应用LC-MSn数据分析方法而得到确证。青霉素G的七种代谢产物的精确质量数通过质谱校正软件(MassWorks)得到确证。本文的LC-MSn数据分析方法能够在代谢分析中提供微量代谢产物的丰富的、必要的结构信息。
前言
略
实验
化学试剂
所有化学试剂均为分析纯,青霉素G(99.7%)购自Riedel-deHae¨n(Sseelze,德国)。青霉素G的代谢产物青霉噻唑盐购自Sigma-Aldrich(St.Louis,MO,USA).色谱级的甲醇、乙腈、甲酸购自Merck(Darmstadt,德国)。用水为经过Milli-Q(大于18.2MΩ,Millipore,法国)净化的超纯水。青霉素G和青霉素噻唑盐储备液(1000 ug/ml)用高纯水制备。青霉素G和青霉素噻唑盐的混合工作液(100 ug/ml)用超纯水稀释到相应的浓度。储备液储存在0℃冰箱中。
体内血清样品的制备
略
色谱条件
液相色谱分离系统为LC1100(安捷伦科技,Santa Clara,CA,USA)带有二元泵和在线脱气装置。Phenomenex Luna C18柱和C18 预柱用于液相分离,流速为0.2 ml/min。流动相为0.1%甲酸水(A)和乙腈(B)。进样量5 ul,梯度洗脱程序如下:
| 时间(min) | 0.1%甲酸水(A) | 乙腈(B) |
| 0 | 95 | 5 |
| 1 | 95 | 5 |
| 27 | 20 | 80 |
| 41 | 20 | 80 |
| 42 | 95 | 5 |
| 50 | 95 | 5 |
质谱条件
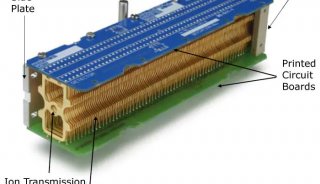
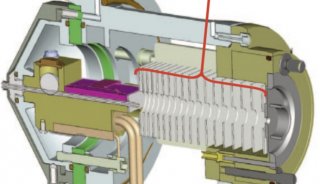
LTQ-线性离子阱质谱仪(Thermo,San Jose,CA,USA)带ESI离子源。将青霉素G和青霉素噻唑盐以10 ul/min的流速经流动注射泵直接注入ESI源得到质谱调谐条件,流动相为40%A,流速为0.2 ml/min,经T型管路与流动注射连接。优化的离子化及离子传输条件如下:鞘气流速为29arb,辅助气流速为5arb,喷雾电压为正离子模式4kv,毛细管温度为275℃,毛细管电压为41V,透镜电压为125V。在多级串联质谱中,质谱分析的参数如下:分离宽度为3.00Th,碰撞能量为25%,Q为0.25,激活时间为30ms。
数据分析条件
为了得到足够的结构信息,同时减少数据采集,设置LTQ的条件如下:(1)执行数据分析的筛查,对代谢产物进行检测;(2)设置选择性数据分析扫描方法;(3)得到母离子和中性丢失离子数据对代谢产物进行确证;(4)解析LC/MSn数据。
一个四项扫描设计用于数据分析的扫描。质谱扫描中,第一个扫描事件为全扫模式,扫描范围为148-1000m/z,第二个扫描事件为相关产物离子的MSn扫描,通过动态排除得到高于预设强度的大量的质谱峰。动态排除的参数为:重复3次,重复持续时间为30,排除列表的大小为100,排除持续时间为30。根据初步的数据分析,有针对的数据分析扫描能够得到目标代谢物的更多结构表征信息。
经过有针对性的数据分析扫描,在Xcalibur软件中多级质谱的色谱图上可以得到母离子和中性丢失离子的数据。母离子数据通过在MS2上提取特定的碎片离子而得到,中性丢失离子数据也是通过在MS2上提取中性丢失离子而得到。
精确质量数评估
开始采集数据前,进一针5ug/ml的包括青霉素G、青霉素噻唑盐、土霉素和玉米黄素的混合校正溶液。得到的轮廓图数据应用MassWorks软件(Serno,Bioscience,Monmouth)对不对称峰形和质量数进行校正。接着进实际样品。同样,LC/MS方法得到的轮廓图数据也应进行峰形和质量数的校正。最后,基于精确质量数和谱图准确度得到所有可能的分子式。
结果讨论
青霉素G和青霉素噻唑盐的碎片
略
体内代谢分析
略
精确质量数测定
单位质量分辨率质谱对定性分析仅提供粗略的质量确证,因此需要精确质量数测定。本文采用MassWorks软件确证检测的代谢产物的分子式。结果如表2所示。质量误差小于25.5mDa。质量精度在96.1%-99.2%范围内。由于外部校正的应用和可能的空间效应对离子阱的影响,目标代谢产物的质量误差仅能控制在50 mDa内。良好的同位素轮廓图校正提供的信息能够对目标物分子式进行确证。
表2 青霉素G及其代谢物的精确质量数
| 代谢产物 | [M+H]+分子式 | 理论质量数(Da) | 测定质量数(Da) | 质量误差(mDa) | 谱图准确度 |
| 母体药物 | C16H19N2O4S | 335.1066 | 335.1187 | 12.1 | 98.1 |
| 青霉素噻唑盐(M1) | C16H21N2O5S | 353.1171 | 353.1342 | -17.1 | 97.8 |
| 青霉素吡唑酸盐(M2) | C15H21N2O3S | 309.1273 | 309.1121 | 15.2 | 96.7 |
| M3 | C19H25N2O7S | 425.1382 | 425.1459 | -7.6 | 98.1 |
| M4 | C19H27N2O7S | 427.1539 | 427.1619 | -8.0 | 99.2 |
| M5 | C16H21N2O6S | 369.1120 | 369.1247 | -12.7 | 97.7 |
| M6 | C22H29N2O11S | 529.1492 | 529.1747 | -25.5 | 98.9 |
| M7 | C22H31N4O8S3 | 575.1304 | 575.1495 | -19.1 | 96.1 |
青霉素G的代谢途径
略
实际样品检测
略
结论
略
如对中文文章感兴趣,请联系北京绿绵科技有限公司市场部 弓俊杰:15011512780 ,010-82676061 ,junjie_gong@lumtech.cm.cn
-
企业风采

-
招标采购

-
标准

-
焦点事件

-
焦点事件

-
标准

-
企业风采

-
焦点事件

-
标准

-
综述

-
投融资

-
企业风采

-
企业风采

-
会议会展

-
会议会展

-
焦点事件
-
企业风采

-
会议会展

-
企业风采

-
企业风采
-
产品技术

-
精英视角

-
精英视角

-
精英视角

-
焦点事件

-
焦点事件

-
精英视角

-
产品技术

-
企业风采

-
精英视角

-
会议会展

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
企业风采

-
精英视角

-
企业风采

-
精英视角

-
会议会展

-
焦点事件

-
企业风采

-
焦点事件

-
产品技术
-
产品技术

-
企业风采

-
焦点事件

-
焦点事件

-
企业风采

-
产品技术

-
焦点事件

-
焦点事件
-
企业风采

-
企业风采

-
企业风采

-
项目成果
-
企业风采

-
会议会展

-
企业风采

-
企业风采

-
项目成果
-
会议会展

-
焦点事件

-
企业风采

-
焦点事件

-
精英视角

-
企业风采

-
企业风采

-
会议会展

-
投融资

-
综述

-
产品技术

-
精英视角

-
产品技术

-
精英视角

-
精英视角

-
企业风采

-
会议会展

-
会议会展

-
项目成果
-
焦点事件

-
会议会展

-
焦点事件

-
焦点事件
-
投融资

-
并购

-
焦点事件
-
焦点事件

-
精英视角

-
焦点事件

-
焦点事件
-
会议会展

-
会议会展

-
会议会展

-
焦点事件

-
企业风采

-
焦点事件

-
产品技术

-
产品技术

-
焦点事件

-
综述
-
焦点事件

-
精英视角

-
精英视角

-
技术原理
-
会议会展

-
精英视角

-
企业风采