纳米孔直接RNA和cDNA长读长测序概述
RNA测序已经在生物学和医学的各个领域取得了前所未有的发展。在包括癌症在内的诸多疾病中,转录异构体的表达和用途是健康组织和患病组织之间变异的重要来源。鉴定差异剪接的异构体和融合转录本,可以为疾病的诊断和治疗提供信息。RNA测序还有助于揭示从单细胞到整个组织的转录组动力学。同时,cDNA测序也极大地辅助了病毒性病原体的表征和及时检测。
毫无疑问,传统的测序技术使全面转录组分析成为可能,并带来了很多重要的科学发展。然而,这一领域仍有重要的局限性有待解决。
转录本的长度通常为几千碱基对,这使得现有的短读长序列仅能部分覆盖转录本的长度,因此依赖计算重构准确的异构体组装非常困难,短读长也表现出高比率的多重定位。
基于测序的RNA分析均需要将 RNA转化为互补DNA(cDNA)链,在这一过程中,逆转录或扩增可引入偏倚,产生GC偏好性。由于并非所有的转录物都以相同的效率扩增,会导致一些种类的RNA的中断以及其它种类RNA的过度扩增。重要的是,在PCR 扩增过程中会丢失有关碱基修饰的所有信息。
随着长读长测序技术的发展,越来越多的国内外科学家将目光转向了由英国Oxford Nanopore公司开发的纳米孔测序技术。与其它基于光学原理的合成测序法不同,纳米孔测序是通过将蛋白质纳米孔嵌入电阻膜,并使离子电流通过纳米孔。当像DNA或RNA这样的分子穿过纳米孔时,会对电流带来干扰。该信号会被实时分析,用来确定正在通过纳米孔的DNA或RNA链的碱基序列。
纳米孔技术是唯一可以进行直接DNA与RNA测序的技术,当前最长读长已达2Mb 。此外,与在测序运行完成后开始数据分析的传统测序方法不同,纳米孔测序实时运行,可在测序进行中对读长进行碱基识别和分析,从而显著缩短从拿到样本到出检测结果的时间。一旦生成了足够的数据,例如达到覆盖度目标,可以立即停止运行。

在这里,我们将介绍和回顾几篇发表的文章,讨论应用纳米孔技术进行全长转录本识别、异构体表达和定量、以及病毒检测。
Nanopore长读长RNA测序揭示个体B细胞表面受体之间广泛的转录变异
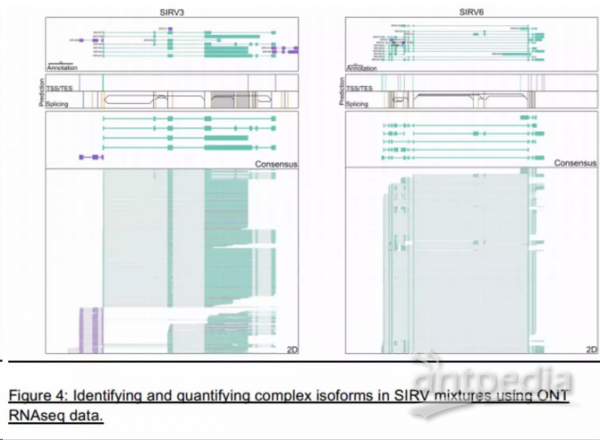
早在2017年,由Byrne等人发表于《自然通讯》的一篇文章中【2】,作者研究了使用长读长单分子Oxford Nanopore MinION测序仪的RNA测序是否能够在不牺牲准确的基因表达定量的情况下,鉴定和定量复杂的异构体。
在对方法进行基准测试后,Byrne等人使用定制的混样建库策略分析了单个小鼠B1a细胞。作者在这些B1a细胞中鉴定了数千个未注释的转录起始和终点位点,以及数百个可选择的剪接事件。同时还鉴定了在B1a细胞中表达的数百种基因,这些基因显示出多种复杂的异构体,包括几种B细胞特异性表面受体。
Byene表示,他们的数据结果可以在单细胞水平上识别和量化复杂的异构体。使用Oxford Nanopore Technologies MinION测序仪的RNA测序研究有可能重新定义单个RNA测序实验收集的信息水平。作者表示:“纳米孔RNA测序在单细胞水平上测序全长转录本的能力真正突出并证实了IGH基因座的特殊转录多样性”。
使用纳米孔直接RNA测序解读16S核糖体RNA中的经典和修饰的核苷酸
在另一篇Smith等人(2017)文章中,作者使用纳米孔直接RNA测序对16S核糖体RNA中的经典和修饰的核苷酸进行了解析【3】。
核糖体小亚基在所有活细胞中表达。它在翻译过程中发挥了许多基本功能,包括起始复合物的形成和mRNA密码子与tRNA反密码子之间碱基对的校对。小核糖体亚基的核心成分是原核生物中~1.5kb的 RNA链(16S rRNA)和真核生物中的同源~1.8kb RNA链(18S rRNA)。
传统的rRNA基因或rRNA cDNA拷贝的合成测序(SBS)已广泛用于系统发育研究和临床鉴定传染性生物。然而,通过SBS的方法移除了rRNA的表观遗传修饰信息。纳米孔测序的一个显着优势,是可对天然DNA和RNA进行直接分析可以解析碱基修饰。
Smith等人利用纳米孔MinION测序仪,直接对单个全长16S rRNA进行了无逆转录或扩增的测序。作者在文章中提出并回答了三个问题:
1)碱基修饰是否会引起离子电流改变?
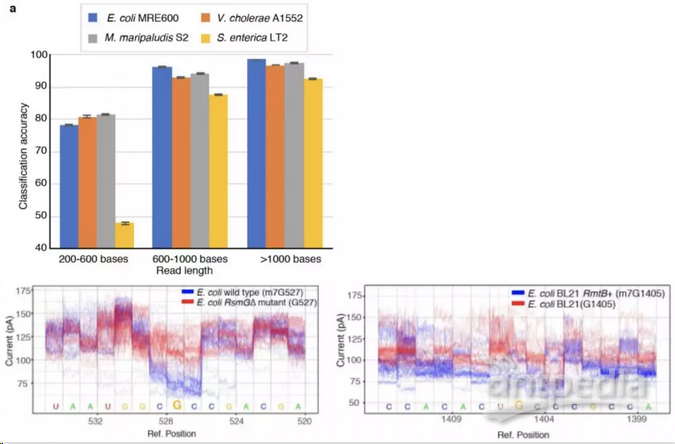
改造后的菌株呈现“有能力”和“无能力”显示特定的甲基化特征。有能力的菌株显示出一致的可再现的碱基识别误差,无能力的菌株识别正确。偏离规范模式的纳米孔离子电流轨迹揭示了保守的16S rRNA碱基修饰,以及引起氨基糖苷类对一部分病理性大肠杆菌菌株产生抗性的7-甲基鸟苷修饰。这种直接RNA测序技术有望快速鉴定环境和患者样本中的微生物。
2)分类的精度是否会随读长长度增加?
分类准确度随测序长度从短读长(200-600bp)的67.9%增加到长读长(> 1000bp)的96.9%。读长更长=更好的分类准确性(如下图所示)。
3)是否能够从人类总RNA背景中选择性地测序16S rRNA?
成功在4.5微克的总人RNA中检测到了少至5皮克(~10阿托摩尔)的大肠杆菌16S rRNA。表明可在2小时内从复杂的临床或环境样本中检测到微生物16S rRNA。
对编码完整甲型流感病毒基因组的直接RNA测序
传统的RNA测序方法,RNA通常通过将其逆转录为cDNA进行间接测序,cDNA通常通过PCR扩增为dsDNA,然后使用多种DNA测序方法进行分析。
Keller等人(2018)使用纳米孔技术,首次以其天然形式对编码完整的RNA病毒基因组进行了测序【4】。作者针对甲型流感病毒基因组的高度保守末端设计了一种接头,使用这种修饰的将(-)RNA靶向Oxford Nanopore MinION测序平台上的蛋白质纳米孔。作者证明了对编码完整甲型流感病毒基因组的成功测序,具有100%核苷酸覆盖率,99%共识一致性,99%的读长定位到甲型流感病毒。该方法还具有识别和量化剪接变体和碱基修饰的潜力,而这些变体和碱基修饰实际上在使用当前其它方法中是无法测量的。
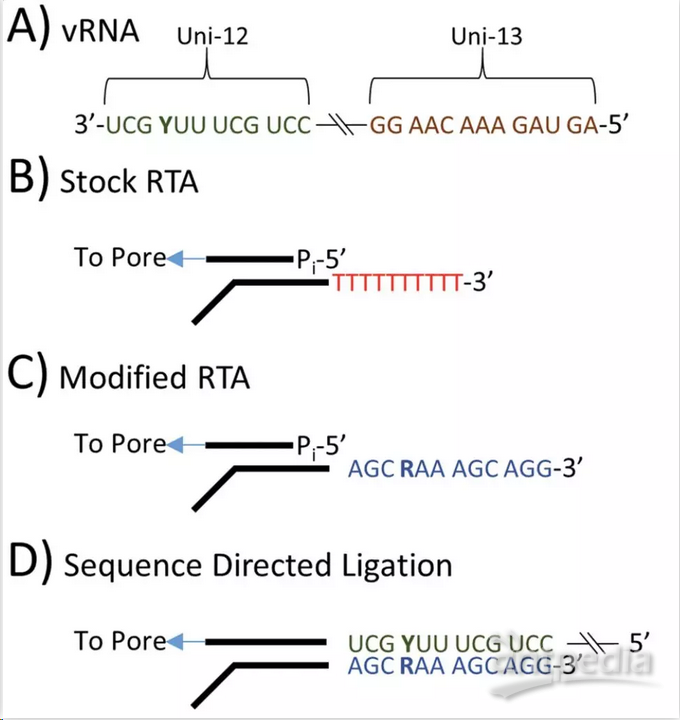
(A)甲型流感病毒在3'和5'末端含有高度保守的12和13个核苷酸序列。(B)Oxford Nanopore直接RNA测序的关键组分是逆转录酶接头(RTA),其标靶poly(A)mRNA并连接到mRNA的3'末端。然后将测序接头连接到RTA,RTA将RNA链导入孔中用于测序。(C)修改RTA以标靶甲型流感病毒基因组的3'保守12nt。(D)修饰的RTA在直接RNA测序的第一步中与vRNA杂交并连接。
纳米孔直接RNA测序揭示全长冠状病毒基因组的修饰
Viehweger等人(2018)使用全长、直接RNA测序方法,不经过任何扩增步骤,来表征感染人类冠状病毒的细胞中产生的病毒RNA 【5】,所述人类冠状病毒代表迄今已知的最大RNA病毒基因组之一。
使用来自感染冠状病毒的细胞的总RNA,在便携式测序仪MinION的两张芯片上进行了直接RNA测序,获得最长读长为26 kb(基因中大小为27.3 kb)并成功比对到病毒参考基因组,冠状病毒基因组覆盖率达到99.86%。使用不需要组装步骤的长读长,作者在受感染的细胞中鉴定出仍有待表征的多种新型HCoV-229E sg RNA。由于该方法不需要RNA的逆转录和扩增,作者能够检测病毒RNA中的甲基化位点。我们的工作通过证明样品内单倍型分离的可行性,为基于单倍型的病毒准种分析铺平了道路。
参考文献
1.使用Oxford Nanopore的cDNA测序指南
https://nanoporetech.com/cn/resource-centre/guide-cdna-sequencing-oxford-nanopore-cn
2. Byrne etal., Jul 2017, Nature Communications, Nanopore long-read RNAseq reveals widespread transcriptional variationamong the surface receptors of individual B cells.
https://doi.org/10.1038/ncomms16027
3. Smith etal. 2017. BioRxiv, Reading canonical and modified nucleotides in 16Sribosomal RNA using nanopore direct RNA sequencing.
https://doi.org/10.1101/132274
4. Keller etal., Sep 2018, Scientific Reports, DirectRNA Sequencing of the Coding Complete Influenza A Virus Genome.
https://doi.org/10.1038/s41598-018-32615-8
5. Viehweger etal., 2018, BioRxiv, Nanopore directRNA sequencing reveals modification in full-length coronavirus genomes.
https://doi.org/10.1101/483693
6. 纳米孔测序白皮书: 无偏倚全长转录本的价值。
链接:https://nanoporetech.com/cn/resource-centre/wupianyiquanzhangzhuanlubendejiazhi