λ噬菌体的局限性转导实验
λ噬菌体是一种温和噬菌体,在大肠杆菌宿主细胞内其DNA可整合在宿主染色体上,如同细菌的基因一样传递给子代细胞,此为溶原状态。在溶原菌中,λ噬菌体有两种选择:①溶原生长:即继续维持其溶原状态;②裂解生长:在某些物理化学等因素的诱导下,λ噬菌体借助宿主细胞的酶系统,开始有序的复制、转录、表达,装配成完整的噬菌体颗粒,最后裂解宿主细胞,释放出大量具有感染能力的成熟噬菌体。紫外线是一种常用物理诱导因素。不过,当溶原菌(供体菌)经紫外线诱导产生的噬菌体颗粒中极少数(约10-4)带有细菌gal基因,而噬菌体则失去自身的部分DNA片段时,这种噬菌体称之为缺陷噬菌体,用λdg表示。这种噬菌体所进行的转导为低频转导(lowerfrequencytranslocation,LFT)。用这种低频转导噬菌体裂解液以高感染复数(HIF)感染另一非溶原性gal-受体菌,λdg不仅能进入细胞,而且能和正常λ噬菌体一起整合到受体细胞染色体上去,使之成为双重溶原菌。双重溶原菌经诱导后,噬菌体同样能复制并释放出约占噬菌体总数50%的具有半乳糖发酵基因能力的噬菌体。这些转导噬菌体所进行的转导称为高频转导(HFT)。来源:《遗传学教程》
| 实验方法原理 | 本实验以含原λ噬菌体和缺陷噬菌体λdg的双重溶原菌gal+作为供体,经紫外线诱导后,获取能转导半乳糖发酵基因的高频转导噬菌体裂解液,然后让这些转导噬菌体将gal+基因转移到受体菌gal-中去。 |
|---|---|
| 实验材料 | 供体菌 : Escherichia coli K12 F2 gal + (带有原噬菌体λ和缺陷噬菌体λdg)受体菌 : E . coli K12 S gal - |
| 试剂、试剂盒 | LB液2×LB液YT液体培养基YT半固体培养基YT固体培养基9皿EMB-gal培养基11皿pH7.0的磷酸缓冲液生理盐水氯仿 |
| 仪器、耗材 | |
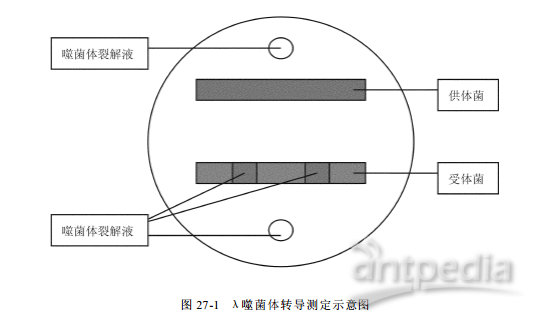
| 实验步骤 | (一)噬菌体裂解液的制备 1.将供体菌接入5mlLB培养液中,37℃振荡培养过夜。 2.取0.5ml过夜培养物转入另一支5mlLB培养液试管中(剩余的菌液置冰箱保存,备用),37℃继续培养4~6h。 3.将培养物转入10ml无菌离心管中,4℃3000r/min离心10min。 4.去上清液,加1ml的磷酸缓冲液(0.1mol/L,pH7.0),振荡悬浮,再加入4ml同样的缓冲液制成菌悬液。 5.取2ml菌悬液于无菌培养皿(Φ6cm)中。在红光下将含有菌悬液的培养皿置紫外灯(15W)40cm处,打开培养皿盖照射10s(边照射边搅拌),然后加入2×LB液2ml,混匀后置37℃避光培养2~3h。 6.将上述暗培养液转入无菌大试管中,加入5~8滴氯仿,剧烈振荡30s,室温静置5min后转入另一支无菌离心管,再经4℃,3000r/min离心10min。 7.小心将上清液吸取转入另一无菌试管中,上清液即为λ噬菌体裂解液。裂解液中加入一滴氯仿,混匀后置4℃保存,备用。 (二)噬菌体效价的测定 1.将受体菌接入5ml培养液(补加麦芽糖和MgSO4),置37℃振荡培养过夜。 2.取0.5ml过夜培养物于另一支5mlYT培养液(同样加麦芽糖和MgSO4)试管中(其余的受体菌液置4℃保存,备用),37℃继续振荡培养3~4h。 3.将噬菌体裂解液用YT培养液稀释至10-7,分别取10-5、10-6、10-7稀释液0.1ml于无菌试管中,再加入0.1ml受体菌液,混匀后置37℃保温15~20min,然后倒入4.5ml半固体YT培养基(培养基温度约为45℃),混匀后,迅速倒入底层YT培养基的平板中。按此操作每稀释度制3皿,待凝固后置37℃培养过夜。 4.观察出现的噬菌斑,计算裂解液中噬菌体的效价。 (三)转导试验 1. 取EMB-gal平板二皿,在平板底部按图27-1画上标记。
2. 取保存的受体菌液少许涂成一条带,再取保存的供体菌液少许在另一区域涂一条带。待干后在两个圆圈和两个方格内各滴一小滴噬菌体裂解液(先滴两圆圈内,后滴方格内),置37℃培养48h。 3. 观察平板上形成的噬菌体,统计噬菌斑形成单位数(PFUs),并计算λ噬菌体裂解液的效价。 4. 图示转导试验结果,确定是否出现转导现象。 展开 |
| 注意事项 | 1.配制半固体培养基时,使用琼脂粉为宜。琼脂的浓度为0.45%~0.5%。 2.噬菌体裂解液与受体菌液混合保温期间切勿摇动试管,以免影响噬菌体的吸附,使其效价偏低。 |
| 其他 | 实验试剂: LB 液 ( 5ml/ 试 管 2 支 ; 4. 5ml/ 100ml 三角 瓶 1 瓶 ) , 2× LB 液 ( 2ml/ 小 试 管 1 支 ) ,YT 液体培养基 ( 4. 5ml/ 试管 1 支 ; 4. 5ml/ 试管 7 支 ; 4 .5ml/ 100ml 三角瓶 1 瓶 ) , YT 半固体培养基 (4 .5ml/ 试管 9 支) , YT 固体培养基 9 皿 ( 本实验中 YT 培养基均补加麦芽糖和 MgSO4 , 终浓度分别为 1 % 和 10mmol/ L) , EMB-gal 培养基 11 皿 , 0 .1mol/ L pH7. 0 的磷酸缓冲液 ( 4ml/ 试管 1 支 ) , 生理盐水 (4 .5ml/ 试管 3 支 ) , 氯仿。 展开 |