PPTD2018会议科普:抗体标准化
——胡志上(中国计量科学研究院)
单抗是目前最成功的一类生物制品,最近20年发展迅猛,目前已有超过300种单抗处于临床试验阶段,批准上市的单抗数量超过50种,到2020年销售额有望超过1250亿美元。治疗性单克隆抗体制品被广泛批准应用于肿瘤、自身免疫、器官移植和感染性疾病等多个适应症的治疗中,疗效显著、利润丰厚,所以越来越多的企业投入到单抗的开发和生产中来。另一方面,随着一大批疗效明确的单抗药物ZL即将到期,许多医药企业通过生物仿制药的方式加入到单抗制品的开发行列中。
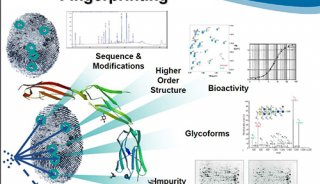
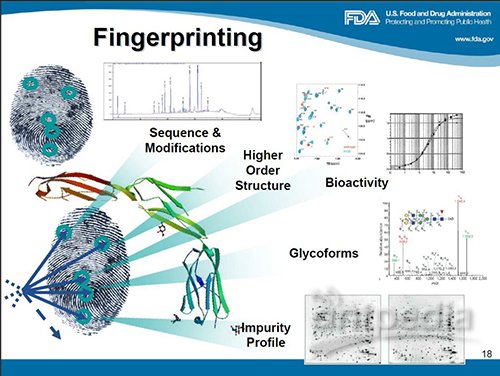
由于治疗性单克隆抗体制品本身结构和生产工艺的复杂性(比如:对单抗分子化学结构与其安全性和有效性间的关系缺乏深入了解),使得单抗类制品质量分析和控制的难度较大。大量治疗性单克隆抗体制品的研发和上市,又催生了单抗成药性分析和工艺优化评价的巨大需求。从国际上看,大批新方法、新标准的出现和应用大大促进了单抗质量控制技术的发展。大型药企基本都有完备的质量分析平台。美欧在单抗质量分析方面的研究也居于世界领先地位。美国标准技术研究院(NIST)与美国食品药品监督局(FDA)合作,已经研制、发布了一种IgG标准物质,针对它投入了大量的人力物力进行单抗质量分析标准化研究。而对于国内药企来说,一方面需要直面领先国家的贸易、技术壁垒,在控制成本的基础上实现新研和仿制的单抗类药品的安全、有效、质量可控;另一方面又缺乏人力、物力和财力去建立、维持足够强大的质量分析团队,这个矛盾在很大程度上限制了国内药企的发展壮大。目前国内药企很多时候主要靠CRO公司的服务满足申报阶段的需要,影响了研发效率。如果有更多的政府和市场机构帮助提升自主产权单抗药物的数量、质量以及相关技术能力,使之与国际水平接轨,将有利于推动我国医药产业的结构调整和转型升级,提升国家竞争力。
举例来说,单抗类制品的检验需求主要存在于新品种注册和生产工艺放大、转移和变更中,体现为成药性分析和工艺效果的评价。比如:生产工艺的变更可能会改变产品的序列、结构、内在均一性和各种结构所占的比例等,最终对产品的有效性和安全性产生影响。计量学是研究测量及其应用的科学,目标是保证全球范围内的质量检测活动单位统一、量值准确,通俗地说就是不能测的想办法测、能测的要保证结果准确、除此之外还要建立完善国际国内贸易中质量检测结果的等效互认体系。中国计量科学研究院是中国的国家计量院,保存着我国的计量基准和最高测量能力,相当于美国的NIST。NIST与企业和FDA合作,在单抗类药物安全性和有效性评价相关测量技术的研究及标准化方面发挥了重要的作用,咱们中国计量科学研究院也有能力、有义务在国内发挥相应的作用。我们关注单抗类药品质量分析技术标准化研究,希望能建立相应的模型与平台,找到并针对一些关键指标,在单抗类药品质量分析中建立量值溯源性。通过研制高准确度测量装置、方法和可溯源的标准物质,提高测量结果的准确度,建立科学、精确的表征、评价体系,以支撑单抗类药品的安全性、有效性评价和质量提升,服务产业发展。
PPTD会议简介:
蛋白和肽类药物及诊断试剂的有效性评价和质量的精确控制是目前全球生物产业面临的巨大挑战之一,是企业研发的重点,是标准化工程化开发的前提。为推动体外诊断与肽类、蛋白质药物工程化发展,加强计量及分析表征技术对该领域质量控制及标准化的支撑,更好地促进我国体外诊断与肽类、蛋白质药物研发生产等相关技术交流,中国计量科学研究院、国际计量局(BIPM)、成都市人民政府、中国食品药品检定研究院联合主办了2016年“蛋白和肽类药物及诊断试剂研发与质控国际研讨会(PPTD 2016)”。国际计量局、国际检验医学溯源联合委员会(JCTLM)、世界卫生组织(WHO)、国际临床化学联合会(IFCC)等国际组织,及多国计量院和世界著名生物医药企业的30余名代表和中国科学院、中国工程院、相关科研院所、高校和企业的约450名国内代表参加了会议。与会代表以计量技术为桥梁,对前沿研究、药物研发、临床医学检验技术及标准化等研究热点展开了交流。本次研讨会促进了生命科学计量新领域的发展,加强了世界各国、各组织在化学生物计量领域的交流与合作,建立了蛋白和肽类药物前沿研究与工程化转化的桥梁与纽带;同时为研发、质控、科技创新以及产业化等全链条合作奠定了基础,在国际上获得了广泛赞誉。
-
科技前沿
-
会议会展