Nature发现触发细胞死亡机制:“左手杀手”
Z型核酸(Z-DNA)是具有不寻常的左手双螺旋结构的双链DNA和RNA分子,与经典的右手Watson-Crick双螺旋相反。这种核酸是40多年前发现的,但迄今为止,我们对其生物学功能的了解仍然很少。
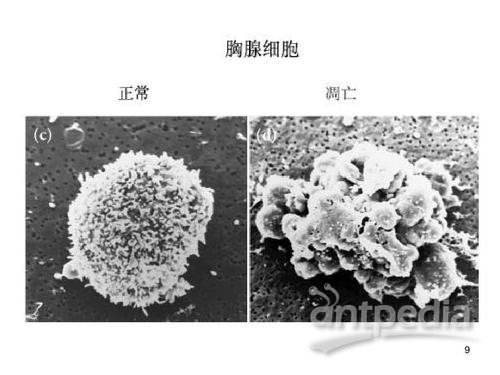
德国科隆大学CECAD衰老研究所的Manolis Pasparakis教授,与德州大学健康科学中心等处的科学家合作,研究了Z-DNA结合蛋白1( ZBP1),这是哺乳动物中已知与Z核酸相互作用的仅有的两种蛋白质之一。以前显示ZBP1可以感测某些病毒的遗传物质,并诱导感染细胞死亡以防止病毒传播。
但是奇怪的是,在他们较早的研究中,研究人员获得的证据表明,在没有病毒感染的情况下,ZBP1还可引起细胞死亡和炎症。他们发现,当RIPK1(一种抑制ZBP1的蛋白)的功能受损时,ZBP1被激活并引发炎症性细胞死亡,这被称为细胞坏死(necroptosis)。
最新研究背后的一个关键问题是在没有病毒感染的情况下如何激活ZBP1。研究人员利用实验小鼠模型,发现ZBP1的促炎活性取决于其与Z核酸结合的能力,这表明ZBP1被细胞内存在的Z型核酸激活。下一个问题是ZBP1结合哪种类型的内源核酸。Pasparakis说:“我们可以证明ZBP1与双链RNA结合。” “尽管我们目前缺乏实验方法来证明其具有Z构象,但基于所有可用的结构研究,我们对结果的解释是ZBP1通过其Za结构域与内源Z-RNA结合。”
双链RNA(dsRNA)在细胞中并不常见,但会在某些病毒基因组的复制过程中形成,并被认为在病毒感染期间提供了激活ZBP1的配体。科学家们推测,细胞dsRNA可以通过内源性逆转录因子产生,内源性逆转录因子是来自古代逆转录病毒感染或活性逆转录转座子,以及“跳跃基因”,后者构成了人类和小鼠一半以上的基因组。
为了了解内源性逆转录元件作为dsRNA来源的可能作用,Manolis Pasparakis团队与Francis Crick研究所的George Kassiotis逆转录病毒免疫学实验室合作。他们发现实际上,对来自小鼠皮肤的RNA测序数据的计算分析表明,大多数互补的,推测为双链的RNA均来自特定组的内源性逆转录元件。
这些发现表明,感知细胞dsRNA(大部分源自内源性逆转录元件)激活ZBP1,诱导细胞死亡和炎症,这一机制可能与人体炎症性病理的发病机制有关,尤其是在具有抑制ZBP1的蛋白质(例如RIPK1)突变的患者中。
作者指出,“ Z-DNA多年来一直保持着神秘感。目前,我们研究其功能的唯一方法是研究能感知其功能的蛋白质。我们取得了一些进展,但是未来还有许多挑战,比如了解它们为什么,在何处以及如何在一个细胞内形成以及其目的是什么。”
一个特别令人着迷的方面是与内源性逆向元件的联系。 “目前对这些基因组附件如何影响我们的健康,知之甚少。似乎在进化过程中,一些可以模仿病毒感染的逆转座子被招募为有用的伙伴元件,应对细胞对损伤,压力或真正感染的反应,但这种伙伴关系也可能出错,导致疾病。”
就像在病毒感染期间一样,ZBP1感知内源性逆转录因子产生的Z-RNA,这可能会为细胞死亡和炎症提供有效的诱因,导致疾病。不过这些研究还处于初期阶段,我们还有很长的路要走,未来了解其机制将有助于研发人类疾病新疗法。
-
科技前沿

-
技术原理
-
项目成果
-
焦点事件












