首都医科大学最新文章取得关键因子研究进展
来自首都医科大学宣武医院,教育部神经变性病学重点实验室的研究人员针对一种关键的作用因子:胶质源性神经生长因子(glial cell derived neurotrophic factor, GDNF)展开研究,实现了人胚胎神经干细胞GDNF在体外培养条件下的表达调控,这对于帕金森病等神经退行性疾病的治疗具有意义。
领导这一研究的是首都医科大学张愚教授,张教授在美国西北大学攻读博士学位期间,曾发现了第一个同时在胚胎分节和神经分节中起关键作用的“分子开关”,2001年回国后,张教授担任首都医科大学宣武医院细胞治疗中心主任,主要从事干细胞基础及临床应用方面的研究,先后在《Nature》、《Neuron》、《Development》等国际期刊发表SCI学术论文多篇。
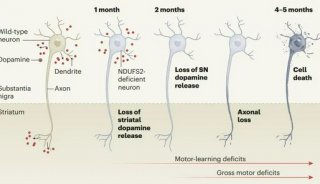
胶质源性神经营养因子(glial cell derived neuro-trophic factor, GDNF)对多巴胺能神经元有特异性的营养作用。帕金森动物模型实验和临床研究都表明,在纹状体中注入GDNF能够阻止黑质多巴胺能神经元发生神经退行性变,并促进其轴突生长。
但由于GDNF作为一种大分子蛋白难以通过血脑屏障,因此其在临床应用方面的效果一直不尽人意。目前已发现的几种将GDNF应用于帕金森病治疗的方法中, 以细胞作为载体将GDNF注入病变部位被认为是一种最为有前景的方案。
由于人胚胎神经干细胞在体外分化和移植入动物模型脑内都具有分化成为神经元, 星形胶质细胞和少突胶质细胞的能力, 并能够很好的整合入移植宿主的脑区, 因此被认为是进行神经体统修复和细胞替代治疗的理想选择。
在这篇文章中,研究人员利用含有GDNF基因的可调控慢病毒载体,转染人胚胎神经干细胞, 实现了GDNF在人胚胎神经干细胞在体外培养条件下的表达调控。
研究人员首先利用含有GDNF基因的慢病毒载体成功转染人胚胎神经干细胞, 其中GDNF基因受四环素操纵子 7(tetracycline operator 7, tetO7)调控, 由延长因子 1(elongation factor 1, EF1-α)驱动。转染后的神经干细胞,经过潮霉素筛选后,同时转入对下游基因起抑制作用的慢病毒载体 TTS(tetra-cycline repressor fusion protein, TTS), TTS蛋白表达后可与tetO7相互作用抑制GDNF在人神经干细胞中的表达。
研究人员发现,当加入强力霉素(doxycycline, DOX)后, TTS与tetO7解离,GDNF表达可恢复到未调控前水平,并且转染GDNF后的人胚胎神经干细胞仍然表达神经干细胞特异性抗原 nestin, Sox2。放线菌素D诱导凋亡后, 转染GDNF组较正常对照组凋亡细胞比例有显著降低,同时, 转染 GDNF 的神经干细胞分化成神经元的比例有显著提高。利用可调控的慢病毒调控GDNF在人胚胎神经干细胞中的表达为GDNF应用于神经退行性疾病的治疗提供了实验数据。
鉴于GDNF对黑质多巴胺能神经元的营养功能和保护作用, 很多研究小组都在试图寻找一种安全而有效的方法使 GDNF 能够避开全身应用难以通过血脑屏障的局限直接作用到受损脑区, 这种方法应同时能对 GDNF 的作用剂量和作用时间进行调控,以避免过量的应用带来的副作用,与脑组织具有良好相容性的神经干细胞载体被认为具有很好的应用前景。
这项研究表明,利用可调控的慢病毒载体可以严格调控 GDNF 基因在人胚胎神经干细胞中的表达。实验结果提示, GDNF分泌量和转染拷贝数成正相关, 即通过控制人胚胎神经干细胞感染过程中含 GDNF基因慢病毒载体的病毒颗粒数,来控制 GDNF 的总体分泌水平,可以作为利用细胞载体携带GDNF时, 选择合适 MOI 值和控制合适剂量的参考依据。
-
焦点事件

-
科技前沿

-
科技前沿

-
科技前沿
-
科技前沿
-
项目成果

-
焦点事件

-
科技前沿
-
科技前沿

-
科技前沿
-
科技前沿
-
科技前沿
-
市场商机
-
科技前沿

-
项目成果
-
科技前沿
-
科技前沿

-
科技前沿

-
科技前沿

-
科技前沿

-
科技前沿
-
科技前沿
-
科技前沿

-
科技前沿
-
技术原理

-
项目成果
-
项目成果

-
焦点事件

-
项目成果

-
项目成果
-
焦点事件

-
科技前沿
-
项目成果

-
项目成果
-
项目成果

-
项目成果
-
项目成果
-
焦点事件

-
项目成果

-
项目成果
-
项目成果
-
项目成果
-
科技前沿
-
科技前沿
-
项目成果

-
项目成果
-
项目成果
-
项目成果

-
项目成果
-
项目成果

-
焦点事件
-
焦点事件

-
项目成果
-
项目成果

-
项目成果
-
项目成果
-
项目成果

-
焦点事件
-
科技前沿

-
项目成果
-
项目成果
-
科技前沿

-
项目成果
-
焦点事件

-
科技前沿

-
科技前沿

-
科技前沿