抗体偶联药物(ADC)浅析(二)
目前,ADC药物采用人源化单抗,对可结晶片段(Fc)进行修饰,以降低ADCC和CDC等。首先抗体分子作为生物大分子,存在一般生物大分子的毒性风险,如免疫原性和免疫毒性,以及单抗可能的ADCC作用、CDC作用、肾基底膜免疫复合物沉积等。其次,在ADC药物中,抗体分子最重要的作用是靶向作用,即将小分子化合物定向投递到抗原抗体结合位点。如果抗体选择性较差或正常组织存在该抗原,则会造成细胞毒药物投递到正常细胞中,造成靶向毒性。因此在ADC的研发中正确的选择抗体尤为重要。

图3、ADC抗体[8]
ADC的发展史
抗体药物的研发技术一直在不断更新换代,ADC的研究可以追溯到1980年,但是直到2000年,首个抗体偶联药物才被FDA批准用于治疗急性粒细胞白血病,但由于致死性的毒性的产生,于2010年撤市。随着原有技术的改进,研究人员开发了新型抗体偶联药物,并于2011年被FDA批准用于治疗霍奇金淋巴瘤和系统性间变性大细胞淋巴瘤。2013年抗体偶联药物再次取得突破,Genentech/ImmunoGen联合开发的Ado-trastuzumabemtansine被FDA批准用于HER2阳性乳腺癌,这是首个针对实体瘤的抗体偶联药物。随着这两个药物的研发成功,ADC药物再次以火热的状态进入人们的研究视野。
第一代ADC
在第一代ADC药物中,主要通过不可降解的连接子与小鼠单克隆抗体结合,药效和活性均较低。
第一代ADC药物失败的原因有很多因素,首先就是药物效力不足,血液中药物浓度低于治疗有效浓度,而靶点抗原低表达又导致药物递送量少,细胞内药物不足以杀死细胞。其次,初代ADC药物对肿瘤的靶向性不强,定位率低,而当时使用的连接子也不稳定,以致于药物毒性较大。最后,由于早期ADC中单克隆抗体是鼠源而不是人源化抗体,导致免疫反应和人抗鼠抗体(HAMAs)的产生。以上都是第一代药物失败的因素,但是研究永无止境,很快第二代ADC药物进入人们的视野。
第二代ADC
第二代ADC药物的研发中,mAb技术得到改进,单克隆抗体被仔细选择,提高了肿瘤细胞靶向性,并减少与健康细胞交叉反应。更重要的是,早期使用当时治疗癌症的小分子药物作为毒性荷载缺乏临床研究,后来发现了更有效的小分子物质。与第一代ADC相比,第二代ADC具有更好的CMC特性。从当时FDA批准的三种二代ADC药物来看(vedotin、emtansine、ozogamicin),
第二代ADC药物显示出良好的临床疗效和安全性。
然而,由于脱靶毒性、存在未结合抗体以及药物抗体比(DAR)为8引起的ADC聚集或快速清除等原因,目前大多数第二代 ADC显示出较窄的治疗窗口。此外,DAR>4的ADC被证明耐受性低、体内疗效低但是血浆清除率高。至此,二代ADC药物也难以满足患者的需求。优化单克隆抗体(mAbs)、连接物和结合化学物质可以提高第三代ADC的疗效,位点特异性偶联现在被认为是ADC成功开发的关键。
第三代ADC
第三代ADC药物综合了一代二代失败的因素,利用小分子药物与单克隆抗体的位点特异性结合,产生DARs为2或4的ADC,这种ADC药物毒性降低,无未结合的单克隆抗体,稳定性和药代动力学大大提高,偶联脱落速度更低,药物活性高,低抗原水平下的细胞活性高。综上所述,第三代ADC药物攻克了导致一代二代药物失败的因素,让患者得到更好的治疗[9]。
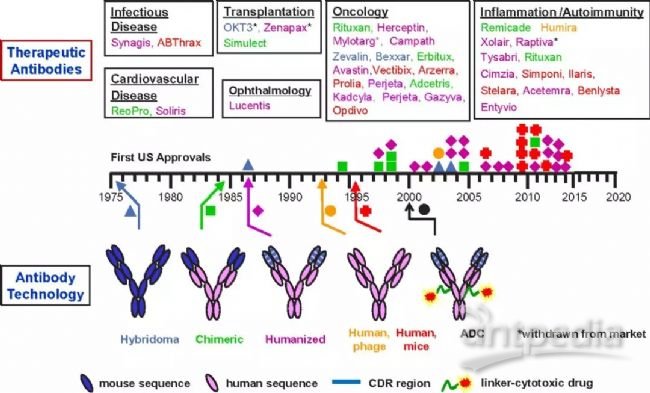
图3、抗体研发及制备技术史[10]
ADC现状
尽管已经有几十年的研发历史, ADC依然有巨大的改良空间。因为靶点清楚、技术成熟、选择性好等优点,抗体药物偶联物研究在未来几年里预计继续成为抗癌领域的研究热点。据悉本月11日,美国FDA宣布加速批准基因泰克的抗体偶联药物Polivy(polatuzumab vedotin-piiq)上市,与苯达莫司汀与rituximab联合使用,治疗难治的弥漫性大B细胞淋巴瘤成人患者。FDA指出,针对这一疾病,这也是首款免疫化疗(chemoimmunotherapy)。希望这款创新药能够尽快研制成功,也期待各大药企在未来研发更多更优质的ADC药物,能够为更多患者带来新的治疗方案。
参考资料
[1].Nirnoy Dan, Saini Setua, Vivek K. Kashyap.Antibody-Drug
Conjugates for Cancer Therapy:Chemistry to Clinical
Implications.Pharmaceuticals. 2018, 11, 32,1-22.
[2].Siler Panowksi,Sunil Bhakta,Helga Raab.Site-specific antibody drug
conjugates for cancer therapy.Landes Bioscience.2014,6:1, 34–45.
[3].Adam C. Parslow, Sagun Parakh, Fook-Thean Lee.Antibody–Drug Conjugates for Cancer Therapy.Biomedicines.2016, 4, 14,2-17.
[4].Nikolaos Diamantis,Udai Banerji.Antibody-drug conjugates—an emerging
class of cancer treatment.British Journal of Cancer.2016,7,362–367.
[5].Scott, A.M.;Wolchok, J.D.; Old, L.J. Antibody therapy of cancer. Nat. Rev. Cancer 2012, 12, 278–287.
[6].Shuptrine, C.W.; Surana, R.; Weiner, L.M. Monoclonal antibodies for
the treatment of cancer. Semin. Cancer Biol. 2012, 22, 3–13.
[7].Kubota, T.; Niwa, R.; Satoh, M.; Akinaga, S.; Shitara, K.; Hanai, N.
Engineered therapeutic antibodies with improved effector functions.
Cancer Sci. 2009, 100, 1566–1572.
[8].Antibody-Drug Conjugates: Possibilities and Challenges.PubMed.2019,1-3,11(1), 3-23.
[9].Meghdad Abdollahpour‐Alitappeh1.; Majid Lotfinia.; Tohid Gharibi.
Antibody–drug conjugates (ADCs) for cancer therapy:Strategies,
challenges, and successes.J Cell Physiol.2018,6,1-15.
[10].Eunhee G. Kim1 and Kristine M. Kim.Strategies and Advancement in
Antibody-Drug ConjugateOptimization for Targeted Cancer Therapeutics.
Biomol Ther.2015, 23(6), 493-509.
-
焦点事件

-
焦点事件

-
科技前沿