实验室分析方法--液相色谱的定性方法介绍
液相色谱法作为一种重要的分离分析手段,具有能通过色谱柱分离复杂样品中不组分的能力,这种能力是任何其他分析方法所无法比拟的。对色谱柱分离后的组分进行。尽管液相色谱法包多定性及定量鉴定,是色谱工作者完成分析工作的一个重要环节。尽管液相色谱法包括多种模式,但无论采用何种模式,对样品进行定性及定量分析皆基于通过检测器得到的图信息。
液相色谱过程中影响溶质迁移的因素较多,同一组分在不同色谱条件下的保留值可能相差很大。即便在相同的操作条件下,同一组分在不同色谱柱上的保留也可能有很大差别。在同根色谱柱上的分离,有时甚至会因为流动相组成的改变而出现出峰次序颠倒的现象。显然,与气相色谱相比,液相色谱法定性的难度更大。对液相色谱中组分定性方法的研究一直是色谱工作者努力探求的一项重要工作。这里只介绍几种最常用的定性方法。
一、利用已知标准样品定性
在具有已知标准物质的情况下,利用标准样品对未知化合物定性是最常用的液相色谱定性方法,这也是唯一在任何条件下都有效的方法。当无标准物时,其他定性方法才被推荐采用。
液相色谱的分离机理比较复杂,除了吸附和分配机理外,还有离子交换、体积排除、亲和作用未知物疏水作用等分离机理。组分的保留行为不仅与固定相有关,还与流动相的种类及组成有关。因此,利用该法定性的依据是:在相同的色谱操作条件下(包括柱长,固定相、流动相等),组分有固定的色谱保留值。即在同一根色谱柱上,用相同的色谱操作条件分析未知物与标准物已知标准物,通过比较它们的色谱图,对未知物进行比较鉴别。当未知峰的保留值与某一已知标准物完全相同时,可以初步判断未知峰与该标准物是同一物质;在色谱柱改变或流动相组成经多次改变后,被测物的保留值与已知标准物的保留值仍能相一致,能够进一步证明被测物与标准物是同一物质。(如图1所示)

图1 醇溶液定性分析色谱图
已知标准物:A-甲醇;B-乙醇;C-正丙醇;
D-正丁醇;E-正戊醇
二、利用检测器的选择性定性
各种不同的液相色谱检测器均有其独特的性能。示差折光检测器是一种通用性的检测器,但是灵敏度一般较低;紫外、荧光及电化学检测器为选择性检测器,灵敏度相对比较高。择性检测器只对某类或某几类化合物有响应可以借此对特定化合物进行定性分析。在相色进条件下,同一样品在不同检测器上有不同的响应信号,亦可结合几种选择性检测器的测试结果对其定性。
样品经色谱柱分离后进入并联或串联的几种(两种或两种以上)检测器,根据其响应情可以初步判别未知化合物的具体类别。以烃类及其衍生物为例,在紫外光谱区(190~400nm)饱和烷烃的响应很小;而以共轭双键结合的分子如芳香烃等则有较强的响应,分子中环的数量越多,响应越强。对于包含几种烃类组分的混合物样品,将色谱柱中的流出物时引入并联的两种检测器,或按顺序依次引入串联的两种检测器,可以得到两张色谱图,对比各组分在不同谱图上的相对峰高可初步判别组分所属化合物的类型。
在实际分析中多采用双检测器定性。同一检测器对不同种类化合物的响应值有所不同,而不同检测器对同一化合物的响应也不相同。当某一被测化合物同时被两种或两种以上检测检测时,两个检测器或几个检测器对被测化合物检测灵敏度比值与被测化合物的结构性质密切相关,可以用来对被测化合物进行定性分析,这就是双检测器体系的原理。
观检测器体系的连接方式可采用串联连接和并联连接两种方式。当两种检测器中的一种是非破坏性检测器(如TCD)时,可采用简单的串联连接,将非破坏性检测器串接在破坏性测器之前。此时要注意两个检测器的出峰时间差。若两种检测器都是破坏性的,则需采用并联方式连接。在色谱柱的出口端连接一个三通,然后分别连接到两个检测器上。连接后的两台检测器同时进行数据采集,对照所得到的两张色谱图可进行定性。
图2为三组分样品经色谱柱分离后分别在并联的紫外和示差折光检测器上得到的色谱,比较图2中(a)和(b),可以对样品中的三个组分的类别作出初步判定。相对而言,峰1在紫外检测器上的响应较高,峰2和峰3的响应则很弱,初步判断组分1可能带有苯环。而组分2和组分3不大可能带有芳环。总之比较各组分在不同检测器上的色谱图相对响应值,有可能粗略地推测某一类化合物是否存在。


图2 双检测器定性
(a)UV;(b)RI
固定相: Nucleosil-CN
流动相:10mmol/L乙酸水溶液+0.18mmol/L
N-二甲基普罗替林
溶质:1一辛胺;2一辛磺酸;3一辛硫酸
紫外检测波长:292m
三、利用DAD三维图谱检测器定性
光电二极管阵列检测器(DAD)可以对色谱峰进行光谱扫描。在进行未知组分与已知标准物质比对时,除了比较未知组分与已知标准物质的保留时间外,还可比较两者的紫外光谱图。如果保留时间一样,两者的紫外光谱图也完全一样,则可基本上认定两者是同一物质;若保留时间虽一样,但两者的紫外光谱图有较大差别,则两者不是同一物质。这种利用三维图谱比较对照的方法大大提高了保留值比较定性方法的准确性。传统的方法是:在色谱图上某组分的色谱峰极大值出现时,即最高浓度谱带进入检测器时,通过停泵等手段,使组分检测池中滞留,然后对检测器中的组分进行全波长(180~800nm)扫描,得到该组分的外可见光谱图取可能的标准样品按同样方法处理,对比两者光谱图即能鉴别该组分是否与,也可以通过对照标准谱图的方法来识别来标准品相同。对某些有特征紫外光谱图的化合物,也可以通过对照标准谱图的方法来识别未知化合物(如图3)。
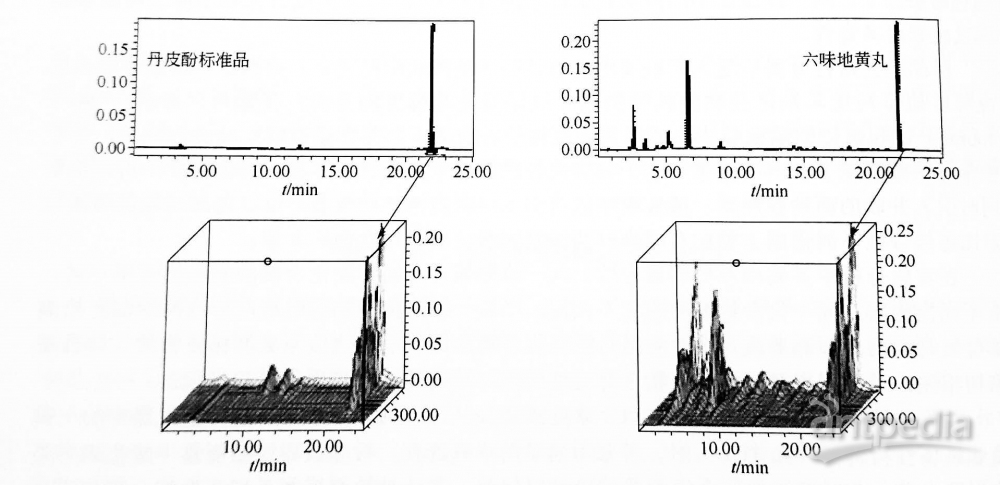
图3 丹皮酚标准品和六味地黄丸的三维色谱图
DAD不仅可以得到样品色谱图,还可以得到样品的时间-检测波长-色谱信号的三维过样品的光谱图,可以很方便地观察到不同出峰时间段内组分的紫外(或紫外-可见)区光谱图,通过样品的光谱图也可以进行样品鉴别,对液相色谱定性具有更大的优势。图4是一组化合物的色谱光谱图,图5是对应的光谱图。通过对比色谱峰上各点的光谱图可以判别峰的纯度,而与标准品的紫外光谱图或标准谱图相比较,也可以进一步确认未知化合物的结构。
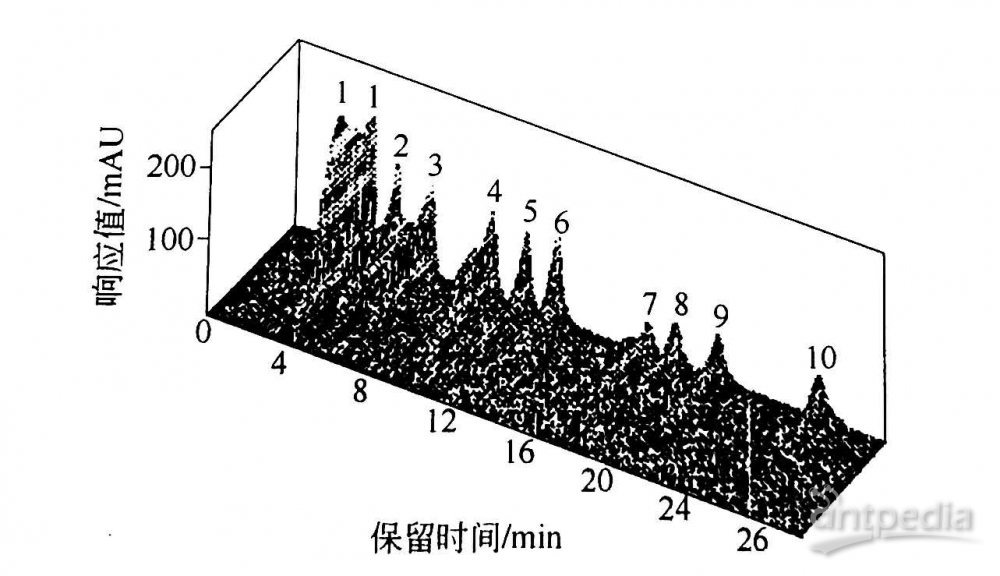
图4 10种头孢类抗生素混合物的三维色谱图
1一头孢;2一头孢米诺;3一头孢他;4一头孢唑肟
5一头孢克洛;6一头孢氨苄;7一头孢曲松;
8一头孢拉定;9—头孢呋辛;10—头孢唑啉
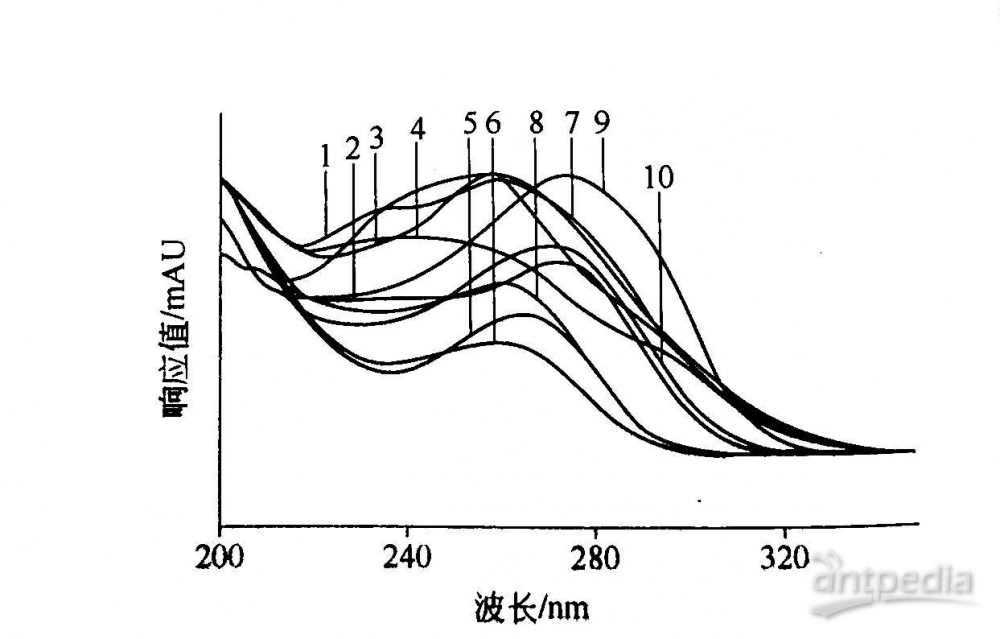
图5 10种头孢类抗生素的光谱图
注:图中标记1~10同图4
实际上,当样品中的不同化合物具有相同的UV生色团时,DAD的定性功能很有限。且当流动相或其他因素改变时也会对DAD的峰定性产生一定的影响。
四、利用保留值规律定性
与气相色谱相比,液相色谱中组分的保留行为也不仅只与固定相有关,还与流动相的种类及组成有关,为了使样品中的多种溶质组分得到更好的分离,可以通过改变流动相组成等手段实现。相应地,亦可以根据某一化合物在特定条件下的保留值变化规律来推测其结构特性。在液相色谱中,溶质保留值变化规律一般受3个或3个以上因素的协同制约,从而给这种提供定性信息方法的实践带来很大困难。
对通过流动相组成与化合物保留值之间关系的理论研究,一些在局部范围内有参考应用价值的经验关系式已经被得到,可以在一定程度上用于样品的定性。
1.反相色谱中的a、c指数定性
理论研究表明,在以键合硅胶为固定相的反相色谱中,溶质保留值与流动相组成关系式中的系数能够反映溶质的结构特征,因此可用于对溶质的辅助定性。液相色谱中存在如下规律:
![]()
(1)
其中,a、c为常数,φB为强溶剂的体积分数。
对非极性、同系物或极性相似、氢键作用能相似的组分,a、c之间有很好的线性关系:
![]()
(2)
其中:

式中,I1、I2、I3、I4是与色谱柱以及流动相种类有关的常数;m1、m2、m3、m4是与流动相有关的常数;X为相互作用能;μA为组分的偶极矩。
采用一个化合物校正后,即可从作用指数c计算出a,并由式![]() 计算出容量因子。所以建立一个指数c的数据库就可以对非极性或同系物进行保留值预测及定性。
计算出容量因子。所以建立一个指数c的数据库就可以对非极性或同系物进行保留值预测及定性。
对于同种类型的键合均匀的C18固定相,当组分与固定相作用不发生氢键变化以及构象变化时,各C18柱热力学上的差别主要反映在固定相C18的键合量、比表面积以及柱相比上。同一种化合物在两支不同色谱柱上的参数a有简单的线性关系:
![]()
(3)
不同极性取代基化合物的定性需同时建立a、c双参数数据库,在作用指数的基础上,将保留指数换算为参数a,再利用式(3)定性。
采用作用指数定性时,可先选几个标准物来标定柱系统,获得式(3)的线性关系。卢佩章等给出了460种化合物在C18柱上不同条件下的参数a、c,并提出了不同柱系统,大同冲洗剂浓度组成时参数a、c之间的换算方法。在相同的色谱条件下,如果样品中某一组分的a、c值与一已知标样相同,即可认定两者为同一种化合物。
2.有机酸碱的pH-pKa规律定性
在反相液相色谱系统中,改变流动相pH值,不同种类的可解离有机酸、碱等样品的保留值变化有其独特的规律,如图6所示。
对一类有机酸组分而言,在特定的条件下其解离常数pKa本不变,流动相中pH值变化后,对有机酸的解离起到调节作用,因此溶质的容量因子也将随之变化。对于有机碱类的溶质,容量因子随流动相pH值的变化与有机酸正相反。因此,对一个未知化合物而言,测定其容量因子随流动相pH值的变化规律,即能判断其为有机酸类或有机碱类化合物,以及其酸、碱性的强弱。
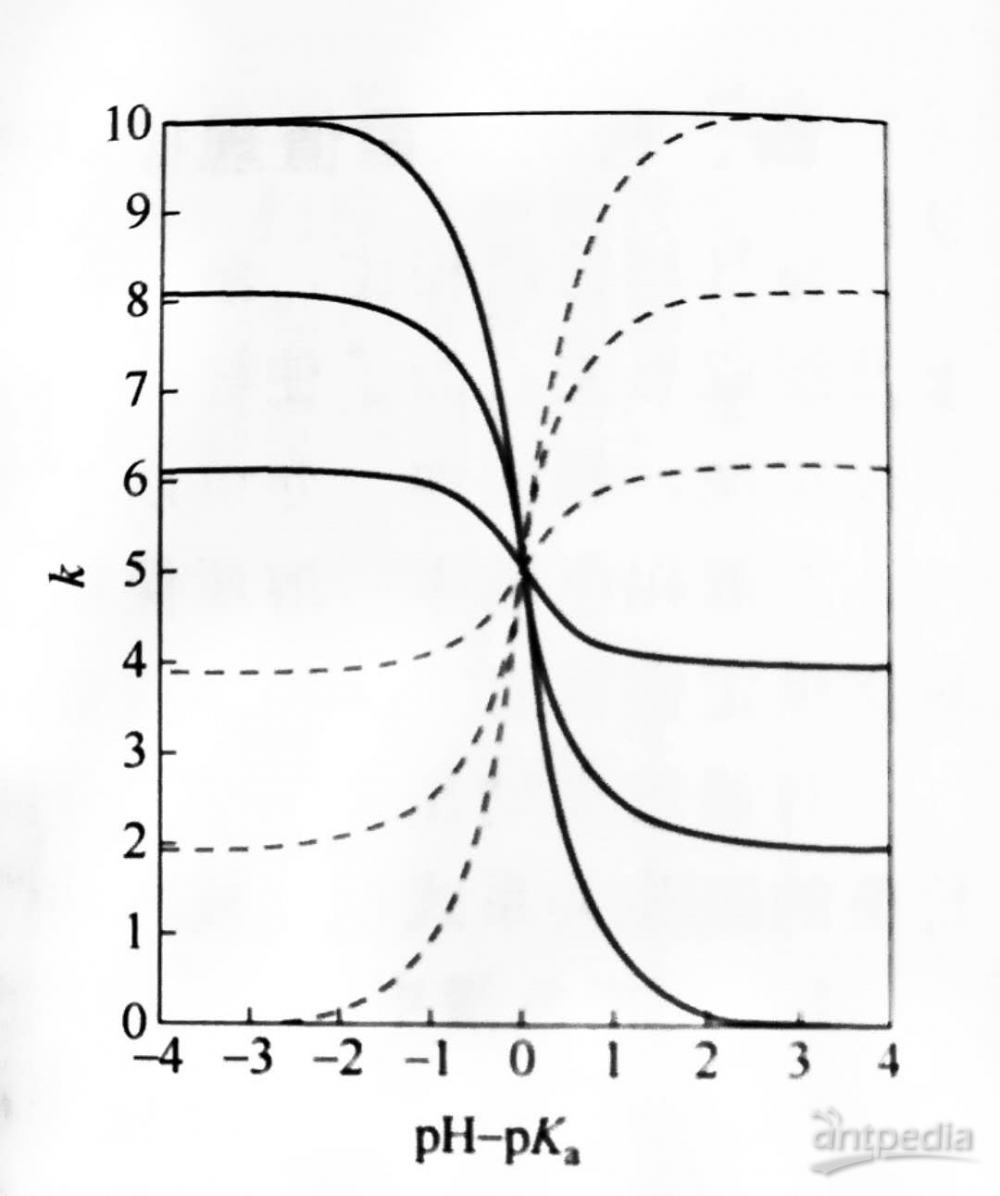
图6 一元有机酸(实线)、碱(虚线)的容量因子与流动相pH-pKa关系
3.碳数规律定性
利用碳数规律定性,可以在已知同系物中几个组分保留值情况下,推出同系物中其他组分的保留值,然后与未知物的色谱图进行对比分析。
容量因子(k')是溶质的一种结构型物性参量,其对数值与同系物碳数之间存在良好的线性关系:
![]()
(4)
其中,a、b为常数,n为同系物碳数。
对于包含有同系物组分的样品,已知部分同系物在色谱图中位置的情况下,可以根据碳数规律推出同系物中其他组分的保留值,并对同系物的未知部分进行定性。
利用碳数规律定性时,应先判断未知物类型,才能寻找适当的同系物。与此同时,要注意当碳原子数较小或较大时,可能与线性关系发生偏差。
这一规律适用于任何同系物,如有机化合物中含有的硅、硫、氮、氧等元素的原子数及某些重复结构单元(如苯环、C=C、亚氨基等)的数目均与溶质容量因子的对数呈线性关系,同样适用于上述规律。
五、联用技术结合定性
色谱法具有很高的分离效能,但它不便于对已分离的组分直接定性。而红外光谱、质谱、核磁共振等是剖析有机物结构的强有力工具,特别适用于对单一组分定性,但是它们对混合物无能为力。将色谱仪与定性分析的仪器联用,则可以取长补短,解决组成复杂的混合物的定性问题。随着计算机技术的发展及应用,色谱联用技术得到了很好的发展。
近年来,液相色谱与其他分析方法的联用技术得到较大的发展,曾经需要离线完成的定性工作可以很便利地在线解决。高效液相色谱质谱联用技术为样品特别是生物大分子的定性分析提供了一种强有力的手段,它能准确测得未知物分子量,是目前解决复杂未知物定性分析的最有效工具之一;高效液相色谱-核磁共振联用技术是有机化合物结构分析的强有力的工具,特别是对同分异构体的分析十分有用高效液相色谱红外光谱联用技术在有机化合物的结构分析中有着很重要的作用,可用于对官能团定性;色谱原子光谱(原子吸收光谱和原子发射光谱)联用技术主要用于金属或非金属元素的定性、定量。关于联用技术的应用,最近已有相关专著问世,可供参考。
1.与红外光谱仪联用
红外光谱是一种强有力的结构鉴定手段,几乎没有两种物质有完全相同的红外光谱。20世纪80年代后,傅里叶变换红外技术得到迅速发展。傅里叶变换红外光谱仪(FTIR)具有测量快速(0.2s)、灵敏度高(纳克级)的特点能够在得到色谱图的同时监测每个色谱峰的完整光谱。
与HPLC联用的傅里叶联用光谱仪有两种类型,一类不必除去流动相,仪器的数据处理系统能够通过差减的方式扣除溶剂的红外吸收光谱,得到被测物的红外光谱。由于流动相组成通常不是单一的,且各组分含量不定,所以光谱差减较困难。一般只适用于正相色谱,对于反相色谱,需要采用细内径柱和氘代溶剂。另一类需除去溶剂后进行检测,已有的接口包括漫反射转盘接口、缓冲存储接口和粒子束接口等。各种接口有其适用范围和限制。总之,傅里叶变换红外光谱仪在提高灵敏度、记录光谱等方面的改进,可使它用于普通HPLC分析物的检测,但联用技术特别是接口技术尚有较大的改进空间。
2.与核磁共振的联用
与其他HPLC检测器相比,核磁共振(NMR)是一种信息丰富的检测手段,其化学位移和偶合常数能提供丰富的有关分子中每个氢原子的局部电子环境的结构信息。在有机结构分析四大谱(红外光谱、紫外光谱、核磁共振、质谱)中,NMR是最好的一种推断化合物结构的手段。HPLC与NMR联用的有利条件是:HPLC与NM都是在溶液状态下操作,无需挥发和加热步骤。核磁共振对样品是非破坏性的,为实现HPLC-NMR-MS三联用和HPLC-NMR-FTIR-MS四联用提供了可能性。
LC-NMR联用技术在20世纪80年代初期已经开始研究,但是由于NMR灵敏度低(10-4~10-5g),液相色谱使用的氘代溶剂十分昂贵和溶剂信号对样品的千扰等技术上的原因,联用技术发展缓慢。近年来,NMR技术迅猛发展,磁场强度不断提高,氘锁通道性能改善,可以不用或少用氘代试剂,在抑制溶剂峰方面也有很大进展,设计方面已有专为LC-NMR联用的流动液槽探头。LC-NMR联用主要有三种模式:连续流动模式、停止流动模式和峰存储模式,也有多种接口可供选择。
3.与原子吸收光谱仪的联用
HPLC能分离各种各样的有机或无机金属化合物的样品,原子吸收光谱(AAS)仪对大多数元素能做选择性的、高灵敏度的检测。HPLC和AAS的联机使用,在环境和生物化学研究中已得到应用。
HPLC柱流出物是溶液,而AAS测定所用样品也为液体,因此HPLC与AAS的联机较为方便,一般认为只需将HPLC流出液引入原子化器即可。但困难是HPLC柱流出液的流速(0.5~2ml/min)和样品溶液引入AAS仪的流速(2~10ml/min)不匹配,一般而言,一滴液滴(100μl)可满足AAS的分析要求,因此采用人工调节使两者匹配很困难。一种分析小量样品的原子吸收注入方法已经被发展。用液滴形成器收集HPLC流出物,产生的小液滴落入漏斗中,然后被吸入火焰,实现AAS分析。
4.与原子发射光谱仪的联用
许多元素受到适当的激发时会发射特征波长的辐射,可采用原子发射光谱(AES)仪进行测定。同AAS比较,AES能够同时进行多元素测量,适合于在线监测HPLC柱流出物。
AES分析温度大大高于AAS分析同种元素时所需要的温度,这是因为在AES中要使原子激发,而在AAS中仅是原子的气化。AES常用的激发原子的方法包括火焰法和电感耦合等离子体法,二者都已用于HPLC-AAS联用仪器系统。相比之下,电感耦合等离子体AES(ICPAES)比火焰AES(FAES)的灵敏度更高。
ICPAES用作HPLC检测器对多数金属离子的检测限达到10-9~10-10g/ml虽然与HPLC-FAES相比,HPLC-ICPAES法具有更高的灵敏度和选择性,但其成本却高得多。AES用于许多物质的测定,如螯合物中的铜,有机金属配合物中的金属,磷酸盐中的磷,生物样品中的砷、蛋白质、核糖核酸、硒等。
HPLC-ICP借口连接的主要问题是典型的LC流动相流速不适于等离子体源。这种专属的原子发射光谱检测器一般使用在线雾化激发小体积(5~200μl)液体,液体转化成气溶胶后引入原子激发池,使用一种全注入微浓喷雾器,有助于提高较低的雾化和迁移效率减小等离子体焰炬、水冷喷雾室、采用低压和低流炬、氧掺杂等方法也可以提高转化效率。
5.与电子自旋共振光谱仪的联用
除了红外光谱区,电磁辐射的微波光谱区也已经被开发使用,成为(一种有用的检测器。电子自旋共振光谱(ESR)可以满足HPLC对检测器的许多要求,如检测限、选择性、溶可溶性等,但目前应用不多。
ESR的研究对象是至少具有一个未成对电子的原子或分子。分子中的未成对电子在直流磁场作用下产生能级分裂,当施加在垂直于磁场方向上的电磁波满足一定条件时,处于低能级的电子吸收电磁波能量跃迁到高能级,产生电子顺磁共振现象。吸收信号的一次微分谱图反映样品的结构信息,对吸收曲线进行积分,可测得顺磁物质的自旋浓度,从而实现对样品进行定性、定量分析。
为了获取ESR光谱,样品被放在强磁场区,用微波激发。在0.34T(3400G)磁场区,共振所需频率为9.5×109Hz,最小可测量10~13mol未成对电子,这使ESR可能成为一个最灵敏的检测器。HPLC与ESR的连接无需特殊的接口。
用60Co放射源的强γ射线激发生物分子如氨基酸、核酸,能获得样品的ESR谱,但由于混合物样品的谱图重叠,需要在样品结构测定前进行HPLC分离。其缺点是许多自由基的生命周期太短而不能实现分离,为此可以使用各种自旋捕捉试剂来提高自由基的生命周期。在HPLC-ESR的联用分析中,除了可以获得样品浓度信息外,还可以通过停流获得样品的ESR谱,得到未成对电子的化学环境信息。ESR作为HPLC的检测器,具有很高的选择性,特别是对不同氧化态的金属的分析;缺点是ESR的灵敏度不够高,且价格昂贵。
利用金属元素与自旋标记试剂反应形成配合物,通过测定配体的ESR信号,而不是金属元素的顺磁性,也可以进行多元素的分析。
6.与表面增强拉曼光谱仪的联用
当一束单色光照射到样品上后,样品分子使入射光发生散射。在散射光谱中出现频率为几个波数到几千个波数的散射光为拉曼散射。不同的分子或结构有特征的拉曼位移,拉曼光谱线的强度与入射光的强度和样品分子的浓度成正比,据此可以对样品分子定性、定量分析。目前的拉曼光谱一般都采用激光激发,虽然激光使拉曼效应增强了,但拉曼散射仍比较弱,而表面增强拉曼散射(SERS)可以使拉曼散射截面增加5~6个数量级,具有较高的灵敏度,有利于满足痕量分析检测的需要。SERS已经成为检测药物、生物医学和环境等领域痕量有机化合物的高灵敏度、高选择性和灵活性的一项技术。
许多分子都能产生拉曼散射,但SERS效应只有在少数金属(Ag、Au、Cu、Li、Na、K等)表面上才能出现,其中银的表面增强效果最佳。为了使金属表面达到能产生SERS效应的粗糙度,可以采用多种处理办法,其中采用银金的胶体溶液有较好的效果。但胶体溶液具有凝絮趋向,会导致结果重现性差;而流动系统,如流动注射技术和高效液相色谱,有助于减少凝絮趋向。近年来,采用银的胶体溶液的SERS在HPLC中的应用逐渐发展。研究结果表明,较高的温度会加大胶体凝集,增强拉曼信号,这不但可以得到通常的二维色谱图(时间-SERS强度),而且能获得三维图谱(时间拉曼位移-SERS强度),为定性分析提供更多的依据。
检测器使用普通的流通池时,每次都需要用稀硝酸清洗整个系统,以去除银的胶体溶液和其他物质在管壁的沉积。这些沉积物具有较强的记忆效应,会产生色谱峰的拖尾、基线漂移、谱图干扰等。为此,有人提出了一种无窗流通池的设计,柱后流出液与Ag的胶体溶液混合后进行检测,效果较好。
六、化学方法定性
化学方法定性就是利用化学反应,使样品中某些化合物与特定试剂发生反应,生成相应的衍生物,常用的方法有柱前预处理、柱上选择除去和柱后衍生三种。
1.柱前预处理法
这是使用物理或化学消除剂将样品中某类化合物消除、减少或转化,从而得知样品中是否含有这类官能团化合物的方法。操作时将给定的消除剂涂在载体上或直接放在消除柱中,或放在进样的注射器中,当样品与消除剂接触后,消除剂迅速使这类化合物发生不可逆吸附减化学反应,而使其色谱峰消失、变小或发生位移,通过比较色谱图,可以判定样品中有无这类官能团化合物的存在。
使用这种方法时可直接在色谱系统中装上预处理柱,如果反应过程进行较慢或进行复杂的试探性分析,也可使试样与试剂在注射器内或者其他小容器内反应,再将反应后的试样注入色谱柱。
2.柱上选择除去法
与柱前预处理法的原理相同,将某些有特征性吸附的吸附剂装入一个短柱内,或将某些化学试剂涂到一些载体上,再装入一个短柱内,将该短柱(称为预柱)串联在分析柱前,使样品中某些组分在通过预柱时被吸附或与这些特征化学试剂发生化学反应而被吸附,从而使这些组分不能进入分析柱被分析,在色谱图上与这些组分相对应的色谱峰将消失。
3.柱后流出物化学反应定性法
将色谱分离后的组分直接通入到某些特征试剂中,或将柱后流出物收集后再加入特征试剂,观察这些组分与特征试剂发生化学反应后的某些变化,如颜色变化、沉淀出现,有气体放出或其他明显变化,即可对未知组分的类型作出初步鉴定。
用柱后流出物化学反应定性时,使用的检测器应为非破坏性检测器,即样品在检测器内不能发生化学反应。