重大突破I Cell:外囊泡蛋白质组学研究发现肿瘤诊断及分类的可靠标志物

肿瘤是世界公认的难题,仍缺乏有效诊断治疗手段。目前,临床上对肿瘤的诊断通常采用组织活检,液体活检作为一种全新的手段,避免了手术对患者伤害,具有较大优越性,应用潜力巨大。由于外囊泡携带的信息多种多样,因此外囊泡内含物质作为肿瘤的生物标志物,尤其作为液体活检领域的技术手段,具有巨大潜力。
2020年8月13日,来自美国康奈尔医学中心等多个研究团队,在《Cell》(IF=38.6)发表了题为“Extracellular Vesicle and Particle Biomarkers Define Multiple Human Cancers”的文章。研究对来自426个人的组织、血浆、体液来源的外囊泡及颗粒(Extracellular Vesicle and Particle,EVP)进行蛋白质组学分析,发现了新EVP标记物;同时,利用机器学习算法,找到了组织来源的外囊泡肿瘤分类标志物(具有90%敏感性及94%特异性);以及血液来源的外囊泡肿瘤诊断标志物(具有95%敏感性及90%特异性)。该研究证明外囊泡及颗(EVP)蛋白能够作为肿瘤检测和分类的可靠标志物。

研究材料
健康人及肿瘤患者的组织、血浆、及其他液体样本来源的外囊泡及颗粒
技术方法
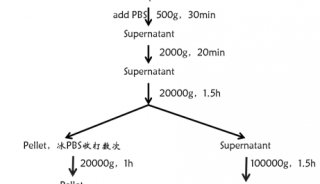
超速离心法分离EVP、Label free蛋白组、PRM靶向蛋白组
实验路线图

研究结果
1. 蛋白组学分析:对不同来源样本分泌的外囊泡进行蛋白质组学分析
2020年8月13日,来自美国康奈尔医学中心等多个研究团队,在《Cell》(IF=38.6)发表了题为“Extracellular Vesicle and Particle Biomarkers Define Multiple Human Cancers”的文章。研究对来自426个人的组织、血浆、体液来源的外囊泡及颗粒(Extracellular Vesicle and Particle,EVP)进行蛋白质组学分析,发现了新EVP标记物;同时,利用机器学习算法,找到了组织来源的外囊泡肿瘤分类标志物(具有90%敏感性及94%特异性);以及血液来源的外囊泡肿瘤诊断标志物(具有95%敏感性及90%特异性)。该研究证明外囊泡及颗粒(EVP)蛋白能够作为肿瘤检测和分类的可靠标志物。

图1 对不同来源样本分泌的外囊泡进行蛋白质组学分析
2. 鉴定患者中组织特异性的肿瘤相关EVP蛋白标志物
为了找到可用于诊断肿瘤患者的外囊泡蛋白标志物,研究人员分析了癌及配对癌旁(包括胰腺癌、肺癌)组织来源的外囊泡蛋白质组成分,研究结果分别在胰腺癌、肺癌中鉴定了356种及123种EVP蛋白,进一步功能分析比较发现,胰腺癌组织来源外囊泡蛋白(PaCa EVP)成分参与上皮间质转化(EMT)等, 肺癌组织来源外囊泡蛋白(LuCa EVP)成分参与RNA加工等途径。综上,不同来源外囊泡中的蛋白选择性包装不同蛋白,并具有区分不同癌种的潜能。
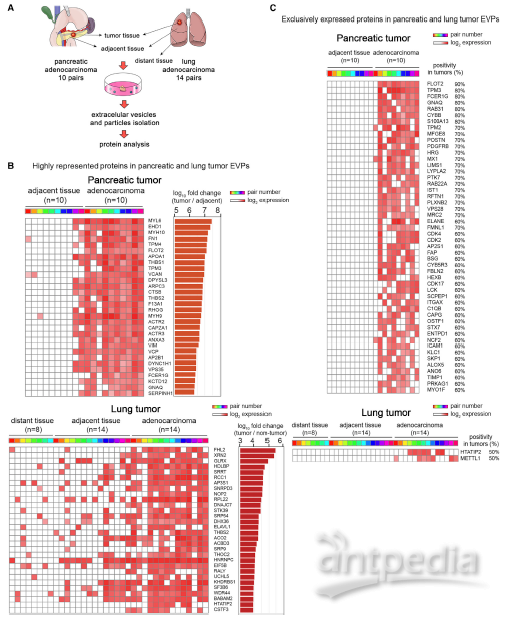
图2鉴定患者中肿瘤衍生的组织特异性EVP蛋白
3. 从多种癌症组织衍生EVP中确定与肿瘤相关EVP特征蛋白标志物
为了明确肿瘤组织及非肿瘤组织来源的EVP蛋白是否能够区分癌症,分析了131个组织来源、20个骨髓来源的EVP样品。通过机器学习算法进行分类比较,鉴定出了区分肿瘤与正常组织的EVP蛋白可用于进行癌症诊断, 例如VCAN,TNC和THBS2, 对于特异性癌症检测具有90%敏感性及94%特异性。
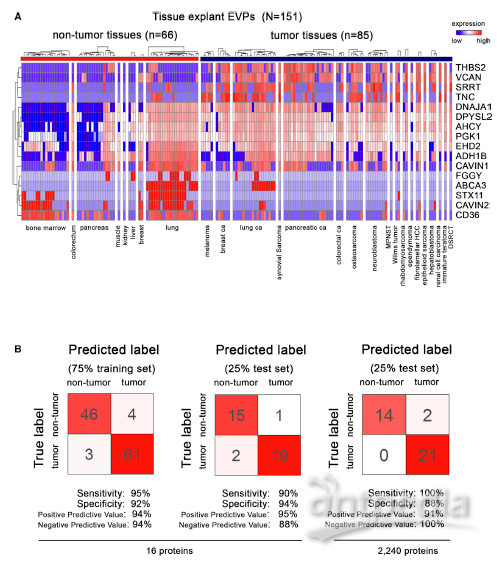
图3鉴定多种肿瘤来源的组织中EVP特征标志物
4. 从多种癌症血浆衍生EVP中确定与肿瘤相关EVP特征蛋白标志物
进一步,采用与组织来源EVP相同的机器学习分析方法,寻找血浆来源EVP中的特征性可用于诊断的蛋白标志物,分析了120例血浆来源EVP样品,包含77例癌症病人(16个不同癌种)及43例健康人。鉴定出了不同免疫球蛋白相关蛋白的组合,对于癌症的检测具有最佳预测效果,达到了95%敏感性和90%特异性。综上表明,血浆来源的EVP 蛋白质可用作液体活检以进行癌症诊断。
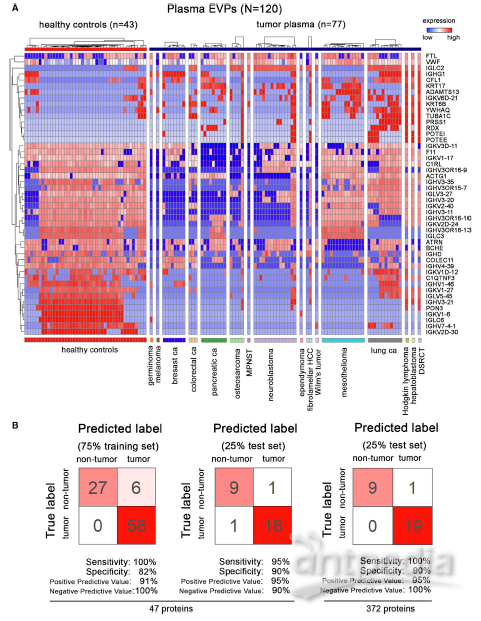
图4 鉴定多种肿瘤来源的血浆中EVP特征标志物
5、肿瘤组织及血浆来源的EVP蛋白质对癌症类型进行分类
最后,研究团队在组织和血浆来源EVP中定义了一组肿瘤类型特异性EVP蛋白。首先分析了组织来源的EVP, 通过对四种不同癌症类型(黑色素瘤,结肠直肠癌,胰腺癌和肺癌)患者的原发性肿瘤或淋巴结中获得的组织来源EVP蛋白,基于机器学习算法,找到了29种EVP蛋白,其中一些与免疫功能有关,发现它们在区分不同癌症中具有最高的预测能力,可以对原发性未知的肿瘤进行分类。
由于组织活检并非总能用于确定肿瘤类型,因此研究团队接下来使用血浆来源的EVP蛋白质组进行了类似分析,通过对五种不同癌症(乳腺癌、结肠直肠癌、肺癌、胰腺癌、间皮瘤)分析,发现血浆来源的EVP蛋白尽管大部分是造血起源,但仍然在同类型肿瘤之间存在强相关性。在可区分癌种的30种EVP蛋白中,免疫球蛋白高频出现。进一步对五种癌症类型EVP分析发现,无论癌症分期如何,样本均能基于原发肿瘤类型进行聚类。综上表明,血浆来源的EVPs蛋白质组代表真正的肿瘤特异性信号,且能够区分癌症类型。
根据以上分析,研究团队找到了能作为可靠生物标记物,可用于癌症检测和确定癌种的EVP蛋白。
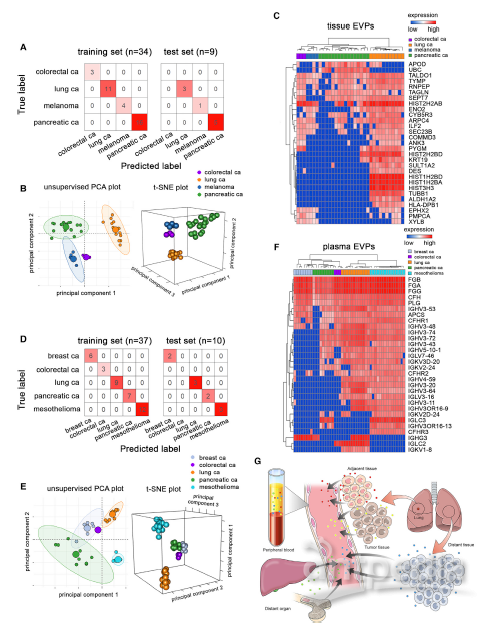
图5 肿瘤来源EVP可对原发性肿瘤进行分类
小结
该研究从健康、肿瘤患者不同组织、血液、体液来源的外囊泡出发,利用蛋白质组学技术结合机器学习等方法,找到了适用于不同样本类型的EVP肿瘤特异性标记物,或可用于癌症检测及确定癌症种类,为采用外囊泡分析进行肿瘤的诊断等带来了新视角。中科新生命现可提供外囊泡提取至蛋白组学分析一站式服务,同时能够提供基于机器学习算法的标志物筛选分析,欢迎感兴趣的老师咨询。

-
仪器推荐

-
仪器推荐

-
仪器推荐

-
仪器推荐
-
仪器推荐
 询底价 Tel:400-6699-117 转 3981
询底价 Tel:400-6699-117 转 3981 -
厂商文章

-
厂商文章

-
厂商文章
-
厂商文章
-
厂商文章
-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章

-
厂商文章
-
厂商文章

-
厂商文章