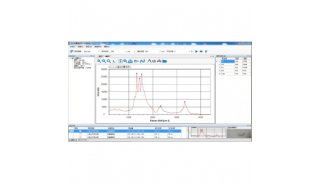
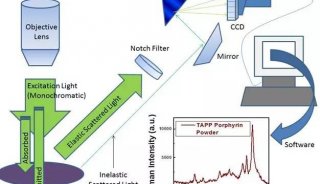
水和冰的拉曼谱图一样吗?
水和冰是我们生活中常见的物质之一,通常人们从感性上会认为这两种物质是一样的,只是从物理角度形态上来区分就是液态和固态的区别,从化学成分上来分析并没有区别,化学式都是H2O。对此,上述两种看似相同又不同物质到底隐藏了哪些更深的“秘密”,他们的拉曼谱图又有哪些特别之处呢。
水被称为人类生命的源泉,包括天然水(河流、湖泊、大气水、海水、地下水等)[含杂质],蒸馏水[理论上的纯净水],人工制水(通过化学反应使氢氧原子结合得到的水)。水是由氢、氧两种元素组成的无机物,无毒,在常温常压下为无色无味的透明液体。

水的密度变化主要由分子排列决定。也可以说由氢键导致。由于水分子有很强的极性,能通过氢键结合成缔合分子。液态水,除含有简单的水分子(H2O)外,同时还含有缔合分子(H2O)2和(H2O)3等,当温度在0℃水未结冰时,大多数水分子是以(H2O)3的缔合分子存在,当水温降到0℃时,水结成冰,水结冰时几乎全部分子缔合在一起成为一个巨大的缔合分子,在冰中水分子的排布是每一个氧原子有四个氢原子为近邻两个氢键这种排布导致成是种敞开结构,冰的结构中有较大的空隙,所以冰的密度反比同温度的水小。
科学家们通过X-ray 衍射分析,得出了水是微观晶体的结论,具有短程有序性,在短时间内可能会产生与冰相似的结构,如图1所示。
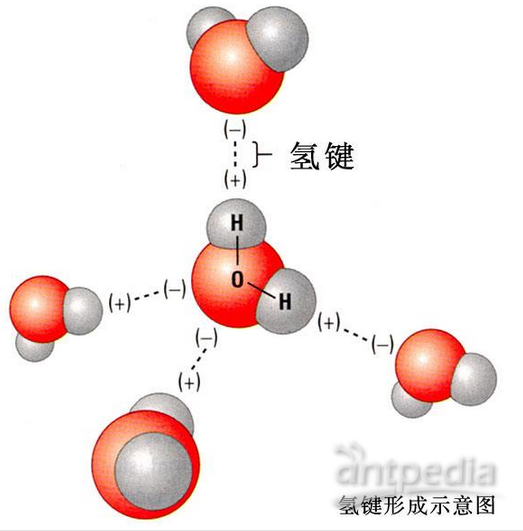
图1.水的四面体结构图
冰的结构与性质

冰是由水分子有序排列形成的结晶,而自然界中的水大部分会以固体冰的形式存在。其中,最普遍的存在形式是水分子间靠氢键连接在一起形成非常“疏松”(低密度)的刚性六角冰结构(图1)。每个水分子都能缔合另外4个水分子,形成四面体结构,所以水分子的配位数为4,即每个氧原子周围存在四个邻近的氢原子,而氧原子规则排列在六角晶格上。
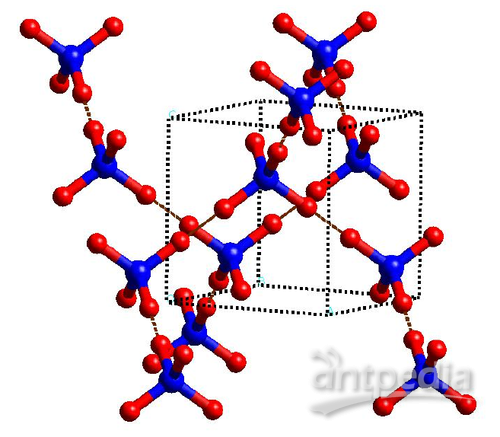
图2.冰的六角冰结构
冰是无色透明的固体,分子之间主要靠氢键作用,晶格结构一般为六方体,但因应不同压力可以有其他晶格结构。密度比水小。
以上描述的水和冰的性质当中都提到了关键词“氢键”,什么是氢键?
氢键是一种弱相互作用力,当氢离子与电负性较大的原子(如N,O,F)以共价键形式结合之后,会吸引周围原子的外层电子,这就会使H变成类似H+的结构去吸引其它原子身上的孤对电子,因此,氢原子会在两个原子之间形成这种类似于共价键的结构,叫做氢键。
其中,最为普遍的存在形式是水中的氢键。在离散的水分子中,存在两个H原子和一个O原子,两个水分子之间就可以形成一个氢键。当仅存在两个分子时,最简单的情况称为水的二聚体,当存在多个水分子,例如在整个水体系中,一个水分子有可能会形成多个氢键,因为一个氧中有两个孤对电子,每个孤对电子可以和另一个水分子上的H形成氢键,这样一来一个水分子最多可以形成四个氢键,如图所示。氢键对水的晶体--冰的结构影响是非常大的,他可以使冰形成一个六边形,因此在相同温度下,冰的密度要小于水的密度,与其它物质略有不同。
水和冰的拉曼谱图对比:
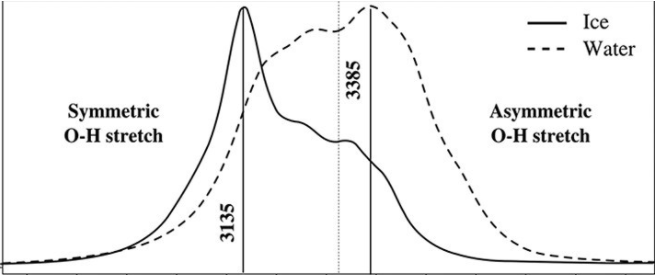
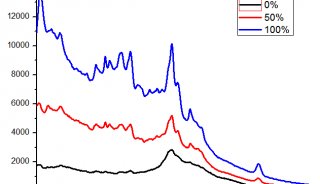
图3.冰和水中的H—O键振动的特征拉曼信号。
在液态水的情况下,分子不断运动,引起相当弱的氢键的连续产生和断裂。水可以被认为是通过氢键形成簇的分离的水分子和水分子的混合物。因此,所有贡献,就存在的氢键数量而言,都有助于H—O振动带。这导致具有几乎等同表示的带的对称和不对称区域的广谱。发现每个分子的氢键的平均数为2.75,其表现为对应于具有三个H键的贡献在84625px-1处的稍大的强度。
在冰的情况下,另一方面,温度的降低将加强氢键,导致了较弱的H—O键,因此会在较低频率下振动。此外,除了向较低频率的转变之外,由于在较低温度下分子间氢键的重要性增加,与完全H键合原子相关的光谱的下部增强并变得更窄。