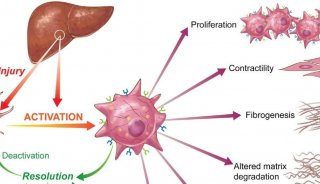
Nature综述珍藏版!肿瘤中的免疫细胞代谢

景杰编者按:肿瘤免疫代谢是当今研究的热点问题,近日Nat Rev Cancer上发表了重磅综述,详细阐述了癌细胞代谢和免疫代谢之间的相互作用。
值得关注的是,癌细胞的代谢产物乳酸,在糖酵解、肿瘤微环境中发挥重要作用,业已成为肿瘤研究的热点方向。【景杰生物】独家提供“乳酸化抗体、乳酸化修饰组学分析“等多种蛋白质修饰检测服务,助力科研工作者探索更多生命奥秘!

本文共计约13000字,预计阅读时长20分钟。全文内容深度解读,建议收藏!


抗肿瘤反应的代谢
TME中的葡萄糖受限会明显影响T细胞反应。例如,低葡萄糖条件(0.1μmM)抑制了T细胞中糖酵解中间体磷酸烯醇式丙酮酸(PEP)的生成,从而破坏了体外钙依赖性NFAT信号传导。与对照相比,降低生长培养基中的葡萄糖浓度可以抑制细胞外酸化率,增加耗氧率,减弱mTOR信号传导并抑制两者的效应功能。降低的mTOR复合物1(mTORC1)信号干扰Teff细胞分化,并且在CD4 + T细胞的情况下有利于免疫抑制性Treg细胞的发展。有趣的是,在CD8 + T细胞中,雷帕霉素对mTOR的阻滞促进了Tmem细胞的分化,这可能在维持抗肿瘤反应中发挥重要作用。与对照培养基相比,葡萄糖的下降抑制了Teff细胞中关键效应分子干扰素-γ(INFγ),IL-17和颗粒酶B的产生。原发性卵巢癌细胞条件下培养基中的葡萄糖限制导致microRNA介导的组蛋白甲基化酶EZH2的抑制,导致NOTCH信号减少,细胞因子产生受到抑制以及Teff细胞活力降低。
像癌细胞一样,高度增殖的免疫细胞(例如活化的T细胞)也依赖于氨基酸代谢来支持蛋白质和核苷酸的合成。因此,氨基酸转运蛋白,包括SLC7A5(也称为LAT1),SLC38A1(也称为SNAT1),SLC38A2(也称为SNAT2)和SLC1A5(也称为ASCT2)在T细胞激活后被高度上调。必需氨基酸必须是外源获得。例如,亮氨酸是效应CD8 +和CD4 + conv T细胞中mTORC1信号传导,效应功能和分化所必需。活化的T细胞还可以快速代谢精氨酸,外源性精氨酸的补充可以改善T细胞的适应性并增加中央Tmem细胞的生成。丝氨酸,色氨酸和半胱氨酸也是T细胞反应的重要营养成分,因此是抗肿瘤免疫反应的重要介质。色氨酸是必需氨基酸,在TME中是决定T细胞反应强度和有效性的重要因素。与正常培养基相比,在不含色氨酸的培养基中,人类T细胞的增殖和活化受到了强烈抑制。癌细胞,肿瘤相关巨噬细胞(TAM),MDSC,抑制性DC和癌症相关成纤维细胞可通过吲哚胺2,3-二加氧酶(IDO)的酶促活性耗尽色氨酸水平,这些酶可在TME内高水平表达。代谢途径对肿瘤生长的十分重要,IDO表达与多种癌症类型(包括胃癌,结肠直肠癌,非小细胞肺癌和黑色素瘤)患者的不良预后相关。
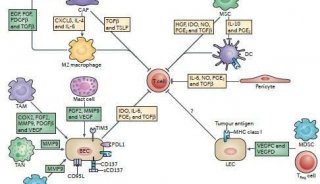
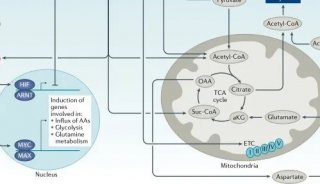
在增殖细胞中,谷氨酰胺为氨基酸和核酸的合成提供氮,为TCA循环中间体提供补充的碳,这个过程被称为“ anaplerosis”(图1)。癌细胞和一些活化的免疫细胞,例如T细胞和巨噬细胞,通常富含高度谷氨酰胺。在体外刺激鼠CD4 + conv T细胞的过程中,谷氨酰胺转运蛋白SLC1A5和SLC38A1和/或SLC38A2的表达显着上调。在MYC的驱动下,谷氨酰胺被谷氨酰胺酶(GLS)代谢为谷氨酸,在由谷氨酸脱氢酶(GLUD1)转化为α-酮戊二酸(αKG;也称为2-氧戊二酸)后,谷氨酰胺可能进入TCA循环。随后在TCA周期中,αKG被代谢为琥珀酸盐和富马酸盐。有趣的是,在谷氨酰胺受限的情况下,一些癌细胞系转换为葡萄糖引起的 anaplerosis,其中丙酮酸被丙酮酸羧化酶转化为草酰乙酸,进入TCA循环。最近表明,在体外谷氨酰胺阻断的条件下,效应CD8 + T细胞也能够上调丙酮酸羧化酶的活性。
与Teff细胞不同,CD8 + Tmem细胞优先依赖OXPHOS。与CD8 + Teff细胞相比,增强的备用呼吸能力也是Tmem细胞的高度特征。最初研究显示使用埃托莫西酯作为肉碱棕榈酰转移酶1A(CPT1A)的抑制剂,该酶是线粒体转运蛋白,负责长链脂肪酸的进入以进行脂肪酸β-氧化(FAO),表明FAO是Tmem中OXPHOS的主要燃料。然而,最近使用T细胞特异性Cpt1a敲除模型进行的研究对此提出了质疑,并证明了高剂量依托莫昔(200μm)的脱靶效应可能是原因。
尽管肿瘤具有高度异质性,但高水平的代谢活性和相关的氧气消耗以及功能紊乱,功能差的脉管系统仍会产生缺氧区域,中位氧饱和度水平低于2%(正常组织中值约为5%) 。缺氧对Teff细胞的影响并不直接。在常氧条件下,HIF-1转录活性会响应T细胞活化而被上调,因此要了解缺氧对进一步增强HIF-1活性的影响,同时还要评估HIF-1的依赖效应,具有一定的挑战性。早期对CD8 + Teff细胞活化,分化和功能的体外研究表明,尽管在缺氧条件下抑制了增殖和某些细胞因子的表达,但其溶解能力,活化标记物和存活率却得到了改善。随后的体内研究表明,与暴露于环境O2张力(20%)的小鼠相比,暴露于低于大气O2张力(8%)的小鼠中CD4 +和CD8 +脾T细胞的活化更弱。其他研究表明,体外低氧暴露会导致代谢物(S)-2-羟基戊二酸(S-2-HG)在细胞内积聚,从而深刻改变CD8 + T细胞的活化和分化,抑制细胞因子的分泌和溶细胞能力。但有趣的是,在小鼠模型体内转移后增强增殖,长期生存和抗肿瘤反应。糖酵解活性通过组成性HIF-1α活性(通过有条件地敲除HIF-1调节剂Vhl来实现)实际上促进了疫苗模型中长效效应记忆细胞的数量。其他工作表明,缺氧诱导了TME中各种细胞外切核苷酸酶CD39和CD73的表达,这些酶将TME中的ATP分解为腺苷。腺苷是A2A和A2B嘌呤能受体的配体,它们在广泛的免疫细胞中表达,并且广泛地具有免疫抑制作用,抑制效应细胞功能和Teff细胞增殖。有趣的是,补充氧气通过下调腺苷信号传导途径来增强小鼠T细胞的抗肿瘤免疫反应。缺氧对抗肿瘤T细胞的影响是一个不断发展的研究领域。考虑到肿瘤中低氧区域的普及以及低氧对适应性免疫反应的深远影响,其进一步的研究将显然有益于免疫治疗领域。

由于NK细胞在主要组织相容性复合物I类(MHC-I)下调(癌细胞的常见逃避策略)期间杀死细胞,所以它们形成了先天反应的关键效应组成成分。在体外,NK细胞的细胞因子刺激(IL-12和IL-15)后,有氧糖酵解和OXPHOS在代谢上被上调。有趣的是,在体外NK细胞刺激过程中,这些细胞因子诱导的代谢变化需要SREBP转录因子。在体外,SREBP活性的药理抑制作用抑制了代谢重编程,细胞因子产生和细胞毒性,并在过继性NK细胞小鼠模型中减少了抗肿瘤反应。有趣的是,据报道内源性SREBP抑制剂(例如27-羟基胆固醇)可在TME中增加,因此可能是NK细胞抑制的机制。小鼠的肺癌进展和与肿瘤相关的转化生长因子-β(TGFβ)与肿瘤相关的NK细胞中果糖-1,6-双磷酸酶(FBP1)表达的增加有关。FBP1是糖异生的关键酶,一旦激活,FBP1会强烈抑制NK细胞的糖酵解,从而导致功能障碍和活力降低。有趣的是,FBP1的药理抑制作用足以在体外重建糖酵解代谢以及细胞因子的产生和细胞毒性,并改善过继细胞疗法小鼠模型的抗肿瘤反应。这些研究表明,通过FBP1抑制来挽救NK功能取决于葡萄糖代谢的恢复,因为用2-脱氧葡萄糖(2-DG)阻断葡萄糖代谢阻止了FBP1抑制引起的拯救。2-DG本身也导致NK细胞功能异常,这表明抑制葡萄糖代谢可能对NK细胞抗肿瘤反应产生深远影响。TME内的其他代谢紊乱也可能影响NK细胞功能。例如,精氨酸水平低会损害NK细胞的增殖和IFNγ的产生,而缺氧会抑制细胞溶解活性。在体外研究中,人类NK细胞激活受体(例如NKp46和NKp30)在响应低氧或精氨酸水平较低时受到抑制。如在TME中一样,高乳酸水平和相关的低pH值在体外研究中也抑制了NK细胞的细胞毒性,细胞因子产生和NFAT信号传导。最后,TME中腺苷水平升高可强烈抑制NK细胞效应功能和增殖。
其他先天细胞,巨噬细胞和DC也会在激活时引发特定的代谢程序。在早期的体外研究中,将巨噬细胞分为炎性(M1)或免疫抑制(M2)表型,但很少有证据表明这些极化表型在体内发挥着独特的作用。最近发现了以不同转录状态为特征的一系列巨噬细胞表型。也就是说,具有炎性特征的巨噬细胞在抗肿瘤免疫中发挥重要作用。葡萄糖代谢是巨噬细胞中炎症表型的重要方面。被Toll样受体激动剂激活后,这些细胞显示出糖酵解基因的表达增加,葡萄糖摄取的高水平,乳酸的产生增加以及谷氨酰胺过表达。这种代谢重编程导致琥珀酸水平升高,从而通过稳定HIF-1而增加了炎性细胞因子IL-1β的表达。炎性巨噬细胞还特别依赖于PPP来产生NADPH,13C-葡萄糖示踪研究证实,通过激活培养物中的炎性表型,通过该途径的葡萄糖路径增加。NADPH对于产生高水平的ROS(作为氧化性爆发的一部分)是必需的,这是这些细胞的关键效应机制。精氨酸也是促炎性“ M1”巨噬细胞功能中的关键营养物质,因为在体外研究中,精氨酸比其他活化或“ M2”极化巨噬细胞表达更高水平的诱导型一氧化氮合酶(iNOS)。iNOS需要精氨酸才能产生细胞毒性一氧化氮,这是抗肿瘤反应的重要促炎介质。
TME中特定的营养缺乏,特别是葡萄糖和精氨酸,会严重限制这些细胞中新陈代谢和效应程序。葡萄糖限制不仅可以整体抑制糖酵解,而且可以降低PPP活性和TCA循环功能,从而限制了NADPH,ROS和琥珀酸酯的生成,所有这些都可以严重限制M1巨噬细胞的功能。2-DG的糖酵解抑制作用显着减少了巨噬细胞促炎细胞因子的分泌。
癌症免疫逃逸的新陈代谢
免疫抑制性Treg细胞优先依赖TCA循环和线粒体呼吸。尽管初步研究表明Treg细胞对FAO的依赖性并未说明依托莫昔的脱靶作用,但其他研究表明,FAO确实支持Treg细胞中的OXPHOS,尽管不是唯一途径。与Teff细胞相反,Treg细胞在体外显示降低葡萄糖摄取并表达较低水平的GLUT1的表达。有趣的是,尽管糖酵解似乎并未在Treg细胞分化或长寿表型中发挥关键作用,但据我们发现,一部分高活性Treg细胞(称为效应Treg细胞)依赖于糖酵解的上调以获得最佳功能。Treg细胞似乎具有新陈代谢的灵活性,可以在相对苛刻和异质的条件下(例如TME)生长。为此,据报道,Treg细胞转录因子FOXP3通过抑制MYC(有利于OXPHOS和NAD(H)氧化)来重新编程细胞代谢。在低葡萄糖和高乳酸的条件下(例如在TME中发现),这些适应作用使这些免疫抑制细胞具有代谢优势,从而使Treg细胞能够在体外抵抗乳酸诱导的功能性和增殖性抑制(不同于Teff细胞)。在体外实验中,培养基中的葡萄糖或谷氨酰胺缺乏(导致细胞内αKG减少)可以改变CD4分化并促进Treg细胞的发育。
TAM表型为高度免疫抑制。像Treg细胞一样,M2巨噬细胞上调FAO和线粒体呼吸。尽管早期研究表明FAO必须在M2巨噬细胞中发挥作用,但并未考虑到CPT1A抑制剂etomoxir的脱靶作用,但由于过表达Pgc1α引发巨噬细胞而导致免疫抑制表型,并且抑制促炎细胞因子的产生。M2巨噬细胞以不同于炎性巨噬细胞的方式代谢氨基酸,表达高水平的精氨酸酶1(ARG1),这会消耗精氨酸并生成多胺,多胺是伤口愈合的重要介质,但也具有高度免疫抑制作用。
虽然可以通过抑制许多代谢途径来减弱Teff细胞的激活,增殖和功能,但是其他属性,例如重新刺激时的长期生存力或效应功能可能增强。尽管用2-DG抑制糖酵解代谢抑制了Teff细胞的产生,但它也使T细胞趋向于长效记忆表型。有趣的是,在再次输注用于肿瘤治疗之前,在离体T细胞活化和扩增过程中阻断糖酵解,不仅可以提高抗肿瘤T细胞的存活率,还可以改善细胞因子的产生和细胞毒性。此外,有研究证明了该途径在维持谷氨酰胺阻断的CD8 + T细胞中维持代谢稳态方面的重要性。这些发现可能表明一种普遍的治疗策略,即阻止使用典型的代谢燃料(例如葡萄糖或谷氨酰胺)可能使某些癌症在代谢上受到损害,但鉴于抗肿瘤性T细胞使用其他来源的能力,它们可能会在代谢方面保持完整和正常运转,如醋酸盐。尽管可以通过药理学方法将特定的代谢干预作为检查点封闭的辅助手段引入,但这些靶点可能特别适用于CAR T细胞疗法,其中可以通过遗传手段精确定义代谢途径。
定义检查点疗法的代谢后果和其反应后的代谢情况都非常有意义。在多项研究中,检查点信号已显示出调节代谢的作用。例如,癌细胞上PDL1的表达可以驱动癌细胞中Akt-mTOR的活化和糖酵解,增加葡萄糖的摄取并增强与T细胞竞争葡萄糖的能力。人胃癌组织中T细胞中的CD155-TIGIT信号传导抑制了葡萄糖的摄取,乳酸的产生以及糖酵解酶GLUT1和HK2180的表达。相反,与同种型处理的对照T细胞相比,共刺激途径GITR的激动作用广泛提高了T细胞的代谢活性和增殖。最后,活化的人T细胞上的体外PD1和CTLA4信号抑制了与T细胞活化相关的代谢途径,如有氧糖酵解。为此,将代谢抑制剂与检查点抑制剂结合使用的前景有望提高检查点封闭的疗效。同样,通过对T细胞进行代谢重编程以使其更强大,持久的记忆细胞可能会改善其对检查点抑制剂的反应。最近的临床试验预示了抗叶酸培美曲塞与抗PDL1免疫检查点封闭的结合。除具有直接的抗肿瘤作用外,培美曲塞治疗还增强了抗肿瘤CD8 + T细胞的代谢适应性和效应功能,并诱导了癌细胞的免疫细胞死亡,从而触发了免疫反应。
免疫代谢的基础已从癌症代谢的观察中获悉,而癌症与免疫代谢重编程之间存在的明显差异能够为靶向代谢提供机会,以此作为增强免疫疗法功效的手段(图3)。这种方法可以通过许多不同的策略来实现。这些措施包括:靶向肿瘤代谢程序以抑制生长和改变TME;靶向抑制性免疫细胞的代谢以抑制其功能;以及靶向效应细胞代谢以增强肿瘤杀伤力。同样,在过继细胞治疗之前,T细胞代谢途径的体外药理或基因重编程也可以增强其功能,包括延长寿命或增强效应功能。

往期精彩推荐
Development Cell 前瞻性聚焦 | 代谢物在蛋白质修饰组学及细胞生长信号中的调控作用
2020-09-02

Nat Met | 刘兴国组报道乳酸化修饰介导细胞命运的“表观组-代谢组-表观组”跨界调控
2020-08-25

“多面手”乳酸调控之---肿瘤微环境
2020-08-21

“多面手”乳酸调控之---肿瘤免疫抑制
2020-08-11

Nature Metabolism | 为乳酸正名:能量代谢中的丑小鸭
2020-08-03

Nature亮点丨胚胎发育过程中与癌细胞Warburg效应之间的异曲同工之处
2020-07-27

Nature重磅:翻译后修饰家族“新宠”,全新乳酸化修饰研究如何展开?
2020-07-23


文章作者
推荐