Nature:“生命字母表”中的新成员
众所周知,地球上的一切生命都可看作是五个字母(A, G, C, T, U)的编码组合,这五个字母代表了核苷酸内的五种不同碱基。日前,科学家构建出了可以将非天然 DNA 碱基对稳定代代相传的新型有机体,这一成果意味着我们将对生命的基础重新定义。
一直以来,所有生命有机体都是通过核酸内的五种不同碱基:腺嘌呤、胞嘧啶、鸟嘌呤、胸腺嘧啶以及尿嘧啶,来实现遗传信息的储存及代代相传的。在核酸双螺旋结构中,这些碱基通过固定的配对方式形成碱基对。具体来说,在 DNA 中,腺嘌呤与胸腺嘧啶,鸟嘌呤与胞嘧啶分别互不配对,在RNA中,则由尿嘧啶代替胸腺嘧啶与腺嘌呤配对,所有的生命体都遵循着这样的规则,没有例外。然而,前不久的一项研究结果表明,我们一直所坚信的生命遗传“字母表”似乎只是一个巧合,而并非是不可改变的。该研究中,科学家合成了其它碱基对,并利用体外实验证明了这些碱基对可以被 DNA 复制酶类进行处理。由于地球上的生命具有生化均一性的特点,因此,想要证实遗传“字母表”被扩充,是需要强大有力的实验证据支持的。 Malyshev 等人在《自然》(Nature)杂志网站上发表了文章,给出了“字母表”被扩展的证据,他们的研究表明非天然碱基对可以在大肠杆菌(Escherichia coli)中稳定传递至下一代。
在发现 DNA 结构不久,就有人提出可能存在和天然碱基配对类似的第三种配对形式,但之后又过了将近30年,直到有机合成领域以及 DNA 扩增技术得到了长足的发展,才使得科学家有条件去验证那个早就提出的假设。1989年,科学家利用鸟嘌呤和胞嘧啶的同分异构体合成了新的碱基对,并在体外对含有合成碱基对的 DNA 序列进行了复制、转录及翻译。1995年,又有研究者带来令人惊喜的结果:在互补配对过程中,碱基之间形成氢键并非是必需条件,如果在空间上能够具有相容性(也就是分子形状彼此契合),或者形成疏水性的相互作用力,也同样可以维持碱基配对所形成的空间构型。这一研究证实了三种独立的剪辑配对方式,每种在体外实验的复制保真率都超过99%。
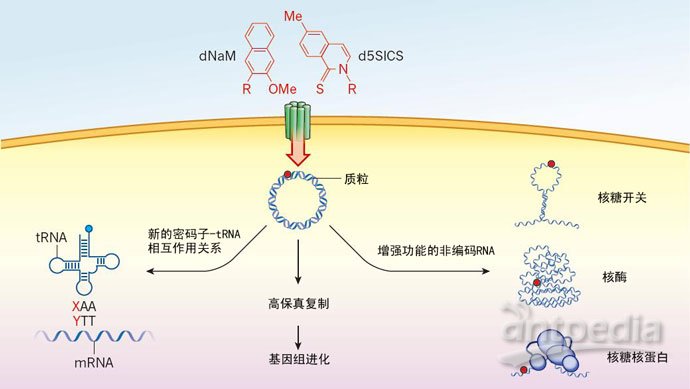
Malyshev 等研究者构建了一种细菌,它可以准确复制含有疏水性 d5SICS:DNAM 碱基对的质粒,质粒是一种小的环状 DNA 分子(图1)。由此,便产生了第一个含有来源于基因工程操作的、含有扩充了的“遗传字母表”的有机体。这个研究成果堪称一项壮举,而且远非说起来的这么简单:研究者需要首先找到一种方法,使细菌摄入非天然的核苷酸,然后使这些核苷酸能够被那些已经按照既定规则“运行”了数十亿年的“老古董”聚合酶所识别和处理,聚合酶是用来合成核酸大分子的酶类物质。
图1 含有非天然 DNA 碱基对的有机体的前景。 Malyshev 等人构建了一株表达藻类转运蛋白(绿色)的埃希式杆菌,杆菌能够从培养基内摄入非天然核苷三磷酸 DNAM :d5SICS碱基对(红点)。从而赋予有机体多种生物可能性:如增添新的遗传密码子(XAA和YTT分别是tRNA和mRNA的反密码子和密码子;X和Y代表非天然碱基,A和T是天然碱基);那些可以使用非天然碱基对进行复制遗传的有机体有可能带来基因组的进化发展;非编码RNA(如核糖开关,核酶以及核糖核蛋白内的RNA)可以扩展其功能。Me,甲基;R代表核苷三磷酸内的糖及磷酸基团。
为解决第一个问题, Malyshev 等人人工构建了一个大肠杆菌(E. coli)菌株,使该菌株表达藻类核苷三磷酸转运(NTT)蛋白,这个大肠杆菌菌株可以直接摄入核苷酸d5SICS及 DNAM 。为确保高效复制,研究者将非天然碱基对置于质粒中的一个特殊位置,这个位置只会被 DNA 聚合酶I识别进行复制。 DNA 聚合酶I不像那些 DNA 复制中勤勤恳恳的“老黄牛”那样,一个个把核苷酸连接起来,相反,它负责把 DNA 分子间的空隙连接起来,或者将 DNA 冈崎片段连接起来。用这样的方式对 d5SICS:DNAM 碱基对进行复制,无疑是十分高效的,这一点已经被体外实验证实。
在把含有一个 d5SICS:DNAM 碱基对的质粒引入到大肠杆菌中,并给培养基中也增加了这两种非天然核苷酸后,研究者发现在经过数天培养后,非天然碱基对仍然出现在质粒中。他们用一系列方法证实了回收到的质粒中存在着非天然碱基对。在细胞经过15小时的生长以及质粒复制后,经实验证实,质粒每次复制中,非天然碱基对的复制保真率都能至少达到99.4%,这可以和某些病毒聚合酶相媲美。
接下来的一步是需要确保这种复制可以更长期的进行下去,也就是需要使有机体能够自主将非天然碱基对当作它们自身的遗传“字母表”来进行合成。如果可以做到这一点,将意味着基因工程技术将引导我们迈入一个新的阶段。这也许看起来是异想天开,但我们要承认,曾经我们也认为几十亿年来所遵从的遗传密码是不可打破的,但现如今我们也用事实证明了这个密码的改写是可能的。
如果非天然碱基对不仅可以被有机体耐受,而且还可以被主动接受并加以利用,那么,接下来的关键一步将是证实它们可以在体内被转录生成RNA。如图1所示,可以通过很多种方式实现这一目标。例如,非天然核苷酸碱基对可以增加功能性RNA元件的数量,如核糖开关及核酶等。将非天然核苷酸整合入 DNA 启动子序列或者阻遏蛋白结合位点(这些序列作为蛋白质结合位点,分别可以启动或者抑制基因表达),加之对其搭档蛋白的基因改造,用这样的方法也许可以构建新的独立调节机制。
相似的基因工程改造技术同样也可以为RNA-蛋白质复合物提供新的功能,比如,通过限制Cas9酶(一种广泛用于解开 DNA 双链的工具酶)结合到包含非天然碱基对序列的位点,来实现这一目的。但是需要注意的是,可能最终在应用这些非天然碱基对时,需要在我们现在熟识的密码子-转运-RNA相互作用过程中,添加新的遗传密码子。遗传密码子指的是由3个连续的核苷酸组成,用于编码合成蛋白质所需要的氨基酸种类。这将极大地扩充可用于蛋白质翻译过程中密码子的数量,从而产生具有更多新功能的产物,例如编码新的类型的氨基酸;同时也避免了合成生物学家在基因工程操作中,因使用现有遗传密码子,为产生新的翻译产物需要重新编码的麻烦。换句话说,一个扩展了的遗传字母表必将帮助我们建立一个扩展了的翻译字母表。
但为什么 DNA 的遗传信息就停留在六个字母(三对碱基对配对)的阶段了呢? Malyshev 等人所使用的NTT可能纯度不高,同时引入了天然与非天然的核苷酸,而没有加以区别。其它研究小组所得到的非天然碱基对可以同时作为转运蛋白及细胞内遗传信息复制过程中所需的底物。如果将 d5SICS:DNAM 引入大肠杆菌的技术也适用于其它碱基对,那么 DNA 遗传信息编码便可以扩展到这三对碱基对之外。这就提出了一个关于生命的基础问题:为什么有机体会倾向于选择两对碱基对的配对法则,而那些可以储存更多遗传信息的半合成有机体,是否意味着会具有更多如上文我们所设想的功能,或者将会由于 DNA 复制中更低的保真性,RNA的错误折叠或者翻译过程中更多的差错,从而产生更多的问题。
为扩展遗传字母表的所做的努力,可看作是对 DNA 的共同性质勇敢地提出的质疑,同时也可能引来反对声。合成生物学家应该在反对声一出来,就马上给与坚决的回击。James Watson和Francis Crick的发现,开启了遗传学新的篇章,而现在我们已经到了迈入遗传学下一个时代的时候,我们将看到更加多样丰富的世界,这将为我们在未来更好地了解生物世界打下坚实的基础。