Nature:诺华发现,这种“胶水”可杀死癌细胞
磷酸酶作为一种在多种细胞信号通路中发挥重要作用的蛋白,几十年来,科学家们在磷酸酶上已经花费了无数时间,却难以开发出以它们为靶标的药物。
直到最近,诺华生物医学研究所的研究人员发现了一种新颖的方法来阻断其中一种磷酸酶——SHP2。
SHP2在许多癌症中都有涉及。在对其研究中,研究团队鉴定了几个化合物能够像胶水一样,通过粘合这些蛋白质将其沉默关闭。进一步研究还显示,这些“分子胶”能在小鼠中杀死人类的癌症细胞。这个发现于7月7日发表在Nature上,目前诺华的团队正在为了做患者中的测试而对这种抗肿瘤“胶水”进行优化。
文章的通讯作者Pascal Fortin不胜欣喜的说:“我们是第一个发现药物那样的分子能够阻止这个重要的靶标的团队。”
为什么是SHP2?
为什么诺华的科研人员会对SHP2感兴趣呢?
SHP2的全名叫做蛋白酪氨酸磷酸酶2,它与乳腺癌、白血病、肺癌、肝癌、胃癌、喉癌、口腔癌,以及其他多种癌症类型密切相关。SHP2一般由EGFR、 FGFR2、 HER2 和ALK等酪氨酸激酶受体所驱动。这样的酪氨酸激酶受体有30%在人类的癌症细胞系中被改变。它们活化调节细胞生长和分化的MAPK分析信号途径。
正因为SHP2在如此之多的癌症中起重要作用,文章的第一作者Ying-Nan Chen在2007年就第一次提出将它作为靶标。她说:“在过去的5年里,我们发现SHP2比我们最初所想的更重要。”
SHP2的重要性在一个大型的基因敲除实验中被发现。诺华的研究人员以390个人类癌症细胞系为对象,逐一敲除了7500个基因(几乎是三分之一的人类基因组),来观察细胞出现的问题。该研究小组发现了一个惊人的模式:在一个或多个酪氨酸激酶受体有改变的细胞中SHP2的降低让癌细胞几乎“残废”,也就是说癌细胞的生存依赖于SHP2。
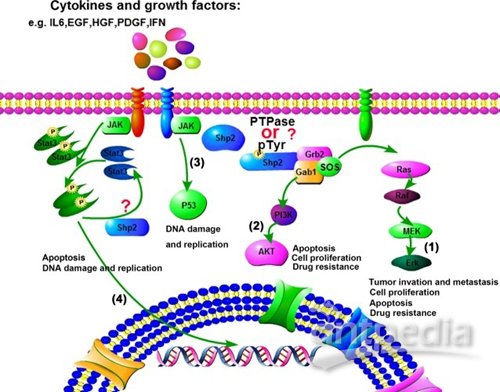
SHP2的主要信号途径和功能的总结 J Cell Mol Med. 2015 Sep; 19(9): 2075–2083
电荷的挑战
随着SHP2抑制剂治疗潜力的明确,如今,研究者比以前更想找到合适的药物候选。但他们必须克服一个主要的障碍:蛋白质的结构。
负责SHP2活性的主要部位具有巨大的正电荷,比较易于吸引带负电荷的分子。诺华的研究团队以前已经发现了好几个可以阻止SHP2功能的化合物,但它们都带负电荷。因为带电分子很难穿过细胞膜并到达它们的靶标,这一特点使得这些分子化合物很难成为有潜力的候选药物。
然而没有任何困境是持久不变的,换一种思路和方式,往往会柳暗花明。本文的另一通讯作者——诺华蛋白质组化学中心的执行董事Travis Stams说:“在针对SHP2活性位点进行研究的两年后,我们决定退后一步,重新审视其生物学。我们有一个预感能有一种截然不同的办法来关闭这个蛋白。”
SHP2“分子胶”的发现
正如PascalFortin事后解释:“我们的研究受益于SHP2就像一个铰链一样工作。当它打开时才有活性,并且我们能够将其保持关闭。”研究团队开始将目光投向SHP2不同的构象,琢磨它的铰链结构。
很快,研究团队意识到,活性位点只有在蛋白质被打开时才暴露出来。那么,是不是保持这个蛋白关闭就能让它沉默呢?于是他们设计了一个非常规的、多步骤的化学筛选来寻找候选物。而正是这样,导致了SHP2“分子胶”的发现。
通过晶体学和遗传突变实验,科学家们发现了一个化合物能够填补蛋白质靠近铰链处的一个孔,像胶水一样把所有东西“粘”起来。他们又将这种有类似药物特性的“分子胶”运用到包含酪氨酸激酶受体改变的人类肿瘤的模式小鼠身上,实验证明,癌细胞最终消失了。
事实上,这种“分子胶”其实是一种被称为SHP099的抑制剂,它具有一个变构作用机制,它通过该机制在一个自抑制的构形中使SHP2稳定。SHP099还能抑制RAS-ERK信号作用,从而在人类癌细胞系中和小鼠肿瘤异种移植模型中抑制由RTK驱动的癌细胞扩增。
Fortin说:“我们的发现具有治疗各种难治性血液系统恶性肿瘤和实体瘤的潜力。这也可能影响相关的肿瘤免疫学领域,因为有一些证据表明SHP2可以调节免疫功能。”
值得一提的是,该研究挑战了行业内关于困难靶标的教条。很多团队都试图阻断磷酸酶却失败,导致很多研究者将它们贴上了“无药可救”的标签。不过Keen说:“如果你持续专研这些困难的靶向就会变成‘有药可医’”。
-
科技前沿
-
项目成果