Nature医学:解读肿瘤外显子组新平台
在迈向个体化医疗的进程中,癌症基因分型正变得越来越复杂。利用分析芯片来捕捉成百上千潜在重要基因发生的变异,可以帮助医生确定一种特定肿瘤的运作机制以及最佳的疗程。全外显子组测序(Whole-exome sequencing,分析基因组的所有编码区域)一直是临床肿瘤学领域的一个“白日梦”,发表在5月19日《自然医学》(Nature Medicine)杂志上的一项研究为分析癌症患者肿瘤全外显子组提供了一个平台。
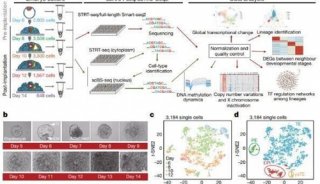
这一新的全外显子组平台从保存肿瘤样本中提取出DNA,对基因组中的所有编码区域进行测序,随后通过一种算法运行数据,解读揭示出的遗传变异的意义,由此挑选出可用治疗方案可靶向的那些遗传突变。重要的是,这一实验方案所采用的肿瘤样本是通过福尔马林固定,石蜡进行包埋——这是一种常规的肿瘤组织保存方法,但往往会给测序造成麻烦。
马克斯普朗克分子遗传学研究所癌症生物学课题组负责人Michal-Ruth Schweiger(未参与该研究)说:“能够对这类保存材料运用测序技术,将使得我们能够利用大量的样本。”Schweiger曾成功测序福尔马林固定、石蜡包埋的样本,但比当前研究作者们所取得的规模要小很多。
该研究的主要作者、哈佛医学院和Dana-Farber癌症研究所医学讲师Eliezer Van Allen说,不只是重新设计一些芯片靶向有限数量基因,随着越来越多的遗传信息涌现,捕获全外显子组具有重要的意义。
Van Allen和同事们设计出了一种叫做PHIAL的算法,可以基于生物学活性和临床相关性挑选出患者肿瘤中的一些遗传变异。他们利用PHIAL在511名患者样本的总共250,000个变异中挑选出了1,842个变异,当前有一些现有的药物可以作用于包含这些变异的基因。
为了证实PHIAL适用于进行临床决策,该研究小组挑选出了一名罹患转移性肺癌的患者。“结果表明这名患者携带一种非常罕见的KRAS突变,而在通常情况下我们无法检测到它,”Van Allen说。CDK4抑制剂被认为能够阻止表达KRAS的肺细胞生长,非常凑巧的是该名患者被招募到了一项针对CDK4抑制剂的临床实验中,并对这种治疗产生了反应;这是针对他唯一取得成功的一种治疗方法。“它提供了一个令人信服的例子表明了我们想在更广泛的范围内这样做的原因,”Van Allen说。
该研究小组构建出了一个临床可靶向基因数据库,至今已纳入了130个基因,可在线免费使用这一数据库。Van Allen和研究小组还打算让人们能够免费获得PHIAL程序。Roychowdhury说,这一平台为致力扩展癌症基因组用途的其他研究组提供了一个极好的模型。