查看完整版本请点击这里:
【求助】二维电泳帮我分析下我的图吧
这是为什么呢,因为我的研究生课题其中一部分是大肠杆菌(Escherichia coli)(Escherichia coli)(Escherichia coli)二维电泳,我做了整整一年二维电泳都没有结果(另有一年在做基因芯片),我真是想死的心都有了,如果我还做不出来,老板是不会让我毕业的,我不想再延期了,呜呜呜,身边求助的人都没有,我只能整天埋着头做实验,蛋白质组相关的文献和书籍不知道学习了多少遍,还是没有用,实验失败了无数次,我怎么办啊,怎么办啊。。。。。。只希望路过此帖的朋友能帮我下,我真的是一点办法都没有了,我的问题如:【求助】二维电泳帮我分析下我的图吧
查看完整版本请点击这里:
【求助】二维电泳帮我分析下我的图吧
【求助】二维电泳帮我分析下我的图吧
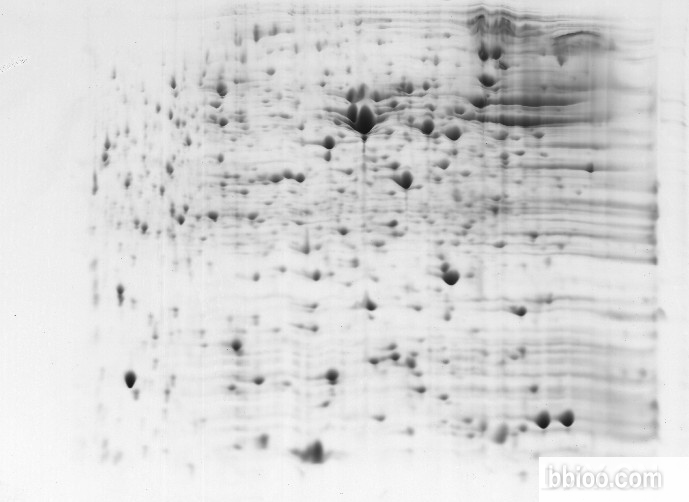
20150828_71bbb952d49a681bef2b3P1mYcmKC5W8.png



最新回复
hcy517 (2016-3-16 10:55:21)
考染图,酸性端横纹很多,IEF聚焦不好,或者根本没有聚焦,仔细想下自己的操作有什么该注意而没有注意到的细节.
比如,IPG胶条是否完全浸润到样品上. 样品在上样前有没有离心一下,去除不可溶性杂质. 还有就是样品中的盐离子浓度高也影响聚焦. 例外检查下酸性端的胶条是不是有问题啊.我也碰到过类似问题,换了一批胶条就没问题了.
总之,影响结果的因素较多,楼主要逐一排除,找出问题根源.
美人鱼 (2016-3-16 10:55:54)
样品处理是否得当啊.
还有银染灵敏度高,取单个点去做质谱,也可能量太少,质谱鉴定不出.
没有细节不好妄加推断.
燕子@ (2016-3-16 10:56:15)
你可以把具体条件详细说明一下 大家也好帮你分析
哈密瓜 (2016-3-16 10:56:50)
考染的IEF是100v,3h;200v,1h;500v,1h;1000v,1h;1000-8000,1h;85000vhr;500v,8h
还有就是银染上样量是50ug,考染上样量是500ug,其他的都是一样操作,IEF都很正常,顺利聚焦,我就不知道是不是银染上样量少,考染上样量多杂质就相应的多起来了,才会导致酸性端聚焦不好呢
886爱 (2016-3-16 10:57:12)
1. 用双蒸水洗银染后的胶2-3次,每次10分钟。
2. 剪刀将 200 μl Eppendorf 吸头尖端剪掉约1cm,孔的直径约为1mm,用修剪后的吸头从凝胶上戳取蛋白质点,再转入200μl离心管中。
3. 每管加入50μl脱色液(100 mM 硫代硫酸钠与30 mM 铁氰化钾1:1混合),加完震荡,颜色脱去后马上加水冲洗停止反应,震荡,2分钟内吸出。再加水数次,直至洗掉全部脱色液为止。
4. 加入50%的乙腈,洗1-2次,每次15分钟。
5. 100%乙腈脱水1-2次
6. 25mM 碳酸氢铵吸涨5分钟。
7. 100%的乙腈脱水后,冷冻真空干燥20分钟。
8. 加入8μl (浓度为10ng /μL)溶于20mM碳酸氢铵的胰蛋白酶(测序级)4℃吸胀1小时。吸去多余的酶液,将管子倒置,37℃空气浴过夜。
9. 每块胶加入8μl 5%三氟乙酸,37℃ 1小时,将液体吸净转移至一干净的离心管中,每个蛋白质胶块再加入8μl 2.5%三氟乙酸/50%乙腈,30℃ 1小时,吸出液体与前一次的提取液合并,抽真空
10. 抽干的样品可于4℃放置一个月,也可用2μl 0.5%三氟乙酸充分溶解肽段立即进行质谱鉴定
mimima (2016-3-16 10:57:55)
考染图,酸性端横纹很多,IEF聚焦不好,或者根本没有聚焦,仔细想下自己的操作有什么该注意而没有注意到的细节.
比如,IPG胶条是否完全浸润到样品上. 样品在上样前有没有离心一下,去除不可溶性杂质. 还有就是样品中的盐离子浓度高也影响聚焦. 例外检查下酸性端的胶条是不是有问题啊.我也碰到过类似问题,换了一批胶条就没问题了.
总之,影响结果的因素较多,楼主要逐一排除,找出问题根源.
PS: 实验操作细节一点要多加留心额~
p1900 (2016-3-16 10:58:15)
danzi (2016-3-16 10:58:44)
上样量在正常范围内,不过你蛋白浓度多少呢?如果说因为考染的上样量增加了而导致杂质也增加了的话,我觉得问题还是出在样本纯化上。其实我一直做银染,对考染不了解。不过你这个是不是胶体考染啊,貌似胶体考染效果会好点。
关于银染的打点,只要确定不用戊二醛,除了量多少的影响,应该就没问题了。或者你干脆挖下来点,送出去鉴定好了。这样结果出的也比较快
8899 (2016-3-16 10:59:08)
大大 (2016-3-16 10:59:36)
【求助】二维电泳帮我分析下我的图吧