诚信认证:
工商注册信息已核实! 扫一扫即可访问手机版展台
扫一扫即可访问手机版展台
应用光阻法和流式成像方法定量评价治疗性蛋白注射剂中不溶性颗粒
| 领域: | 蛋白/抗体/蛋白质组 | ||
| 样品: | 蛋白注射剂中不溶性颗粒 | 项目: | 光阻法和流式成像方法 |
| 参考: | https://www.dksh-instrument.cn/Solution/407 | ||
| 方案文件名 | 下载 |
|---|---|
应用光阻法和流式成像方法定量评价治疗性蛋白注射剂中不溶性颗粒 |
下载此篇方案 |
概述
流式成像(FI)作为一种强大的工具常被用做与光阻法(LO)形成正交的方法来评估来自蛋白质聚集物的不溶性颗粒。 然而,很少有报道直接比较FI和LO方法在商业治疗性蛋白注射剂中蛋白质颗粒的大小和数量。 在本研究中,我们使用FI和LO测量了几种治疗蛋白注射剂中不溶性颗粒的数量,并对这些颗粒进行了表征,以比较这些方法的分析性能。
通常用FI测得的粒子数远高于用LO测得的粒子数,其差异取决于粒子的产物或特征。 有些产品含有大量的透明的、细长的颗粒,这些颗粒可以逃脱LO的捕捉。 我们的结果还表明,与FI方法相比,LO方法低估了预充注射器产品中硅油滴的大小和数量。 使用FI测量的一个产品中≥10毫米颗粒的计数超过了使用LO方法的药典颗粒物质测试中定义的标准(每个容器6000计数)。 因此,应该注意在使用FI方法时所设定验收标准。
介绍
生物制药原料药和药品中的蛋白质聚集体和不溶性颗粒被认为是需要充分评估和控制的杂质,因为它们可能引起免疫原性。 为了控制生物制药产品中的蛋白质聚集体和亚可见颗粒,原料药和药品的纯度检测采用体积排除色谱法,药品的颗粒物质检测采用光阻法(LO)。 在药典中得到国际统一认识的针剂颗粒物质检测方法包括光阻法和显微法。 在重现性方面应优先使用LO法。 虽然本药检将注射中要检测的颗粒物质定义为“溶液中无意中出现的除气泡外的可移动的不溶解颗粒”。 实际上,来自蛋白质聚集物、辅料和制造过程的固有颗粒在实际测试中也时常被检测到。
利用LO评价蛋白质聚集体和不溶性颗粒有几个局限性。 在LO方法中,颗粒的大小和数量由被阻挡光源和传感器之间光通道的颗粒产生的脉冲信号的振幅和数量决定。 颗粒的大小是用由聚苯乙烯标准颗粒生成的校准曲线计算的。 然而,来自蛋白质聚集体的颗粒是半透明的,而且它们的折射率比聚苯乙烯标准颗粒低。 因此,LO可能低估了蛋白质不溶性颗粒的数量和大小。 因此,流动成像(FI)方法已经成为一种有用的工具来表征蛋白质颗粒和补充LO方法。 在FI技术中,当样品流通过流池时,通过捕获颗粒图像,可以确定颗粒的大小、数量和形状,并通过颗粒和分散液体之间的对比来确定颗粒的边缘。 因此,FI方法对于检测近透明颗粒具有更高的灵敏度。 然而,在USP下面提到的章节出版之前,FI方法还没有标准化或在任何纲要中被列出。
我们最近进行了一项合作研究使用LO和FI方法在三个不同的样本中测量和计数亚可见颗粒,以评估FI方法标准化的适用性。我们的研究表明,颗粒计数是使用来自同一制造商的FI仪器获得的,不同制造商的颗粒计数可能略有差异,考虑到观察到的实验室内可变性,这是可以接受的,FI方法具有与LO方法相当的实验室内和实验室间的可变性。 考虑到我们的数据,使用FI作为质量控制检测将是可行的,以精确分析治疗性蛋白注射的亚可见颗粒计数,尽管应该对每个产品进行验证研究。 最近美国药典出版了通则<1788.3>流式成像法测定亚可见颗粒物。
从这些情况下,使用FI方法作为附加的表征方法,可能增加测试项以补充质量控制。 然而,据我们所知,很少有报道比较使用FI和LO检测的商业治疗性蛋白注射剂中的不溶性颗粒,这可能会阻碍生物制药公司在质量控制测试中应用FI方法。 在这项研究中,我们使用LO和FI方法测量了商用治疗蛋白注射剂中存在的不溶性颗粒,以揭示颗粒特征(大小、形状和数量),并比较了FI和LO方法的检测能力。 此外,我们还讨论了从测量结果中使用FI方法时设置一个接受标准。
实验方法与材料
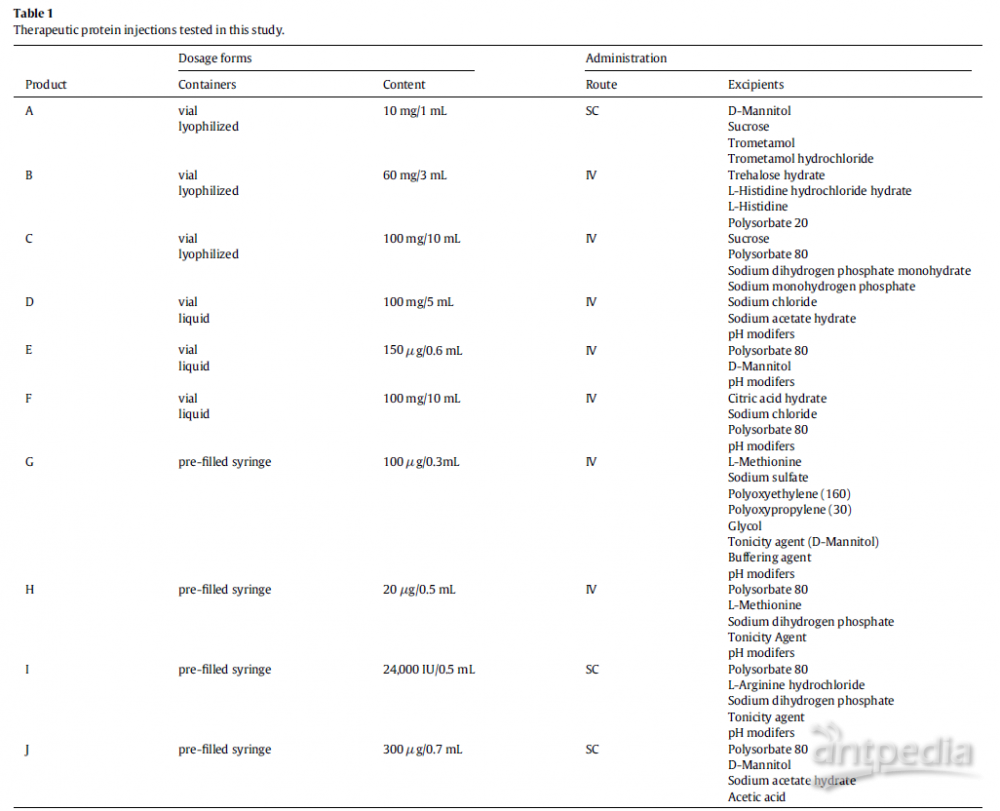
本研究使用了10种治疗性蛋白注射剂,产品A - J,如表1所示。 ENBREL_ 10mg (S.C.注射液)(批号: 15M01A, Pfizer Inc., New York, NY, USA), ESPO_皮下注射注射器(批号:15M01A) 16804T, Kyowa Kirin Co., Ltd., Tokyo, Japan), Filgrastim bs75 mg Inj注射器 MOCHIDA(很多没有。 AA18A, MOCHIDA制药株式会社,日本东京),GRAN_注射器(批号: 16103L, Kyowa麒麟股份有限公司,HERCEPTIN_静脉输液(批号:16103L) 16D070E, Chugai Pharmaceutical Co., Ltd., Tokyo, Japan),英夫利昔单抗BS用于静脉滴注100mg [NK](产品编号:16D070E)。 250060, Nippon Kayaku Co., Ltd., Tokyo, Japan), MIRCERA (lot no.) 16G010Z,中外制药股份有限公司,NESP注射塑料注射器(批号: 16719N, Kyowa Kirin Co., Ltd.), Rituximab BS静脉滴注500 mg [KHK] (lot no.) 17L01E,京和麒麟股份有限公司,VECTIBIX_静脉注射用(批号:17L01E) H127武田制药株式会社,日本东京)、大冢蒸馏水(大冢制药株式会社,日本东京)均从商业供应商处采购。 每次测试的产品都是在过期前使用的。 将冻干配方溶解在给定的溶液或蒸馏水中,并在产品溶解当天进行测试。
光阻法(LO)
使用KL-04A (Rion Co., Ltd., Tokyo, Japan)进行LO实验。 本仪器符合日本药典<6.07>注射剂不溶性微粒物质试验。 基于我们之前关于LO方法中减少测试体积的研究,我们在0.2 mL的样品体积下进行了4次LO测量。 皮重体积设定为0.2 mL,收集4个结果,丢弃个结果后分析3个结果。 颗粒计数是从2.0 ~ 100 mm范围内的颗粒数中获得的。
流式成像法
使用FlowCam 8100 (Fluid Imaging Technologies, Inc., Scarborough, ME, USA)进行FI实验。 在测量之前,通过确认10毫米聚苯乙烯标准颗粒(Count - cal Count Precision size Standards CC10-PK, Thermo Scientific, CA)的颗粒计数和尺寸在认证值内,仪器的性能得到验证。 流速、采样量、自动图像速率、采样效率和分割阈值(暗/光)分别设置为0.1 mL/min、0.2 mL、16帧/s、约70%和10/10。 分割阈值的值是基于我们之前的报告,以适当地检测更多的蛋白质不溶性颗粒 仪器用蒸馏水冲洗,必要时用1% Tergazyme (Alconox Inc., White Plains, NY, USA)溶液冲洗,流速为5 mL/min,确保流动池中没有主要颗粒。 在设置了仪器参数后,为了评估每个仪器的合格性,对700 - 1000毫升蒸馏水进行了测试,以确认在每1ml液体中存在小于100个大小为>2毫米的颗粒,并确保没有任何大小为>10毫米的颗粒。 在一次试验中,将400毫升的样品应用于仪器并测量三次。 收集并分析了三个结果。 颗粒计数是从2.0 ~ 100 um范围内的颗粒数中获得的。
硅油滴制备
将充有PBS的1mL注射器(Terumo 1mL注射器SS-01T)从20cm高度滴入20次,产生硅油滴,收集到管中。 然后将溶液静置2小时以去除气泡。
结论与讨论
通过LO和FI评估了常用治疗蛋白注射剂(包括6个小瓶产品和4个预充注射器产品)中的不溶颗粒。 治疗性蛋白注射剂颗粒计数见表2和表3,两种方法得到的颗粒计数关系见补充图1a和1b。 总体上,FI测得的粒子数高于LO。 然而,用FI和LO测量的颗粒计数比值在不同产品之间存在显著差异。 对于小瓶产品,产品D的颗粒计数比两种方法中最高,FI法的颗粒计数(≥10 mm)比LO法高100倍。 产品A - C和产品f的颗粒计数差异约为10- 50倍。相反,产品E的颗粒计数差异仅为2 - 4倍。预填充产品的颗粒计数差异一般为2 - 10倍。 不包括产品G,其差异为8-25倍。

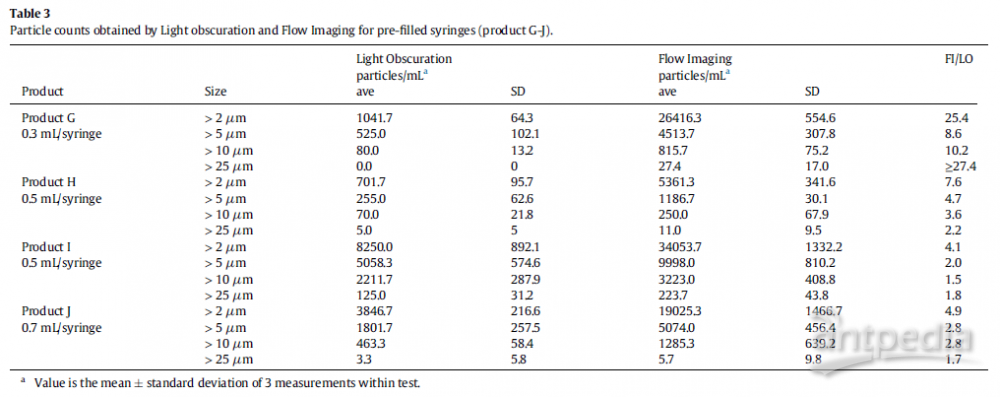
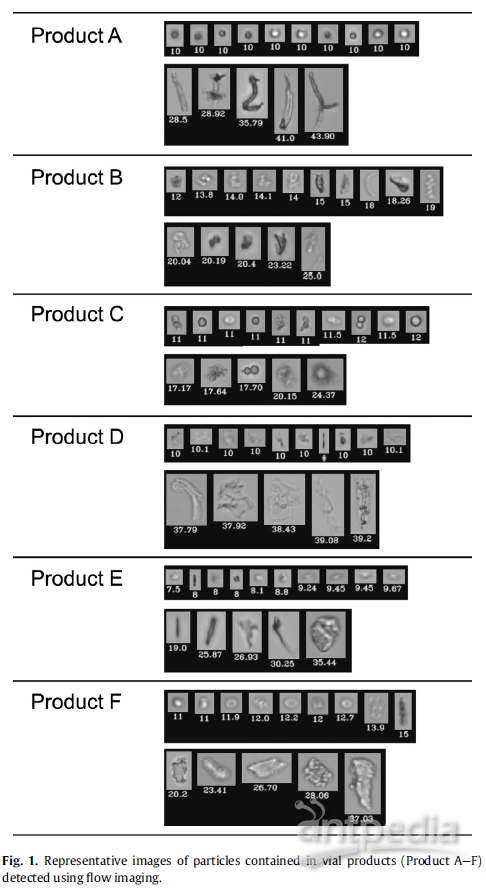
图1和图2给出了使用FI方法检测粒子的代表性图像。 在小瓶产品(产品A - F)中,产品D中观察到的颗粒大多是细长透明的(图1)。相反,其他产品除了细长透明颗粒外,颗粒相对致密且圆。 产品A、C、f中颗粒呈圆形或椭球状。产品E主要为致密颗粒,颗粒轮廓相对清晰,细长透明颗粒较少。 这可能是LO法和FI法在产品E的检测粒子数上没有显著差异的原因之一。 在使用FI和LO方法测量颗粒时,本研究没有使用涂有硅油的针头或注射器。 但是在产品A、E和F中观察到类似硅油滴的颗粒。使用硅油润滑的橡胶塞或灌装过程等制造过程可能会将硅油滴引入小瓶产品的溶液中。 一些报道指出,在治疗性蛋白注射剂中存在来自辅料的更小颗粒。因此,另一种圆形或致密颗粒可能来自辅料。 今后还需要利用x射线能量色散分析、元素分析、振动光谱和拉曼光谱等方法来确定其来源。

对于图2所示的预充注射器产品(产品G−J),从图中可以观察到的大多数颗粒是圆形的,认为它们来自于在注射器上润滑的硅油。 没有超过10毫米大小的细长颗粒。 为了阐明两种方法中硅油滴本身颗粒计数的差异,采用LO法和FI法测量了硅油滴数。 在注射器中滴入1ml PBS产生硅油滴。 结果证实,使用FI方法测量的颗粒计数比使用LO方法获得的颗粒计数高2 ~ 8倍(表4和补充图2)。
为了表征每个产品中存在的颗粒,我们分析了基于捕获图像的FI仪器计算出的颗粒参数。 图3为圆度随Sigma强度的等值线图。 选择这些参数是为了有效地可视化每个产品中的颗粒特征。 圆度值为1.0表示一个的圆。 Sigma强度是图像灰度值的标准差。 如果一个粒子的图像包含了亮部和暗部,那么单个粒子的灰度值的可变性很大,从而导致更高的sigma强度。 图3中,产品D的等高线图清楚地表明,圆度和sigma强度较低的颗粒比其他颗粒更容易被检测到, 表明这些颗粒逃过了LO法的检测(补充图2)。证实所有其他小瓶产品也含有较低圆度的颗粒,虽然也检测到了较高圆度和sigma强度的小颗粒,如图1所示。 相反,硅油滴表现出更高的圆度(最接近1)和西格玛强度(大约30),因为硅油滴的一张图片既有暗部也有亮部。 从产品G−J的等高线图可以直观地看出,预充注射器产品中几乎所有检测到的颗粒都分布在与硅油滴相同的区域,尽管在产品J中观察到一些拉长的颗粒。 有报道表明,利用多重过滤器、随机森林和卷积神经网络对硅油滴和蛋白质颗粒进行分类,FI方法是一种有用的方法。未来则会利用FI方法对硅油滴和蛋白质颗粒进行分类的合作研究是提出标准化分类器/模型。


在本研究评估的产品中,产品D的LO和FI方法的颗粒计数差异最大。从图1所示的颗粒图片和图3所示的等高线图中可以看出, 两种方法之间的颗粒计数差异随着产品中细长颗粒数量的增加而增加。 这一趋势与我们之前使用共享的蛋白质聚集体样本以及其他文章进行的合作研究的结果一致。 我们的研究表明,根据所测试产品中所含颗粒的特征,FI和LO方法的颗粒计数比率从2倍到100倍以上不等。 在另一项研究中,使用FI和LO方法测量的累积颗粒计数比在搅拌或加热的人白蛋白和多克隆免疫球蛋白上大约为3到50倍,也有报道称,预充注射器中低浓度治疗性蛋白产品的LO和FI方法的累积颗粒计数仅略有不同,这与本研究中E和H−J产品的结果一致,我们的结果与这些研究一致。 少数使用FI方法分析市面上可用治疗性蛋白产品的研究之一发现,某些干扰素-b产品中不溶性颗粒的数量超过100,000颗粒/mL,这表明我们在产品C和D中超过10,000颗粒/mL的结果并非不典型。
使用LO方法进行的现行药规颗粒物质测试的验收标准定义如下:“每个容器不超过6000个等于或大于10毫米,每个容器不超过600个等于或大于25毫米”。 当从表2的结果中计算每个容器中所有产品的颗粒计数时,使用LO方法检测到的所有颗粒计数都满足这些标准。 相反,使用FI法测量的D产品每个容器的颗粒数(≥10 mm)远远超过标准。 在本研究中,实际给予患者的颗粒数量将比使用FI方法检测到的颗粒数量小得多,因为D产品应该通过在线过滤器注射。 考虑到本研究使用市售治疗蛋白产品的结果,当使用FI方法作为质量检测时,针对单个产品设置验收标准,而不是参照LO方法的标准设置统一的验收标准,是合理的。 利用LO和FI方法对多种市售治疗性蛋白产品(如酶、单克隆抗体等)在有或无应激条件下的测量数据进行积累,对于FI方法的实际应用是必不可少的,我们的研究有望为实现这一目标做出很大贡献。
在这项研究中,我们比较了FI和LO方法对商业可用产品的检测能力,并讨论了FI方法的接受标准。 治疗性蛋白产品中所含的蛋白聚集物连续分布于纳米级到微米级,亚微米级的蛋白聚集物被推荐作为表征的一部分来评估生物制药产品的免疫原性风险。 在一项跨行业合作研究中,讨论了评估亚微米粒子的技术的效用和分析性能,如纳米粒子跟踪分析和共振质量测量。 在每个治疗性蛋白产品中积累从纳米到微尺度蛋白质聚集物的数据,将有助于未来建立更稳健合理的蛋白质聚集物控制策略。