CRISPR/Cas9技术或能增强治疗肝细胞癌有效性
声动力疗法(Sonodynamic therapy,SDT)能利用超声波与药物的结合,在肿瘤位点释放有害的活性氧(ROS),然而,这种疗法并没有十分有效,因为癌细胞会激活抗氧化剂防御系统来对抗ROS。近日,一篇发表在国际杂志ACS Central Science上题为“Ultrasound-Controlled CRISPR/Cas9 System Augments Sonodynamic Therapy of Hepatocellular Carcinoma”的研究报告中,来自中国同济大学等机构的科学家们通过研究利用CRISPR/Cas9基因编辑技术就突破了癌细胞的这种防御系统,从而就使得声动力疗法能够有效促进肝癌小鼠模型机体中的肿瘤发生萎缩。
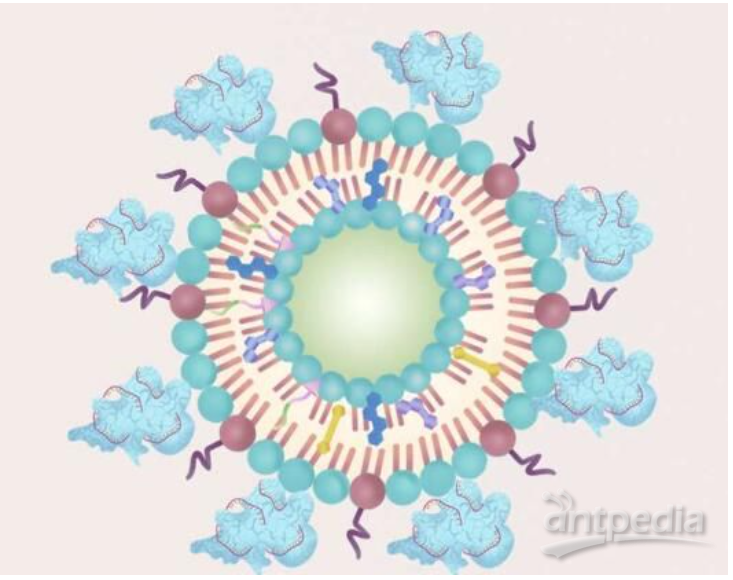
超声波照射肿瘤会导致脂质纳米颗粒释放有害的ROS和CRISPR/Cas9基因编辑系统
肝细胞癌是一种最常见的肝癌形式,患者预后往往较差,通过部分切除肝脏或移植健康肝脏的手术治疗并不适合与疾病处于晚期阶段的肝癌患者;由于超声波能渗透到组织深处,因此声动力疗法就能作为一种有效且无创的方法来治疗肝细胞癌。但目前,癌细胞能通过激活一种名为NFE2L2(核因子红细胞2相关因子2,nuclear factor erythroid 2-related factor 2)的基因来克服这种疗法的攻击,NFE2L2能部署细胞的解毒和抗氧化酶防御功能。CRISPR/Cas9基因编辑技术在实验室中能被用来敲除基因的表达,因此研究人员就想知道是否能利用该基因编辑技术降低NFE2L2的表达从而增加声动力疗法的有效性。
作为第一步,研究人员首先将CRISPR/Cas9系统和ROS前体分子封装到脂质纳米颗粒中,随后他们利用这种纳米颗粒来处理培养皿中的肝细胞癌细胞系,这种脂质纳米颗粒能被细胞中的溶酶体所摄入,而超声波疗法则会促进ROS的形成,从而破碎溶酶体并促进CRISPR/Cas9系统进入到癌细胞细胞核中,从而敲除NFE2L2基因的表达,ROS还会损伤其它的细胞组分,因此,与没有NFE2L2基因编辑的情况相比,会有更多的癌细胞因声动力疗法而发生死亡。

接下来,研究人员将纳米颗粒疗法注射到植入了人类肝细胞癌肿瘤的小鼠机体中,当将纳米颗粒和超声疗法联合作用15天后,小鼠机体中所有的肿瘤都消失了,而且癌症也并不会复发。仅声动力疗法治疗的小鼠则相比未治疗的小鼠携带较少的肿瘤,但额外加上CRISPR/Cas9系统后就会明显改善声动力疗法的治疗有效性,研究者表示,由于基因编辑至发生在超声照射的肿瘤组织中,其并不会导致健康组织发生基因突变,本研究由中国国家自然科学基金好上海市卫健委提供资助。
综上,本文研究结果或为未来人类肝细胞癌的管理提供了一种新的模式,同时也为CRISPR/Cas9基因编辑工具的广泛应用奠定了一定基础,其具有良好的临床转化前景,与此同时将基因编辑技术与声动力疗法联合使用或能展现出一种新型协同的癌症治疗模式。







