新发现可能拔掉病毒的“毒牙”
美国宾夕法尼亚州的Paul Berg生化和分子生物学教授Craig Cameron的新研究显示,研究人员或许可以随便改变一种帮助病毒增殖的酶,从而拔掉病毒的“毒牙”。他表示,这项新发行可能为发明一种快速、便宜的制造疫苗的方法开辟新路。
Craig Cameron表示,他们已经成功地检测了这项技术,并认为能够适用于大多数病毒类型。病毒都有一个简单的任务:感染细胞、复制更多的自己,然后从细胞突破出来感染更多的细胞。这就需要快速和有效的增殖。病毒是在一种称之为聚合酶的酶的帮助下完成这一任务。
一旦病毒感染一个细胞,就开始了一项时间竞赛:病毒试图以最快的速度增殖,而免疫系统则试图控制它们的扩散。如果病毒传播的速度超过免疫系统能够中和它们的速度,则会导致疾病甚至死亡。如果身体能够接种一种毒性被削弱的病毒疫苗,那么身体在接触到这种病毒的毒性病毒株时就能更快地做出应答。因此,研发疫苗的关键就是找到触发免疫系统应答但又不会导致生病的病毒突变株。
宾州的研究人员确定出了脊髓灰质炎病毒的聚合酶中的一个关键氨基酸,该酶控制着病毒增殖的速度和精确度。该聚合酶上的这个位点的细微的化学变化对削弱病毒产生巨大的影响。通过改变一个赖氨酸残基,不但能够改变病毒的复制,而且还能改变它们的拷贝精确度。
由于所有病毒都有类似的调节复制的机理,因此研究人员认为这项发现可能代表了削弱其他致病病毒的一个普遍适用的机制。
此前,美国威斯康星-麦迪逊大学霍华德休斯医学研究所进行的一项研究证实不同类型的病毒复制具有一些共同的特征,这些病毒包括一些引发人类严重疾病的病毒,如HIV、SARS和丙肝病毒等。这些重要发现将可能加深对病毒普遍弱点的了解,并且有助于研制出新一代广谱抗病毒药物。这项研究的论文发表在8月14日的《PLoS 生物学》上。
领导这项研究的Paul Ahlquist博士和同事描述了一种名为flock house virus(兽棚病毒,简称FHV,一种典型的RNA病毒)如何利用细胞内的蛋白膜结构来建造安全的“繁殖基地”的过程。
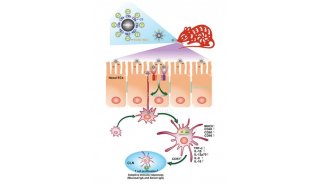
该研究小组借助强大的电子显微技术获得了首张FHV病毒复制复合体(replication complex)的三维图像。和其它病毒一样,FHV病毒也需要在宿主细胞内制造新的遗传物质来扩大感染。
研究人员发现,FHV进入宿主细胞线粒体的内外膜之间,并促使其制造了数万个气球状的囊或者小球。在它们的内部,一层蛋白外壳保护FHV成功逃脱了宿主的监测和防御机制,安全地复制出新的病毒基因组副本。
研究人员解释说,病毒显然已经拥有一种极佳的策略,它令宿主细胞为自身RNA合成创造出了新的迷你细胞器。其整个复制和装配过程都与细胞内的其他生理过程,尤其是防御响应完全隔绝。
此外,Ahlquist和同事还注意到,这些形成的囊或小球都具有狭窄的“颈”伸入线粒体膜外的细胞质,这是FHV病毒复制所需物质进入和新的病毒基因组放出的通道。
-
焦点事件
-
项目成果
-
焦点事件
-
项目成果
-
焦点事件