因打破传统而登上Science封面的神奇技术到底有多牛?
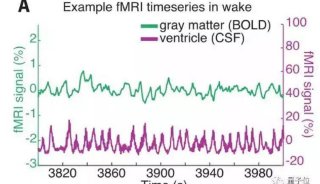
传统流式细胞分选技术具有速度快、通量高、灵敏度高的优势,但无法获取细胞亚结构信息及追踪细胞的动态活动,例如蛋白质运输、信号传导或疾病引起的蛋白质错误定位等。而荧光显微镜技术,可以看到细胞详细的形态和蛋白定位,但获取速度有限,并且无法将感性兴趣的细胞分离出来。虽然目前市面上已有基于图像的流式技术,但通量较低,且无法实现单细胞分选功能,限制了下游更深度的探索。
1月21日,欧洲分子生物学实验室 (EMBL) 与碧迪医疗(BD)在该领域取得重大突破,相关研究成果荣登《Science》杂志并获封面报道!
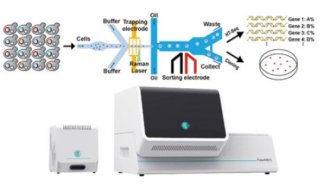
研究团队开发了一种High-speed fluorescence Image-enabled Cell Sorting (缩写:ICS) 高速荧光图像分选技术,融合了1)基于射频发射的高速荧光成像、2)传统石英杯液滴分选和3)独创的无延迟信号处理及电子系统,将传统流式分选和高速成像结合起来,实现高速捕捉基因组筛选中瞬时动态变化的细胞表型,并进行单个目标的分选。
独创的高速成像分选系统

488nm激光束被分为阵列,数字发射信号产生图片,包括FSC、SSC、light loss以及四个不同的荧光通道。如上图示例中,表达高尔基体标志物GalNAcT2-GFP的Hela细胞系,表面marker CD147 PE-CF594(橙色)、细胞核DRAQ5 (红),FSC、SSC、light loss(灰)
为了实现高速blur-free成像,ICS采用FIRE方法将发射光无延迟、即时地被转换成数字信号,实时图像分析,这是与其它技术最大的差别。每个光电探测器产生具有高频调制编码图像的信号脉冲,通过傅里叶分析构建图像。图像处理过程产生图像特有的空间特征参数,基于这些图像参数的评估,圈取感兴趣的细胞,下达分选指令。分选速度可达到与传统流式相当的15,000 events/s,捕捉昙花一现的动态空间表型,适用于下游如基因组规模筛选。

细胞器、亚结构成像,从上至下依次为:细胞膜、细胞、线粒体、细胞核、高尔基体、内质网、核、核膜、P-小体、卡哈尔体、中心体
ICS技术在样本快速流动下,仍可实现蛋白质分布的可视化,上图显示了一组结构、大小、形状和分布不同的13个亚细胞结构,证明了它的广泛适用性。

图像空间参数及应用:A:size parameter,像素点的数量, eGFP-Ki-67信号区分具有单个小核仁和多个或大核仁的细胞;B:radial moment,距离中心的位置,DyeCycle Green信号区分单个或多个核细胞;C:eccentricity,细胞的拉伸程度,区分圆形或拉长形状的细胞;D:maximum intensity,信号聚集度,GalNAcT2-GFP信号区分处理和未处理细胞;E:correlation,相关度,区分RelA和DRAQ5信号重叠程度研究团队独创了ICS技术的空间图像专用参数,并与常规流式信号所用的参数(面积A、宽度W和高度H)联合,以实现基于图像的流式分选。这些参数可以量化细胞的空间特征,在不同的应用中区分以往只能通过显微镜技术来分辨的细胞群体。
ICS技术应用案例
1. 高分辨率区分、高纯度分选有丝分裂全周期内的细胞

传统流式只能检测到有丝分裂间期G1、G2、S期,但无法分辨更详细的阶段。研究团队使用ICS图像分选功能,根据mNG图像可视化染色质以及组蛋白H3丝氨酸10的磷酸化作为染色质浓缩的marker,检测细胞有丝分裂的动态周期变化,成功分离不同分裂阶段的HELA细胞。

从G2、分裂期每个阶段各选取100个细胞,形成数据集和分裂轨迹。通过数据集发现更多分裂阶段的差异特征,其中贡献最大的是图像参数中的H2B-mNG 信号的maximum intensity、radial moment、eccentricity,这些参数将分裂中期、后期和末期的细胞区分开来。

使用图像参数进行圈门,分选不同阶段共5000个细胞;通过共聚焦显微镜手动鉴定,发现ICS技术可以达到非常高的分选纯度:G2 interphase (96% purity), prometaphase(64%), metaphase (78%), anaphase (94%)。
2. 基于高灵敏度成像下的高通量基因组功能文库筛选

对基因组功能文库筛选,使用现有成像技术无法真正实现高通量。ICS技术的出现有望减少这类筛选项目的时间周期、成本及操作的复杂性。本研究中将ICS用于CRISPR文库筛选项目,高通量检测NF-kB激活后RelA蛋白的核易位。
NF-kB信号通路激活与肿瘤生长、发生密切相关,是常用的肿瘤药物研究靶点。NF-kB激活后,RelA由细胞膜转移至细胞核内,激活下游转录因子。团队使用单个gRNA敲除通路三个重要基因(IKBKA、IKBKG、MAP3K7),ICS成功检测到RelA无易位发生,证实了ICS的灵敏度。

接下来,使用gRNA混合文库靶向1068个基因,包括37个NF-kB通路的核心原件。加入通路激活因子TNFα,根据RelA-mNG/DRAQ5correlation parameter图像参数值的最低和最高5%分选细胞。通过ICS鉴定的靶点与以往对NF-kB通路中了解的重要基因保持一致。继续使用全基因组靶向的文库,共鉴定出169个靶点,除了 TRAF5, TAB1, NFKB1,与以往研究中发现这三个基因对于维持通路功能非必须的结论保持一致。全基因组筛选(100X coverage,3个gRNA/基因)在9个小时之内完成,远远高于目前的基于显微镜的筛选技术!

本文通讯作者Lars Steinmetz 、Eric Diebold表示:“ICS技术融合了光学、机械、生物医学、软件工程等多种科技,跨度十多年,是多学科联合研究的成果,旨在为研究人员提供更灵活、更优异的探索工具。期待未来看到科学界如何利用此技术来加速科学探索和疾病疗法的开发!”