Cell | 郑宁组等通过cryo-EM技术解析鼠源NaV1.5结构
心脏有节律的跳动是钠、钾、钙等多种离子通道的协调功能及精细调控完成的。心肌细胞的收缩起始于动作电位的产生,而其中跨膜的快速去极化则依赖于一个能引起钠离子快速内流的特殊电压门控钠离子通道,NaV1.5(Voltage-gated Sodium Channel 1.5)。作为心脏中最主要的钠离子通道, NaV1.5的突变或功能异常会引起心律不齐,威胁人类健康。NaV1.5也因此是临床上常用的一类抗心律不齐药物(Anti-arrhythmic Drug Class I)的直接靶点。
真核NaV通道通常是由一个大约250 kDa可以通透钠离子的大亚基和一到两个大约30 kDa小亚基组成的复合体。在哺乳动物中,9种NaV亚型(NaV1.1-1.9)组织特异性地表达于可兴奋细胞中。NaV1.1-3和NaV1.6主要表达在中枢神经系统细胞中,NaV1.7-9分布于周围神经系统中;NaV1.4表达于骨骼肌细胞中;而NaV1.5主要存在于心肌细胞中。清华大学颜宁教授从2017年开始先后发表了多个真核NaV高分辨率冷冻电镜(cryo-EM)结构,揭示了NaV通道高度的结构一致性【1-4】。鉴于NaV1.5对维持心脏有节律跳动发挥极其重要的作用,深度解析NaV1.5的结构与功能的关系仍然具有重大意义。比如,目前已知超过350个位于NaV1.5氨基酸点突变会导致例如Brugada Syndrome Type 1,Long-QT Type 3和Atrial Fibrillation Familial 10等多种心率不齐疾病。这些点突变的致病机理以及一类抗心律不齐药物如何和NaV1.5相互作用都是有待解决的关键问题。
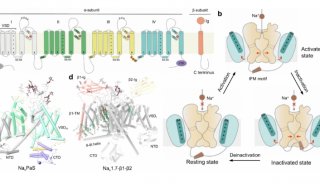
2019年12月19日,来自华盛顿大学William A. Catterall和郑宁课题组合作在Cell杂志上在线发表了题为Structure of the Cardiac Sodium Channel的研究论文,作者利用冷冻电镜cryo-EM技术,解析了鼠源NaV1.5以及NaV1.5结合抗心律不齐药物flecainide复合物的高分辨率结构。通过结合功能性研究,该论文不仅揭示了NaV1.5的特异结构与功能的关系,也为普遍理解NaV的激活,失活,及钠离子选择性提供了精细的结构分析及假说(图1)。


图1
NaV1.5的结构复杂性为蛋白表达和纯化带来挑战。作者通过荧光分子筛方法筛选截短体克隆以提高蛋白表达量和样品均一性。通过膜片钳验证了截短体具有和野生型相似的功能。最终解析了NaV1.5分辨率为3.5 Å的cryo-EM结构。由于超过70%的序列一致性,NaV1.5的整体结构和此前发表的人源NaV1.7等结构非常相似。然而,NaV1.5在一些细微处与其他Nav有所不同。比如,它在本该结合小亚基的界面演化出了不相容的氨基酸。这些看似微小的区别在NaV1.5的特异功能上或许会有重大影响。离子选择性一直是离子通道研究中的核心问题。作者发现对真核NaV离子选择性起最重要作用的氨基酸Lys1421将自己的侧链深入到离子选择性滤器(Selectivity Filter)中。带正电的Lys1421挡在同样带正电的钠离子的狭窄的通道上,那么钠离子是如何通过的呢?通过对NaV1.5结构深入分析,作者提出了一种“电荷转移模型”假设。通过与邻近氨基酸主链的羰基氧相互作用,Lys1421的正电荷或许被转移了。这样电中性的Lys1421就可以与钠离子形成配位并让其通过。
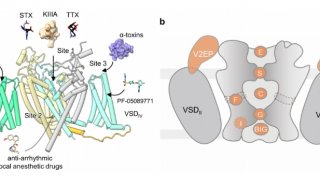
除了NaV1.5的自身结构,作者还解析了NaV1.5结合flecainide分辨率的3.24 Å的复合物结构。根据阻断NaV1.5通透钠离子流的强弱,一类抗心律不齐药物分为IA,IB和IC 3类。 Flecainide属于IC类,广泛应用于治疗例如房颤(Atrial Fibrillation)等心房心律不齐类疾病。在复合物结构中,flecainide结合于NaV1.5第二结构域(DII)和第三结构域(DIII)形成的开口处,其疏水的“身体”部分被三个苯丙氨酸像“三明治”一样夹住,而带电的哌啶环“头部”深入到通道中央空腔,并阻碍钠离子流的通过。
综上所述,通过解析心肌细胞钠离子通道NaV1.5和抗心律不齐药物的复合物的高分辨率结构,本文作者为理解抗心律不齐药物如何阻断NaV1.5以及新的抗心律不齐药物开发提供了结构基础。这是继2019年上半年William A. Catterall和郑宁课题组报道电压门控钠通道静息结构【5】后又一重要研究成果。
参考文献
1. Shen, H. et al. Structure of a eukaryotic voltage-gated sodium channelat near-atomic resolution. Science 355, eaal4326 (2017).
2. Pan, X. et al. Structure of the human voltage-gated sodium channel Nav1.4 in complex with β1. Science 362, eaau2486 (2018).
3. Shen, H. et al. Structures of human Nav1.7 channel in complex withauxiliary subunits and animal toxins. Science 363, aaw2493 (2019).
4. Pan, X. et al. Molecular basis for pore blockade of human Na+ channelNav1.2 by the μ-conotoxin KIIIA. Science, eaaw2999 (2019).
5. Goragot Wisedchaisri et al. Resting-State Structure and Gating Mechanismof a Voltage-Gated Sodium Channel. Cell 178, issue 4 (2019)
-
焦点事件
-
焦点事件

-
焦点事件

-
项目成果

-
项目成果
-
科技前沿

-
焦点事件

-
焦点事件

-
焦点事件