优卡迪、宜明细胞、波睿达CD30 CAR-T均获发明ZL授权
CAR-T疗法是肿瘤免疫疗法的三大马车之一,其中以CD19为靶点的CAR-T疗法已在血液癌症上取得了显着的成效。但淋巴瘤中,存在着不表达CD19的癌细胞,因此CD19 CAR-T对于这类淋巴瘤无能为力,这时就需要有新的靶点来弥补其缺陷,而针对CD30是目前治疗这类淋巴瘤最有希望的靶点之一,相关临床前研究已经证实了CD30 CAR-T治疗的可行性。以该靶点为开发的CAR-T将有望是解决其它淋巴瘤的有效方案。
CD30--被寄予厚望的淋巴瘤靶点
CD30是位于激活的淋巴细胞上的一种膜蛋白受体,是肿瘤坏死因子受体超家族的一员,CD30广泛表达于经典的霍奇金淋巴瘤,间变性大细胞淋巴瘤(ALCL),部分其他淋巴细胞瘤,包括皮肤T细胞淋巴瘤、弥漫性B细胞淋巴瘤细胞等表面。是当前淋巴瘤治疗十分有希望的靶点。
目前,针对CD30的单克隆抗体和抗体偶联药物已被广泛开发应用,并且取得了很高的应答率。同时也为CD30 CAR-T疗法的开发提供了相应的理论基础,但是目前对于复发性和难治性霍奇金淋巴瘤及间变大细胞淋巴瘤患者,抗体药物易产生耐药性,而CD30 CAR-T疗法成为其具有巨大应用前景的治疗方案。
早在今年5月4日,上海优卡迪生物医药科技有限公司CD30 CAR-T就率先获得国家知识产权局的ZL授权(一种靶向CD30的复制缺陷性重组慢病毒 CAR-T转基因载体及其构建方法和应用 ,ZL号:CN201610327646.X)。同时优卡迪生物也是首个拿到CD30 CAR-T发明ZL的企业。
据该发明称:其能显着提高细胞因子的分泌、CAR-T细胞的体外杀伤作用, 且临床治疗霍奇金淋巴瘤或非霍奇金淋巴瘤效果突出。
今年8月中旬,武汉波睿达生物科技有限公司收到国家知识产权局一项发明ZL授予ZL权的通知:《一种靶向表达CD30表面抗原的细胞的嵌合抗原受体(ZL号:201611246081.9)》被授予ZL权。
波睿达生物率先在全球开展CD30靶点的研发(药学研究、临床前动物实验),早在2015年,该公司在华中科技大学同济医学院附属同济医院开展该靶点的非注册临床研究,用于r/r霍奇金淋巴瘤及间变大细胞淋巴瘤的治疗,其首例病人无病生存期已超过3年9个月,已完成的临床前实验数据及已积累的非注册临床数据充分证实了该产品的安全性及有效性。
近期,该公司将以CD30为靶点向国家药品监督管理局药品审评中心(CDE)递交新药研究申请(IND),以促进该靶点注册临床试验的进行。该公司目前拥有30多项国内外CAR-TZL技术,搭建了质粒、慢病毒转导、CAR-T细胞生产等全产业平台,覆盖血液肿瘤、病毒感染性HIV、实体肿瘤等领域。
8月30日,宜明细胞生物科技有限公司公布,其获得国家知识产权局的抗CD30 CAR-T发明ZL(一种重组嵌合抗原受体基因及其应用,ZL号:2018107079050)授权。
贝勒医学院Ramos等人报道了CD30 CAR-T治疗9例复发性,难治性CD30+淋巴瘤(6例HL患者,1例ALK-ALCL患者,1例ALK+ALCL患者,1例DLBCL发展为HL患者)的试验结果,其中8位出现了输注后积极反应。
在这些患者中有7例之前接受过BV(一种靶向CD30的ADC药物)治疗,6位接受过ASCT后复发。这些患者未做淋巴细胞清除处理,输注了高剂量CD30 CAR-T的治疗后。该治疗显示出良好的耐受,未出现细胞毒性和细胞因子释放综合征的报告。
治疗后,8为患者出现了积极的疗效,2例患者完全缓解,其中1例ALK+ALCL患者进入完全缓解9个月后复发。另一位HL患者,截至发稿前,患者完全缓解已达2.5年。3位患者病情稳定,3位患者病情进展。1位接受CAR-T治疗的患者治疗前经过了自体细胞移植后进行抢救性化疗,随后出现完全缓解,再接受CAR-T治疗后,截至发稿完全缓解已达2年以上。
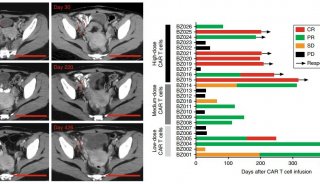
此外,Wang等人使用CD30 CAR-T治疗了18位难治性复发性CD30+淋巴瘤患者(17位HL,1位ALCL),18为患者中9位接受过自体干细胞移植(ASCT)治疗,5位接受过BV治疗。患者在淋巴细胞消耗疗法包括三种组合形式的淋巴细胞消耗疗法。
18位患者中,7位部分缓解,6位病情稳定,未见完全缓解,总缓解率39%,平均无进展生存率为6个月,4名患者截至发稿时仍有反应。5例患者接受了二次CAR-T输注,2次治疗后,3例维持部分缓解,1例维持稳定,1例首次输注病情稳定患者2次治疗后为部分缓解。在大多数接受治疗患者中,外周血中CAR-T细胞输注后3-9天达到峰值,在4-8周后降低到输注前水平,同时CD30+肿瘤细胞也急剧减少,穿刺检测中很少有CD30+肿瘤细胞,这就意外着CD30 CAR-T细胞对肿瘤细胞进行了有效杀伤。
结语
CD30 CAR-T低毒性和低脱靶效应使得其治疗淋巴瘤成为可能,临床研究已证明了CD30 CAR-T治疗CD30+淋巴瘤的有效性,但目前CD30 CAR-T的疗法发展还未像CD19 CAR-T那样成熟,相信随着其更多的临床试验的开展,该疗法也将逐步完善,同时也为淋巴瘤患者带来新的有效的治疗选择。
此外,相比较于大多集中于CD19、BCMA靶点而言,开拓靶向CD30的CAR-T或许是个不错的选择。
-
焦点事件
-
综述