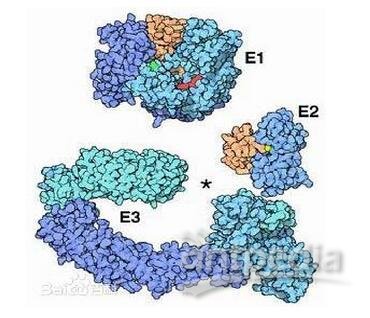
泛素化的过程
具体过程:泛素化修饰涉及泛素激活酶E1、泛素结合酶E2和泛素连接酶E3的一系列反应:首先在ATP(红色所示)供能的情况下酶E1(蛋白质编号1r4n)粘附在泛素分子尾部(淡黄色所示)的Cys残基上(绿色所示,注意在这个结构中,Cys突变为Ala)激活泛素,接着,E1将激活的泛素分子转移到E2酶上(蛋白质编号1fxt),随后,E2酶和一些种类不同的E3酶共同识别靶蛋白,对其进行泛素化修饰。根据E3与靶蛋白的相对比例可以将靶蛋白单泛素化修饰和多聚泛素化修饰。E3酶(蛋白质编号1ldk和1fqv)的外形就像一个夹子,靶蛋白连接在中间的空隙内(星号所示)。酶的左侧结构域决定靶蛋白的特异性识别,右侧结构域定位E2酶以转移泛素分子。蛋白质泛素化的结果是使得被标记的蛋白质被蛋白酶分解为较小的多肽、氨基酸以及可以重复使用的泛素。 泛素-蛋白酶体途径是先发现的,也是较普遍的一种内源蛋白降解方式。需要降解的蛋白先被泛素化修饰,然后被蛋白酶体降解。
不过后来又发现,并非所有泛素化修饰都会导致降解。有些泛素化会改变蛋白的活性,导致其他的生物效应,如DNA损伤修复,机体免疫应答等。 蛋白质泛素化作用是后翻译修饰的一种常见形式,该过程能够调节不同细胞途径中各式各样的蛋白质底物。通过一个三酶级联(E1-E2-E3),蛋白质的泛素连接由E3泛素连接酶催化,这种酶是cullin-RING复合体超级家族的最佳代表。
在从酵母到人类的各级生物中都保守的DDB1-CUL4-ROC1复合体是最近确定出的cullin-RING泛素连接酶,这种酶调节DNA的修复、DNA复制和转录,它能被病毒所破坏。
由于缺少一个规则的SKP1类cullin连接器和一种确定的底物召集结构域,目前人们还不清楚DDB1-CUL4-ROC1 E3复合体如何被装配起来以对各种蛋白质底物进行泛素化。
在这项新的研究中,DDB1-CUL4A-ROC1复合体被病毒劫持的形式进行了晶体结构分析。分析结果表明DDB1利用一个β-propeller结构域作为cullin骨架结合物,利用一种多变的、附着的独立双β-propeller折叠来进行底物的呈递。
通过对人类的DDB1和CUL4A复合体进行联系提纯,然后进行质谱分析,研究人员确定出了一种新颖的WD40-repeat蛋白家族,这类蛋白直接与DDB1的双propeller折叠结合并充当E3酶的底物募集模块。这些结构和蛋白质组学研究结果揭示出了cullin-RING E3复合体的一个新家族的装配和多功能型背后的结构机制和分子逻辑关系。 E1,E2,E3对底物的泛素化可形成几种不同的泛素化底物。有的底物蛋白只能被单泛素化,如H2B;有的底物蛋白有多个赖氨酸残基,在合适条件下会被多位点单泛素化;还有一些蛋白在单个赖氨酸位点会形成多聚泛素链,这种多聚泛素链可以根据连接泛素链的赖氨酸位点的不同可以分为单一、混合以及树枝状的结构。