分子探针红外之—固体表面酸性的测定
本期给大家普及一种可以分析不同强度Lewis酸的分子探针红外光谱技术——乙腈红外光谱。相较于吡啶红外光谱,乙腈红外光谱技术略显“小众”。不过,作为一种吸附质红外光谱技术,它凭借自身的特点在一定程度上弥补了吡啶红外光谱的不足。特别是在面对一些需要精细解析表面酸强度的材料时,乙腈红外能很好地展现出它的优势,可辅助我们开展催化剂活性中心的解析、反应动力学的研究以及理论计算的模型建立等工作。下面将结合我自己的测试经验和经典文献案例,给大家普及一下这种红外光谱技术。
从乙腈的碱性强度说起
我们在前两期聊了聊吡啶类探针分子。其实有很多具有碱性的、可气化的物质都能用来做探针分子表征材料的酸性质。不过,探针分子因碱强度不同,在应用方向和应用范围上会有所区别。探针分子的碱强度对酸性位点的识别可以类比我们在本科时学到的溶剂“拉平效应”和“区分效应”。
复习一下“拉平效应”和“区分效应”:“拉平效应”是指通过溶剂的作用,使不同强度的酸或碱显示同等强度的效应;“区分效应”对应地是指能区分酸碱强度的效应。比如,高氯酸在冰醋酸中酸强度是不同的,但以水为溶剂时,则难于区分他们的酸强度。这是由于水对质子有较大的亲和力,从而掩盖了这些酸给出质子能力的差异,而把这些酸不同的强度拉平了。
再回到碱性探针分子,如果探针分子的碱性较强,那它与不同强度的酸性位点都会有较强的相互作用,因此难以通过它来识别出这些酸性位点的酸强度差别。而如果是碱性较弱的探针分子,那么它就会因与酸性位点作用强度的不同,而“区分”出这些酸性位点的差别。
表1列出了几种常见的碱性红外探针分子的pKa,大家可以对他们有个碱性强度的概念。可以看到,我们最常用的吡啶的pKa是5.2,它的碱强度还是很强的,会“拉平”强酸与弱酸的差别,因此在表征一些固体材料的酸性时,很少采用它来指认每种Lewis酸的酸强度是多少,基本都是用它做总包Lewis酸和Brönsted酸的定性表征。我们在“固体表面酸性的测定(一)”中谈到,吡啶红外光谱表征的Lewis酸和Brönsted酸特征峰分别是1450 cm-1和1540 cm-1,文献中很少通过这两个特征峰的波数的变化判断材料的酸性强弱,就是这个道理。而乙腈的pKa仅有-10.4,是一种碱性非常弱的分子。面对强度不同的Lewis酸性位点,它的作用强度会存在差别。在红外光谱中,乙腈骨架中ν(C≡N)的振动波数可反映与乙腈相互作用的酸位点的强度,酸强度越强,ν(C≡N)的振动波数越高。表1. 几种常见的碱性探针分子的碱强度比较结果 [a]
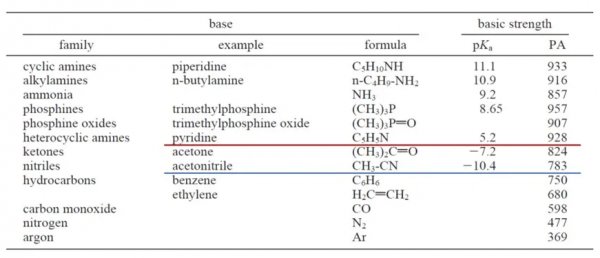
[a]Busca, G., Chemical Reviews, 2007, 107, 5366-410.举个例子乙腈红外光谱在分子筛的活性位解析中有较多应用。以催化大牛Avelino Corma教授的一篇经典工作(Journal of Catalysis, 2005, 234, 111–118)来感受乙腈红外光谱的妙用。Sn-Beta分子筛存在两种Lewis酸中心:骨架上半水化Sn中心(Partially hydrolysed framework tin center)和骨架上四配位Sn中心(fully framework coordinated tin center)。这两种酸中心在吡啶红外光谱的表征结果中区分不开,均在1450 cm-1处有特征吸收峰。然而采用乙腈红外光谱,可清楚地看到催化剂存在两组乙腈特征吸收峰,分别是2316 cm-1和2308 cm-1的乙腈ν(C≡N)的振动吸收峰(图1)。相较于气相乙腈的ν(C≡N)振动波数(2265 cm-1),两组峰分别向高波数移动了51 cm-1和43 cm-1。
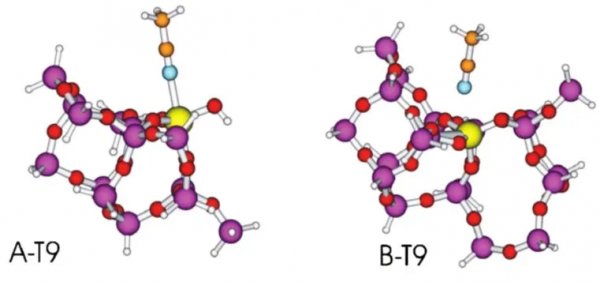
图1. 两种Sn-Beta (a) 1SnB 和 (b) 2SnB_c材料的氘代乙腈红外光谱随氘代乙腈的覆盖度的变化结果为了揭示2316 cm-1和2308 cm-1所代表的Lewis酸中心的精确结构,构建几种可能的Lewis酸中心结构,并采用多尺度模拟(ONIOM)和密度泛函理论(DFT)来计算乙腈与酸中心的相互作用前后已经C≡N振动的波数变化(Δν(C≡N))。通过与上述红外光谱实验数据对比,判断2316 cm-1和2308 cm-1所属的结构(图3)。其中,骨架上半水化Sn中心(Site A)与乙腈的相互作用后Δν(C≡N)更大,表明该种Lewis酸中心与乙腈的结合强度更高,Lewis酸性更强。
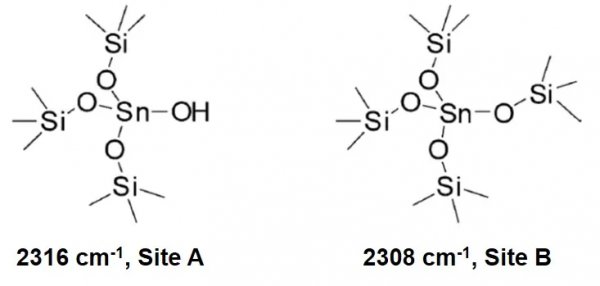
图2. 理论计算构建的Sn-Beta吸附乙腈的模型

图3. Sn-Beta分子筛的两种Lewis酸中心的结构示意图Sn-Beta分子筛可催化金刚烷酮氧化(图4)。为了解析其精确的催化氧化活性中心,对几种Sn-Beta分子筛做乙腈红外光谱表征,并计算它们2316 cm-1(Site A)和2308 cm-1(Site B)的峰强度(表2)。尝试将这几种分子筛这的两个特征峰以峰强度对金刚烷酮的氧化反应速率做关联(图5),发现2316 cm-1(Site A)与金刚烷酮的氧化反应速率呈良好的相关性,而2308 cm-1(Site B)与反应速率的相关性较差。由此判断,Sn-Beta分子筛的骨架上半水化Sn中心(Site A)应是催化氧化金刚烷酮的反应活性中心。

图4. Sn-Beta分子筛催化金刚烷酮氧化的反应式表2. 几种Sn-Beta分子筛的预处理条件和2316 cm-1和2308 cm-1处吸收峰的数据处理结果
图5. a) 骨架上半水化Sn中心(Site A)和b) 骨架上四配位Sn中心(Site B)的乙腈红外光谱吸收峰强度与金刚烷酮氧化反应速率的关联结果我们通过这篇经典案例,可以较快地掌握乙腈红外光谱解析固体材料的某一种Lewis酸性位点的方法。在一些文献中,将乙腈红外光谱做分峰,依据峰面积来计算每种Lewis酸性中心所占的百分比,这也是可以的。乙腈红外光谱的测试方法与吡啶红外光谱大致相同,具体可以翻看我们往期内容(固体表面酸性的测定(一))介绍的吡啶红外光谱测试步骤,在此不做赘述。欢迎各位在专栏给我留言,一起交流在阅读有关乙腈红外光谱的文献以及做乙腈红外光谱测试时遇到的问题和困惑。下一期,我们讲解另一种重要的分子探针红外光谱——CO吸附红外光谱在测定金属催化剂组成方面的应用。敬请期待




















