Nature子刊 | 四川大学赵瀛兰团队发现卵巢癌的重要调节新因子
聚(ADP-核糖)聚合酶抑制剂(PARPi)在由 BRCA1/2 和其他 DNA 修复途径成员突变引起的同源重组(HR)缺陷(HRD)卵巢癌(OC)中具有选择性活性。研究寻求在HR精通细胞中诱导HRD的分子靶向疗法,以诱导PARPi的合成致死作用,并扩展PARPi的效用。
2023年11月16日,四川大学赵瀛兰团队在Nature Communications 发表题为“Repression of LSD1 potentiates homologous recombination-proficient ovarian cancer to PARP inhibitors through down-regulation of BRCA1/2 and RAD51”的研究论文,该研究证明了赖氨酸特异性去甲基化酶1(LSD1)是 OC 的重要调节因子。重要的是,在体外和多个体内模型中,LSD1的基因缺失或药物抑制可诱导HRD,并使HR精通的OC细胞对PARPi敏感。
在机制上,抑制LSD1可直接损害BRCA1/2和RAD51的转录,这是HR所必需的三个基因,依赖于其经典的去甲基化酶功能。综上所述,该研究表明与LSD1抑制剂联合应用可以大大扩大PARPi在HR正常肿瘤患者中的效用,值得在人体临床试验中进行评估。

卵巢癌(OC)是全球死亡率最高的第二大常见妇科癌症。高级别浆液性OC亚型占OC 死亡的 70-80%,其 5 年总生存率低于 40%,且几十年来一直没有变化。虽然手术联合细胞毒性铂类药物化疗是OC患者的标准治疗,但大多数患者对铂类药物化疗产生耐药,导致复发和死亡。
大约50%的OC患者在同源重组(HR)DNA修复异常,最常见的原因是 BRCA1/2 突变,导致DNA双链断裂(DSB)的积累。HR缺乏(HRD)会产生一个漏洞,可以利用该漏洞通过合成致死的方式杀死癌细胞。这种方法的范例是使用聚(ADP-核糖)聚合酶(PARP)抑制剂(PARPi)治疗患有HRD的OC患者。对于HR修复功能异常的肿瘤,PARPi抑制PARP酶的活性,增加PARP-DNA复合物的形成,导致DNA损伤修复障碍,促进肿瘤细胞死亡。
尽管 PARPi 在临床上对 BRCA1/2 突变患者取得了显著成功,但多达50%的OC患者仅从这些药物中获得的有限益处。此外,对PARPi的获得性耐药是OC的一个主要问题,OC最初是HRD,但在PARPi治疗后通过多种机制获得HR熟练度,包括恢复 BRCA1/2 和 RAD51 功能的继发突变。因此,临床迫切需要确定新的分子靶点和潜在的联合治疗策略,以将PARPi效用扩展到HR熟练的OC。
迄今为止,尚无特异性靶向催化HR的蛋白质的直接抑制剂。有趣的是,为了将 PARP 抑制剂的使用范围扩大到更大范围的 HR精通OC 患者,最近的研究集中在使用可诱导 HRD 的药物的新联合策略上。靶向可操作的蛋白会干扰基因表达、核定位或HR蛋白的募集,最终导致 HR 的间接抑制,从而产生 PARPi 敏感性。重要的是,DNA 损伤修复途径与组蛋白修饰介导的染色质重塑密切相关,为 PARPi 与表观遗传因相结合提供了理论依据。在这方面,在临床前和早期临床试验中,选择性损害 OC 细胞中的 HR 已被证明可以使 HR 熟练的癌细胞对 PARPi 敏感。
赖氨酸特异性去甲基化酶1(LSD1)是一个有前途的靶标,可用于基于分子的抗癌治疗。LSD1可使单甲基化和二甲基化的组蛋白H3赖氨酸4 (H3K4me1/2)去甲基化,在与NURD或COREST的复合体中作为转录抑制因子,在与雄激素受体(AR)或雌激素受体(ER)的复合体中作为转录激活因子。此外,LSD1 去甲基化非组蛋白底物。在不同类型的恶性肿瘤中观察到 LSD1 的过表达,发挥促进肿瘤的活性。
一些研究强调了LSD1在肿瘤发生中的重要作用,并提供了抑制LSD1可能为癌症治疗提供治疗策略的证据。根据上述观察结果,包括IMG-7289、CC-90011和SP2577在内的LSD1抑制剂(LSD1i)目前正在进行临床研究,用于治疗AML、SCLC、前列腺癌和尤因肉瘤等癌症。在之前的文章中,已经开发了一种特异性LSD1抑制剂,命名为ZY0511,它在纳摩尔浓度30时抑制LSD1,在裸鼠体内对人结直肠癌和宫颈癌移植瘤表现出生长抑制,并增强人结直肠癌细胞对5-氟尿嘧啶的敏感性。
目前已有研究表明,LSD1 mRNA和蛋白在人OC组织中高表达,这与FIGO分期和淋巴转移相关。LSD1促进OC细胞的增殖、迁移和侵袭。敲低LSD1会损害OC细胞的增殖并介导顺铂敏感性。然而,上述研究仅处于探索LSD1在OC中的作用的初步阶段,LSD1在OC进展中的分子机制以及LSD1i在OC治疗中的潜力尚不清楚。此外,越来越多的研究表明LSD1与DNA损伤修复相关,这些研究表明LSD1可能是OC的潜在调节因子,并在DNA损伤应答中发挥重要作用。然而,LSD1在DNA损伤修复中的确切分子机制以及LSD1抑制是否使HR-精通的OC对PARPi敏感仍不清楚。
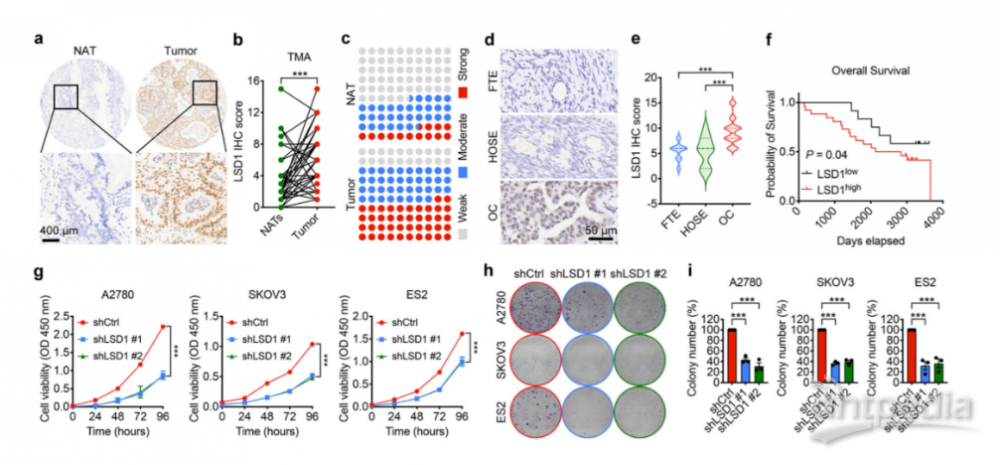
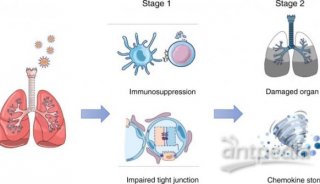
LSD1是OC的关键介质,促进OC的进展(图源自Nature Communications )
该研究探讨了LSD1在 OC DSB 修复中的作用和潜在机制,并讨论了LSD1定向治疗是否代表了 HR-精通的OC联合PARPi治疗的有前景的策略。在此报道了LSD1 敲低和药理学抑制在体外和体内抑制OC生长。LSD1 的抑制通过直接损害BRCA1/2和 RAD51 基因的表达来阻碍 HR 修复。重要的是,体外和多个体内模型中证明了抑制LSD1诱导了 HRD 并使 HR 精通的OC细胞对PARPi敏感。综上所述,研究结果揭示了LSD1在调节HR中的关键作用,并证明了LSD1i是一种提高PARPi治疗HR熟练度的效率和扩大效用的策略。