微流控芯片技术应对临床检验医学考验(二)
(三)病原微生物检测
病原微生物检测主要包括病原鉴定和药物敏感性判定两个方面。目前,临床微生物检测面临的最大问题就是检测周期过长。感染性疾病大多病情凶险,需要及时诊断和治疗,留给病原检测的时间窗口只有30分钟左右。然而,目前的病原微生物鉴定和药物敏感性判定的典型周期是2-3天,这显然难以满足临床需求。病原检测技术的限制所带来的结果是,一方面经验性诊断的准确性难于保证,另一方面抗生素滥用引发了严重的耐药问题。
微流控技术对于病原微生物鉴定的解决方案多是采用核酸检测策略,这在前面部分已经叙述。鉴于药物敏感性(Antimicrobial Susceptibility Testing, AST) 判定的实质是病原在药物暴露条件下的增殖情况判定,微流控技术采用的策略是:1.通过培养器体积的减小,实现检测信号的相对富集;2.使用更为精准的病原定量技术。这两种策略均可以通过缩短病原培养时间实现快速的药物敏感性判定。遵循这种理念,作者课题组发展了一种基于液滴阵列微流控芯片的数字化抗生素敏感性测试方法[11]。我们的设想是借助于数字化分析的精准定量能力显著缩短细菌培养时间。细菌悬液与抗生素孵育后引入微流控芯片完成液滴发生和捕获,生成高密度微液滴阵列。通过对液滴阵列进行荧光扫描成像,检测每个液滴中的荧光信号并以此计算出细菌存活率(v)和阳性微液滴比例(p)。根据阳性微液滴比例,可以泊松分布算法推算出细菌密度,依据细菌密度变化可确定最小抑菌浓度(minimuminhibitory concentration, MIC)。我们的初步研究结果显示应用该方法仅需30 min抗生素暴露时间即可判定大肠杆菌的抗生素敏感性。
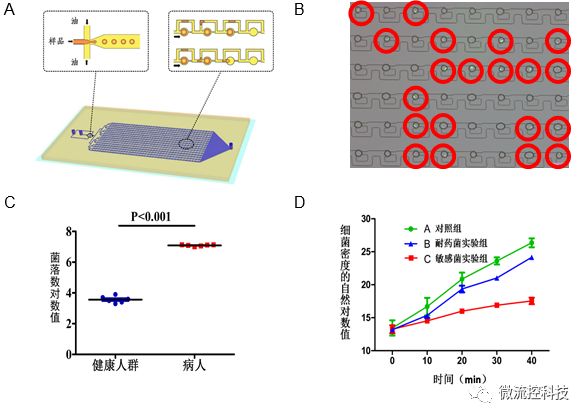
图3A.液滴微流控芯片原理设计图结构包含上游的液滴生成区和下游的液滴捕获区;B.利用液滴荧光成像分辨细菌阳性和阴性液滴;C.液滴数字化分析显示健康人和尿路感染病人尿液细菌计数差别;D.液滴数字化分析显示敏感和耐药细菌对于抗生素的反应。
(四)细胞水平抗肿瘤药物敏感性测试
体外抗肿瘤药物敏感性测试是指导抗肿瘤药物合理使用的有效手段。虽然基因检测可以用来预测抗肿瘤药物敏感性,然而该方法存在一定的不确定性。相比之下,细胞水平的药物测试仍然是判定抗肿瘤药物敏感性更为直接可靠的手段。然而,由于细胞水平抗肿瘤药物敏感性测试存在体内外实验结果差异大、测试通量有限以及操作难于标准化等问题,至今在临床难以推广。
针对该问题,课题组开发了一套微流控肿瘤微阵列药物测试系统[12],其核心是一种复合式结构开放式微流控芯片。芯片顶层是开放式储液池,底层是细胞培养池阵列,中间层是纳米孔薄膜。利用纳米孔薄膜不允许液体通过只允许跨膜扩散的特性,将其用做止流阀实现细胞悬液自动分配以及用作扩散屏障仿真血管内皮层。配合移液工作站,这种微流控芯片可以实现药物筛选所包含的长期细胞培养、换液、多药物处理以及细胞存活检测等一系列操作步骤。
研究利用自行设计加工的1010微流控细胞培养阵列芯片,实现了细胞培养阵列构建、长期细胞培养、换液、多药物处理以及细胞存活检测等一系列功能。乳腺癌细胞在持续培养3天后增殖形成了类组织结构。利用开放式微流控组织阵列芯片实现了3因素3水平正交药物组合测试,并依据细胞存活率检测结果筛选出最佳的抗乳腺癌药物组合。研究结果显示这种明微流控芯片能够以高度仿真的组织实现多药组合测试,因而有潜力成为指导肿瘤个体化精准治疗的有力工具。
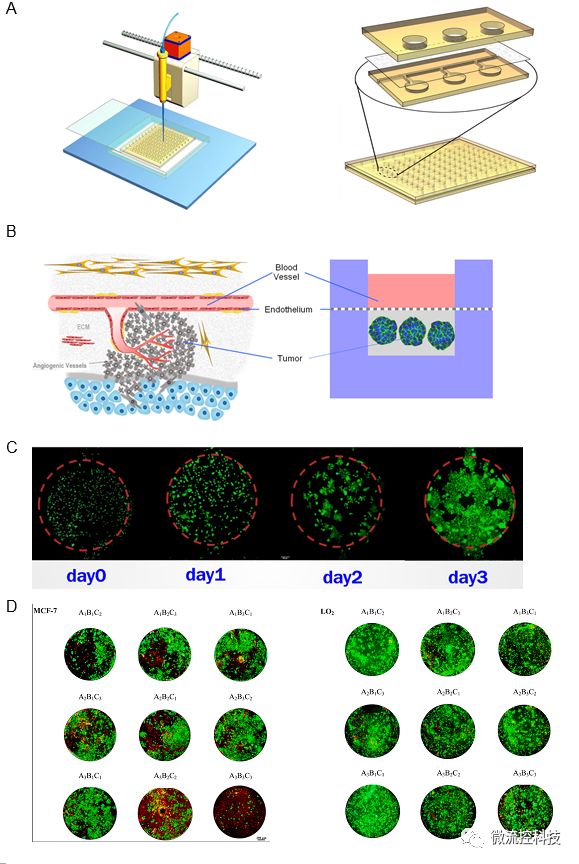
图4A.微流控肿瘤微阵列药物测试系统包含一种复合式结构开放式微流控芯片以及移液工作站;B.微流控芯片上肿瘤微环境重建的示意图。3D培养肿瘤细胞模拟肿瘤实质,水凝胶模拟支持和滋养肿瘤细胞的肿瘤基质,纳米孔薄膜扩散屏障模拟血管内皮层;C.微流控芯片上连续三天内MCF-7乳腺癌细胞增殖情况。(Calcein-AM / EthD-1染色,比例尺:200 μm);D.抗肿瘤药物正交组合测试结果。药物测试包括LO2肝细胞和MCF-7乳腺癌细胞对A.阿霉素,B.紫杉醇和C.顺铂的3因素3水平正交组合药物的反应。
通过上述应用实例,我们将微流控体外诊断技术的优势概括为:1.应用场景的拓展;2.分析效率的提高;3.分析时间的缩短以及4.检测精度的提升。由此可见,微流控芯片是极具优势的体外诊断技术平台。
四、微流控体外诊断技术的机遇与挑战
目前,我国正处于巨大的社会变革过程,一方面国力的增强和科技的进步促进了新技术的发展和推广,另一方面新形势对于体外诊断行业提出了新的要求。体外诊断作为一个高附加值行业,将会在未来相当长的阶段中快速发展,甚至成为国家的支柱产业。随着医疗改革的推进,三级医疗体系将逐渐完善,随之而来的是医疗资源由集中转变变为分散模式。公立医院的改革以及第三方检验机构的兴起,势必会对体外诊断技术提出更高的要求。在这种形势下,微流控技术将会对体外诊断行业的发展提供一个有利的契机。
现实中的微流控技术产业进程仍然是步履艰难。从技术角度来看,微流控体外诊断产品开发涉及多个学科领域,包括医学、生物、化学和工程等。任何一个企业,想要建立这样一个规模的研发队伍都绝非易事。作为微流控系统的核心,微流控芯片的设计、材料选择、表面处理、芯片加工乃至包装保存,都具有一定技术难度。因此,微流控产品的研发难度远远高于传统体外诊断产品。从产业环境角度来看,研究、生产和应用单位的脱节,高端加工技术的欠缺都增加了微流控产品开发的难度。此外,近期实体经济的低迷也导至企业对于这种高技术含量产品研发信心不足。对于微流控体外诊断产品开发,我们认为以下几个方面需要关注:首先是明确的市场定位,相比较传统技术,微流控产品必须在某个应用领域或应用场景下具有突出的优势;其次是前期研究基础。由于微流控产品研发技术门槛较高,缺少扎实的研究基础会增加开发进程的不确定性;再者就是尽量规避技术制约。由于各种条件限制,某些类型芯片可能在一定阶段内不具备量产可行性。因此,我们对于微流控诊断产品开发的建议是:1. 选择恰当的应用对象;2.整合研发资源;3. 开拓创造性的产学研合作模式。
五、结语
总体看来,微流控体外诊断技术的发展前途是光明的,道路是曲折的。无论如何,我们坚信微流控技术是新形势下应对临床检验医学挑战的有力工具,该技术势必会对临床检验能力的提升起到巨大的推动作用。
参考文献:
[1]. 方肇伦,微流控分析芯片发展与展望. 大学化学, 2001,02:1-6.
[2]. 林炳承, 微流控芯片实验室及其功能化. 中国药科大学学报,2003. 34: 第1-6页.
[3]. Whitesides,G.M., The origins and the future of microfluidics. Nature, 2006. 442: 368-373.
[4]. 林炳承, 功能型微流控芯片实验室的高通量和规模集成. 高等学校化学学报, 2004. 25: 121-123.
[5]. Haeberle,S. and R. Zengerle, Microfluidic platforms for lab-on-a-chip applications. Lab Chip, 2007. 7: 1094-1110.
[6]. 林炳承, 微流控芯片的研究及产业化. 分析化学,2016. 44: 491-499.
[7]. 林炳承,秦建华, 微流控芯片实验室及其应用出口:疾病诊断和药物筛选, 第四届全国微全分析系统学术会议,2007: 大连. 6-7.
[8]. Schulte,T.H., R.L. Bardell and B.H. Weigl, Microfluidic technologies in clinicaldiagnostics[J]. Clin Chim Acta, 2002. 321: 1-10.
[9]. Yager,P., et al., Microfluidic diagnostic technologies for global public health[J]. Nature, 2006. 442: 412-418.
[10]. Shu, BW, et al. Active droplet-array (ADA)microfluidics enables multiplexed complex bioassays for point of care testing. Chem. Commun., 2018. 54:2232-2235.
[11]. 梁广铁,杜燕,舒博文,等. 液滴阵列微流控芯片上的数字化抗生素敏感性测试.// 中国化学会,沈阳,东北大学,2017,第十一届全国微全分析系统学术会议,沈阳:2017:1-1.
[12]. Lin D, et al. Orthogonal screening of anticancerdrugs using an open-access microfluidic tissue array system. Anal Chem. 2017; 89(22):11976-11984.











