Nature Nanotech.:纳米颗粒出奇招,撩了抗原杀肿瘤
近年来,免疫治疗已经成为了最有效的癌症治疗方法之一,例如基于抗体的免疫检验点抑制剂(如CTLA-4抑制剂、PD-1抑制剂等)已经能够显著提高部分癌症病人的生存期(如黑色素瘤、非小细胞肺癌等)。但是,目前免疫疗法也存在着响应率低、疗效持续时间不长等缺点。临床研究表明将免疫疗法与放疗结合可以提高抗癌疗效,原因在于放疗不仅可以通过射线损伤肿瘤细胞DNA,还可以激活机体免疫系统。不少研究表明放疗具有“远端效应”——对局部肿瘤进行放疗可以促进远端转移灶的消退,这对病人中长期响应很重要。目前认为这种远端效应由免疫系统介导产生:放疗杀死的肿瘤细胞会释放促炎性细胞因子和肿瘤特异性抗原,从而促进免疫细胞吞噬并呈递抗原,诱导肿瘤特异性免疫反应。因此,放疗免疫联合疗法可以对肿瘤进行多重打击,达到“1+1>2”的效果。尽管如此,我们仍然不得不面对肿瘤治疗成功率较低的窘境,那么有没有可能进一步增强这种组合的疗效呢?
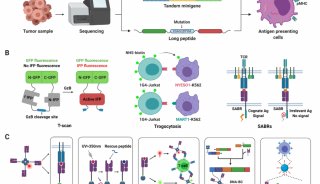
近日一篇发表在Nature Nanotechnology 上的文章就提供了一种增强放疗免疫联合疗法功效的新策略,利用简单的纳米颗粒出其不意打出奇招。由于研究表明纳米颗粒可以吸附体液中的蛋白质,同时抗原呈递细胞(APCs)对纳米颗粒的摄取能力远远超过蛋白质,因此北卡罗来纳大学教堂山分校Andrew Z. Wang教授带领的研究团队制备出了可以抓住抗原的纳米颗粒(AC-NPs)以吸附肿瘤来源的特异性抗原(TDPAs)并被APCs吞噬,增强机体抗癌免疫反应,从而成功增强了放疗的远端效应及放疗免疫联合疗法的抗癌疗效。
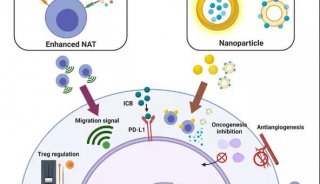
图1. AC-NPs吸附肿瘤抗原、被APCs吞噬、增强抗肿瘤免疫反应,最终增强放疗远端效应及免疫治疗抗癌疗效。图片来源:Nature Nanotech.
作者利用聚乳酸-羟基乙酸共聚物(PLGA)为内核制备了纳米颗粒(PLGA AC-NPs),通过不同修饰方法得到了表面为氨基(NH2 AC-NPs)、DOTAP(DOTAP AC-NPs)、马来酰亚胺(Mal AC-NPs)、聚乙二醇单甲醚(mPEG-AC-NPs)的纳米颗粒,它们分别可以通过疏水-疏水相互作用、静电相互作用、静电相互作用、硫酯键等抓住肿瘤来源的特异性抗原,而mPEG-AC-NPs与蛋白质的作用相对较弱。当这些AC-NPs与放射致死的B16F10癌细胞裂解液共同孵育时,纳米颗粒的表面电势和粒径都发生了变化,表明纳米颗粒均吸附蛋白。通过定量分析发现不同的纳米颗粒吸附的蛋白质的总量、种类和相对丰度均不同,其中PLGA AC-NPs和DOTAP AC-NPs吸附的蛋白种类最多,质谱分析发现除mPEG-AC-NPs之外,其他AC-NPs都吸附较多的肿瘤抗原和促炎性细胞因子(主要为损伤相关的分子模式蛋白,DAMPs,可以增强免疫反应)。这些数据表明这些AC-NPs确实可以吸附放疗杀死的癌细胞释放的特异性抗原。
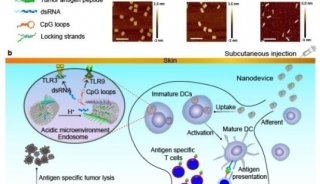
图2. 不同AC-NPs吸附的蛋白数量、种类及丰度不同。图片来源:Nature Nanotech.
为了验证这种AC-NPs是否可以增强放疗的远端效应以及放疗与免疫疗法的联合疗效,作者对正在接受抗PD-1(αPD-1)疗法治疗、患B16F10黑色素瘤的小鼠原发灶进行放疗治疗(转移灶不接受放疗治疗),随后在原发灶注射PBS或者AC-NPs,再通过测量转移灶肿瘤的生长速度来检测不同AC-NPs对肿瘤治疗疗效的影响。结果发现PLGA AC-NPs和Mal AC-NPs对疗效的增强效果最明显,治疗效果最好,显著延长了小鼠生存期,其中放疗+αPD-1+PLGA AC-NPs的完全响应率达到20%,并且3个月后再给这些小鼠注射肿瘤细胞,它们也不会长出肿瘤。此外,如果清除小鼠的CD8+T细胞则会完全消除AC-NPs的疗效增强作用。这表明AC-NPs确实可以增强放疗远端效应及免疫治疗疗效。
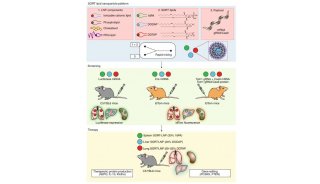
图3. 不同AC-NPs提高免疫疗法及放疗治疗B16-F10肿瘤模型的疗效。图片来源:Nature Nanotech.
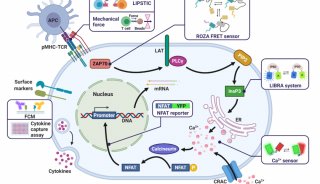
随后,作者对AC-NPs增强放疗远端效应和免疫疗法抗癌疗效的机制进行了研究,他们采用罗丹明标记了AC-NPs,瘤内注射后分析了AC-NPs在淋巴结中各APCs(DCs、巨噬细胞、B细胞)的分布情况,他们发现AC-NPs可以在注射后16小时富集到肿瘤相关引流淋巴结(TDLNs)中,其中PLGA AC-NPs和Mal AC-NPs在APCs中的富集速度最快,同时放疗可以增强APCs对AC-NPs的摄取。进一步分析发现AC-NPs不仅可以促进T细胞浸润到转移灶中,还可以降低肿瘤组织中免疫抑制性T细胞的数量和比例。此外,AC-NPs还可以增强小鼠脾细胞产生干扰素γ的能力,其中PLGA AC-NPs和Mal AC-NPs处理过的小鼠的脾脏细胞中产生干扰素γ的T细胞比例最高。这意味着放疗后注射AC-NPs不仅可以促进肿瘤免疫微环境的改变,同时还可以产生系统性的抗癌免疫反应,通过增加肿瘤抗原特异性的抗癌T细胞的数量和质量,最终增强放疗免疫联合疗法的疗效。
图4. 不同AC-NPs促进APCs抗原呈递和免疫系统激活。图片来源:Nature Nanotech.
最后,为了进一步确认是AC-NPs增强了放疗的远端效应和免疫治疗疗效,作者采用这些不同的AC-NPs直接与TDPAs孵育,然后注射到患肿瘤并接受αPD-1治疗的小鼠皮下。结果发现注射吸附TDPAs的PLGA AC-NPs和Mal AC-NPs可以显著减缓肿瘤的生长,并显著延长小鼠生存期,而清除CD8+T细胞则会消除这些增强效应。这也就进一步证明这些可以吸附肿瘤抗原的纳米颗粒确实可以通过增强肿瘤特异性免疫反应而增强免疫治疗的疗效。
图5. 吸附TDPAs的AC-NPs可以增强αPD-1抗癌疗效。图片来源:Nature Nanotech.
本研究除了奇思妙想的创意,也是纳米颗粒蛋白冠、免疫治疗、放射治疗研究发展整合的必然结果。尽管尚属非常初期的概念验证,但却解决了肿瘤个性化免疫治疗的难题——肿瘤异质性导致每个病人的肿瘤抗原都有差别,而针对每个病人的肿瘤抗原进行治疗实在不是明智之举。本文应用的方法“就地取材”,直接利用纳米颗粒原位吸附肿瘤抗原以激活免疫系统,增强免疫疗效,巧妙避开肿瘤抗原差异性的难题,思路不可谓不巧妙!如果这一策略能在未来顺利地进行临床转化,人类对抗癌症就会又多出一柄利器!