有望利用ABE治疗单基因突变肝病患者
可编程CRISPR-Cas核酸酶通过在目标位置使双链DNA断裂来实现基因组编辑,但在有丝分裂后的细胞中十分低效。而碱基编辑器是最近开发的基因组工程工具,能在转换率低的组织中进行精确有效的编辑。
对于碱基编辑的临床应用,其主要的局限性在于产生潜在的非靶突变。非靶突变可以是单导向RNA (sgRNA)依赖的或sgRNA独立的,并受碱基编辑器表达水平和持续时间的影响。此外,体内碱基编辑尚未在大型动物模型中得到证实。
2021年5月19日,瑞士苏黎世联邦理工学院Gerald Schwank与加拿大Acuitas治疗公司Sean C. Semple团队合作,在国际学术期刊《自然-生物技术》杂志上在线发表了题为“In vivo adenine base editing of PCSK9 in macaques reduces LDL cholesterol levels”的文章,研究表明在猕猴体内对PCSK9进行腺嘌呤碱基编辑可降低低密度脂蛋白(LDL)水平。
DOI: 10.1038/s41587-021-00933-4
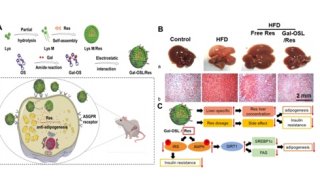
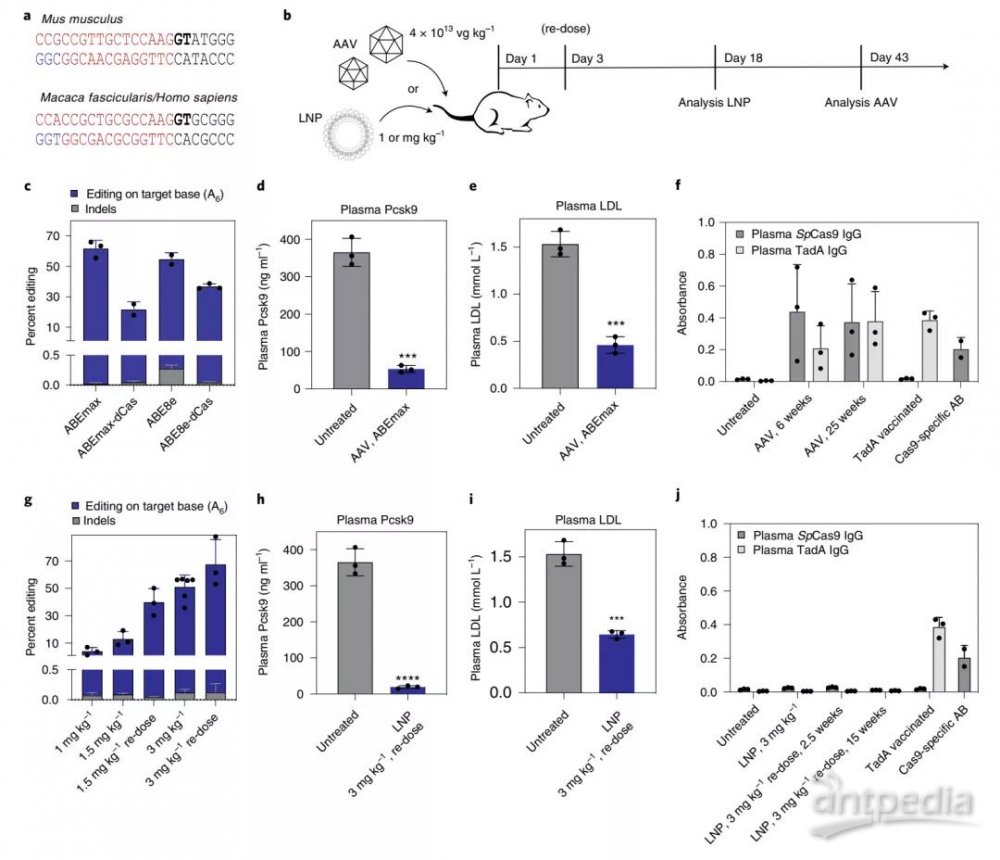
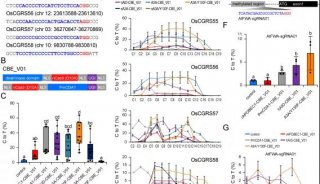
PCSK9,主要在肝脏中表达,是LDL受体的负调节因子。研究人员用腺嘌呤碱基编辑(ABE)在小鼠Hepa细胞中定位了几个典型的PkcK9剪接位点来试图降解PkcK9的mRNA和蛋白质,最后确定了sgRNA_mP01和sgRNA_hP01分别用于小鼠和食蟹猴的体内实验。并且通过将不同的SpCas9-TadA构建体与sgRNA_mP01一起导入小鼠的肝脏,实验表明其血浆Pcsk9水平以及血浆LDL水平显著降低。并且在小鼠中诱导了高达67%的编辑(平均61%),在猕猴中诱导了高达34%的编辑(平均26%)。小鼠血浆PCSK9和LDL水平分别稳定降低95%和58%,猕猴稳定降低32%和14%。
小鼠肝脏中Pcsk9基因的体内腺嘌呤碱基编辑
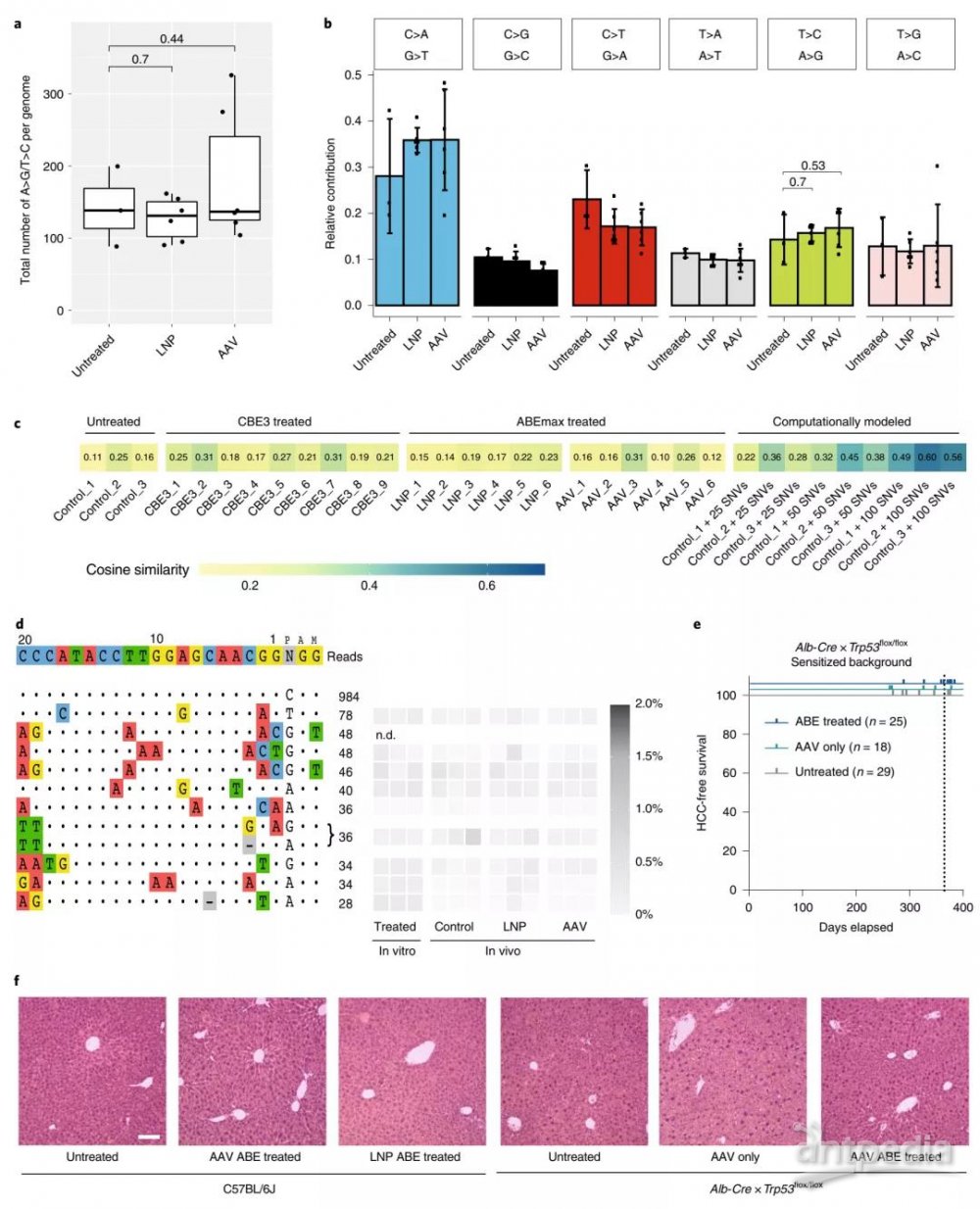
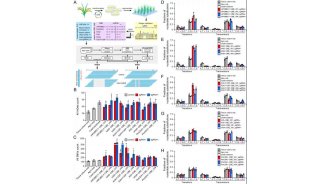
随后,研究人员探究了长期ABE表达产生的非靶突变,在分子水平评估了在DNA和RNA中的非靶突变。实验表明ABE mRNA的非靶效应是暂时的,在注射后第17天就不再检测到,而在基因组DNA中也未发现靶外突变。这些结果表明腺嘌呤碱基在体内编辑是有效和安全的,并有可能用于遗传性肝病患者的治疗目的。
Pcsk9的体内腺嘌呤碱基编辑不会在DNA中诱导大量的非靶突变
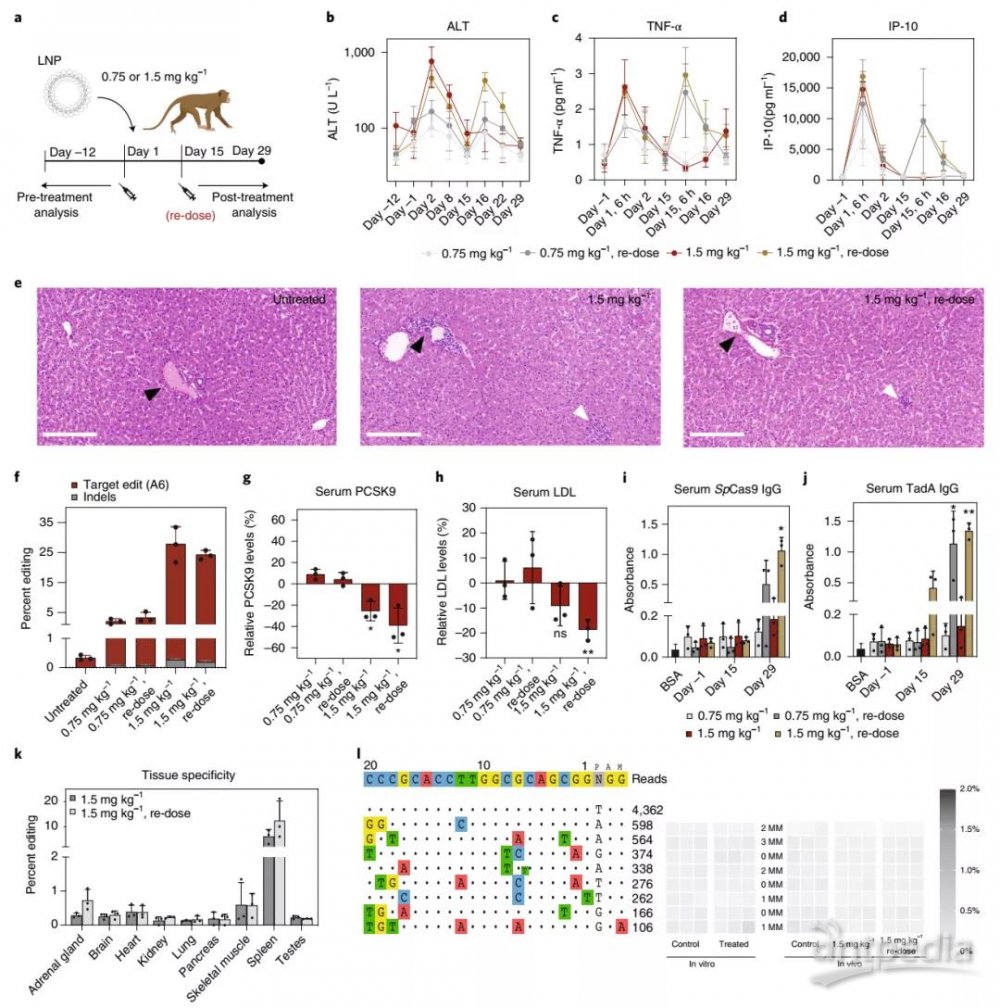
最后,作者为了进一步评估ABE在临床相关大动物模型中的可行性,在成年食蟹猴(食蟹猴)中编辑了PCSK9。实验表明,猕猴的ABE可抑制PCSK9从而降低血液LDL。而且与小鼠实验不同的是猕猴中观察到SpCas9和TadA的特异性IgG抗体,说明产生了对ABE的体液免疫反应,这可能也是猕猴中的再给药没有增加编辑的原因。
猕猴肝脏中PCSK9基因座的体内腺嘌呤碱基编辑
总之,本片文章研究了小鼠和食蟹猴肝脏中ABEs降低血液低密度脂蛋白(LDL)水平的有效性和安全性。利用脂质纳米颗粒实现ABE编码基因和靶向PCSK9(LDL的负调节因子)单向导RNA的递送,这在小鼠中可实现高达67%的碱基编辑(平均61%)水平,在猕猴中也可实现高达34%的编辑(平均 26%)效率。
血浆PCSK9和LDL的含量在小鼠中分别稳定降低了95%和58%,在猕猴中分别降低了32%和14%。ABE mRNA可被迅速清除,并且在基因组DNA中未发现脱靶突变。对猕猴进行重新给药并未增加编辑,这可能是由于治疗后对ABE产生的体液免疫反应所致。这些发现都为进一步利用ABE治疗单基因突变肝病患者提供了支持。
-
科技前沿
-
项目成果
-
项目成果
-
项目成果
-
项目成果