脂肪细胞信号通路研究
糖尿病人明明血糖很高,却还是容易感到饥饿;肥胖的人,不一定比更瘦的人提前感到饱腹。这说明,饱和饿并不完全受体内储存的能量影响。为了帮助减肥或增肥人群控制体内脂肪含量,韩国高级科学技术研究所的Walton Jones博士和他的同事,在分子水平向我们解释了,脂肪细胞如何指挥大脑感受“饱”。他们的文章发表在了3月28的PLOB Biology。
脂肪是动物体内主要的长期能量储存分子,脂肪水平的控制是生存的关键。在哺乳动物中,我们知道“瘦素”能够诱导机体消除脂肪行为,但是到目前为止,这其中的分子信号传导仍然是未解之谜。
比如,我们虽然知道肚子上的脂肪细胞会跟身体另一边的大脑说:“我饱了,请告诉机体不要再吃了。”但我们却并不知道脂肪细胞通过什么来“千里传音”,以及为什么有些脂肪细胞很快就发出了饱的信号,有些脂肪细胞却迟迟没有响应?
Walton Jones课题组首次发现了一个脂肪细胞的“通讯”分子。
果蝇是很好的信号通路研究模型。人类的很多摄食相关机制和基因都能够在果蝇中找到对应的表型和基因。于是研究人员利用果蝇动物模型,开始寻找脂肪细胞抑制大脑摄食的分子信号。
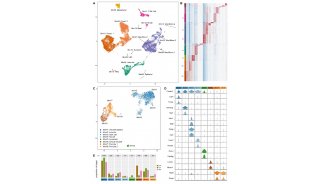
研究人员首先将目光聚焦在microRNA(miRNA)上,因为它们能够抑制基因表达。他们检测了影响摄食行为的脂肪组织中过量表达的miRNA,然后再寻找这些miRNA的靶基因。
想了解Clontech MirTrap系统如何轻松捕获microRNA的靶标请填写联系方式
Jones和同事们找到了一个异常表达的miRNA,名叫miR-iab-4。它的靶基因叫purple,是一个肥胖基因。它们俩合作能让机体多摄入27%的食物。下调purple的表达能够增强进食行为,证明正常情况下这个基因应该是受抑制的。
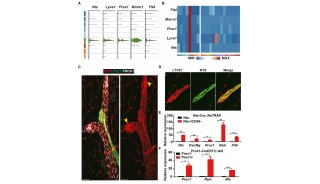
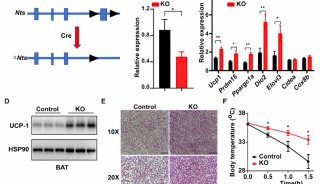
Purple编码两种脂肪体酶中的其中一种,PTP,它存在于脂肪体和大脑回路。在脂肪体酶的作用下能够被转化成BH4(一种辅酶因子),BH4能够帮助神经元生产NPF(一种摄食相关神经肽)。Jones课题组将脂肪体内的purple缺失后,神经元内的BH4下降,NPF减少,摄食行为受到了抑制。反过来,增加神经元内的BH4,NPF被释放,摄食量增多。
研究发现,低卡路里的饮食结构会抑制脂肪体内控制BH4产量的酶类表达,从而导致摄食增加。
这项研究的结果表明,BH4是抑制苍蝇食欲的关键因素。而脂肪体释放的PTP则是脂肪细胞向大脑传递“吃饱了”的分子信号。
虽然,目前的信号传导结论只适用于果蝇,但是这种食欲抑制机制迟早会在人类身上得到印证,倘若这个信号通路可以被安全地调控,将使很多人受益。