著名学者朱健康院士Cell Research发表表观遗传学研究成果
生物通报道:转座子通常是通过表观遗传学机制(包括DNA甲基化)保持沉默的。12月9日,在《Cell Research》杂志上发表的一项研究中,来自中科院上海生命科学研究院、美国普渡大学以及中科院遗传与发育生物学研究所的研究人员,在拟南芥中将一对Harbinger转座子衍生蛋白(HDPs)——HDP1和HDP2,确定为抗沉默因子。hdp1和hdp2突变体表现出转基因和一些转座子的沉默增强。著名学者朱健康院士是本文通讯作者。
转座因子(TEs)是移动的、重复的遗传因子,在真核生物基因组中占很大一部分。转座子由于对宿主基因组的有害影响,通常被视为“自私”DNA或“寄生”因子。然而,新的证据表明,TEs在基因功能的演变和调控中起着关键的作用。此外,越来越多的宿主基因,是从已被发现的转座子衍生或“驯化”而来。在宿主基因组中,这些基因的确定及其功能的阐明,对于理解转座子如何有助于寄主适应性,是非常有意义的。
在植物中,TEs通常是通过表观遗传学沉默机制调节的,包括DNA甲基化和组蛋白修饰。DNA甲基化在多个过程中起着重要的作用,包括基因组的稳定性、细胞对环境刺激的反应和器官的发育。DNA甲基化水平和模式是动态的,并由两个可逆反应确定:DNA甲基化和去甲基化。DNA甲基化可以通过被动或主动的途径、或两者的组合而发生。与被动的DNA去甲基化比较,特定的酶促反应对于活性DNA去甲基化是必需的。在拟南芥中,主动的DNA去甲基化是由一系列双功能的DNA糖基化酶/酶执行的,包括ROS1、DME、二甲醚2(DML2)和DML3。ROS1的功能缺失突变可引起DNA的超甲基化,并增强转基因和内源基因以及TEs的转录后基因沉默(TGS)。
然而,在植物和动物中,主动的去甲基化机制如何被招募到特定的基因组位点,我们还了解甚少。增加的DNA甲基化1(IDM1)——组蛋白乙酰转移酶,是一小部分ROS1介导的DNA去甲基化所必需的。最近,IDM1被证明与IDM2、IDM3和一个甲基DNA结合蛋白MBD7组成一个复合物。在这个IDM复合物中任何组件的突变,都会导致增强的转基因沉默和特定基因组区域(包括TEs)的 DNA超甲基化。MBD7可识别密集的甲基化CpG区域,并有助于IDM1到特定基因组位点的招募。然而,MBD7单独不能决定IDM1的靶标特异性,因为该复合物与具有很高DNA甲基化的所有基因组区域无关。因此,在IDM复合物中可能有其他组件,决定着该复合物的靶标特异性。
Harbinger转座子是DNA转座子,通常编码一个DDE转座酶和含有SANT/Myb/trihelix 结构域的DNA结合蛋白。Harbinger转座子驯化已在哺乳动物、果蝇和拟南芥有过报道,从而指出了它们的进化意义。然而,它们的生物学功能目前还不清楚。
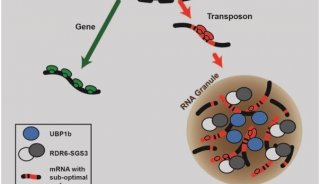
在这项研究中,研究人员使用正向遗传筛选,在拟南芥中确定了一对Harbinger转座子衍生的反沉默因子HDP2和HDP1。这两个基因的功能缺失突变,不仅能引发转基因和一些内源性TEs的沉默增强,而且也增加了DNA甲基化。类似于它们的Harbinger转座子相对物,HDP1在细胞核中与HDP2相互作用。该研究小组提供的证据表明,HDP2和HDP1是以前确定的IDM组蛋白乙酰转移酶复合物的新组件,该复合物还包括IDM1、IDM2、IDM3和MBD7。
这些研究结果表明,HDP1和HDP2是检测位点上IDM1组蛋白乙酰转移酶活性所必需的。此外,HDP2和MBD7共有大量的染色质关联的常见基因组区域。因此,这些数据表明, HDP1和HDP2构成来自Harbinger转座子的一个功能模块,已被招募以在宿主组蛋白乙酰转移酶复合物中发挥功能。HDP1和HDP2模块对于确定组蛋白乙酰转移酶复合物的靶向特异性以促进DNA去甲基化并防止重要的表观遗传沉默,是非常重要的。