标准化建设助力中药上市后再评价
近年来,有关中成药的安全性、有效性的疑虑不时见诸媒体,对现有中成药品种全面进行上市后再评价成为公众和制药企业的共同心声。6月6日,在由世界中医药学会联合会中药上市后再评价专业委员会主办的“第四届中药上市后再评价与药物警戒高级研讨会”上,与会专家和企业人员表示,药品进行上市后再评价是大趋势,企业目前高度重视,正在抓紧进行产品梳理、诊断和顶层设计。
本次会议审议并表决通过的《中药上市后安全性医院集中监测技术规范》、《中药上市后药物经济学评价技术规范》、《中药上市后安全性医院集中监测报告规范》3项技术规范,成为世界中联中药上市后再评价专业委员会标准。专家表示,我国尚未形成较为完善的药品上市后再评价体系,中药由于成分复合多样、中医治疗方案复杂多变等原因,更是缺乏上市后再评价的技术规范。世界中药学会联合会副主席兼秘书长李振吉认为,以上中药上市后再评价相关技术规范的制定切合3个方面的需求。第一个方面是企业需要,企业关心产品的良性发展,希望进行上市后再评价,这个过程需要有一个公认的、规范化的技术规范来引导。第二个方面是管理部门需要这样的规范,来评判一个药品再评价的过程是否科学,得出的结论是否有效。第三个方面是社会需要在科学合理的技术规范指导下进行再评价。
世界中医药学会联合会中药上市后再评价专业委员会秘书长、中国中医科学院研究员谢雁鸣表示,“结合我国中药上市后再评价本身的特点,建立我国中药上市后再评价相关技术规范,是大势所趋。”
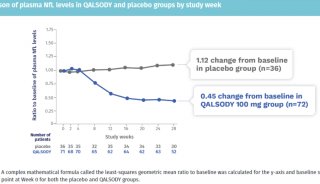
本次研讨会还公布了疏血通注射液等6个中药注射剂品种的上市后临床安全性监测结果。这一监测来源于2012年启动的“重大新药创制”国家科技重大专项“中药上市后再评价关键技术研究”(共10个中药注射剂品种参与监测),是目前中国最大规模的中药注射剂药物警戒计划项目,由中国工程院院士王永炎和谢雁鸣研究员担任总课题负责人。
据介绍,该监测的主要目的为获得中药注射剂的不良反应特征和不良反应发生率,指导临床合理用药,探索中药注射剂过敏反应的发生机制。目前10个中药注射剂品种已监测近30万例患者,最终确定6个品种不良反应发生特征及不良反应发生率,初步探索了中药注射剂过敏反应的发生机制。
谢雁鸣认为,包括“中药注射剂上市后临床安全性监测”项目在内的众多科技成果是技术规范形成的基础,换句话说,中医药标准建设工作的基础条件已经具备。但由于中医药标准建设工作尚处于初级阶段,难免存在不足,技术规范的制定方法和程序还需在今后进行的验证和修缮,进一步完善我国中药上市后再评价技术规范的制定体系,从而建立起符合中药上市后再评价的标准体系和评价模式,建立健全具有特色的中药上市后再评价制度。