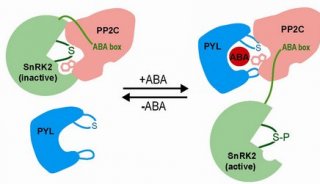
中国医学科学院JBC揭示信号调控新机制
来自中国医学科学院的研究人员在新研究中揭示了过氧化物酶体增殖物活化受体γ(PPARγ)调控KLF4表达的分子机制及其生物学功能,相关论文发表在《生物化学杂志》(JBC)上。
文章的通讯作者是中国医学科学院的刘芝华研究员,其主要研究方向为食管癌变的分子机理研究,目前主要研究S100家族成员及KLF4在肿瘤细胞分化调节及肿瘤侵袭转移中的作用及分子机制,转录调控及表观遗传学调控,在DNA损伤修复及放化疗敏感性中的作用等。
过氧化物酶增殖体激活受体(PPARs)属核激素受体超家族,共有三种亚型PPARα、PPARδ和PPARγ)。像这一超家族的其他成员一样,PPARs通过结合特异靶基因启动子区域的反应元件从而介导转录调控。在PPARs的三种亚型中,研究得最为广泛的是PPARγ,其与脂肪形成、免疫应答以及脂质和糖类代谢等多种生理过程密切相关。近年来 ,许多体外研 究发现 ,配体 活化的PPARγ可以抑制细胞周期、促进细胞分化、诱导细 胞凋 亡、抑制血管形成 ,从而具有抗肿瘤的生物效应。
KLF4(Kruppel—like factor4)是在1996年被发现的一种锌指转录因子,它是Spl/Kruppel样锌指转录因子家族的成员之一,该家族是机体内一类具有重要功能的蛋白质,它们参与调控细胞增殖、分化、胚胎发育等重要生命过程,并与肿瘤等多种疾病有关。近来有研究表明PPARγ可转录激活KLF4,但对于其调控机制仍不是很清楚。
在这篇文章中,ChIP和EMSA实验研究人员证实PPARγ是通过直接结合KLF4启动子的PPAR反应元件(PPRE)调控了KLF4的表达。 PPRE定位在KLF4 ATG密码子的上游-1657bp—— -1669bp,是TGZ转录激活诱导的KLF4表达的必要条件。此外,研究人员还发现稳定沉默KLF4可明显抑制PPARγ配体诱导的细胞G1/S期阻滞和抗增殖效应。
新研究从分子水平证明KLF4是一个直接受PPARγ蛋白调控的下游靶基因。PPARγ特异地通过KLF4启动子的PPRE反应元件而活化了 KLF4的转录表达。作为一个直接受PPARγ调控的下游靶基因,KLF4在由PPARγ介导的细胞周期抑制过程中但任着重要的角色。这些研究结果不仅完善了对PPARγ信号转导通路的认识,而且为PPARγ激动剂在肿瘤治疗中的应用提供新的思路和线索。
-
科技前沿
-
焦点事件