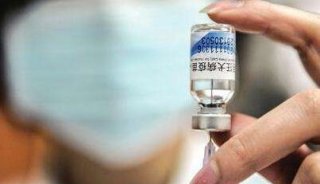
中国史上最严GMP将公布与国际接轨
GMP(药品生产质量管理规范)一直是关注焦点。几日前的国家食品药品监督管理局例行新闻发布会上,新闻发言人颜江瑛证实,“新版的GMP经过反复征求各方意见,包括听取了专家和药品生产企业以及监管人员等各方面的意见,经过了几次的修改,近期经批准后,我们会公布实施。”
有业内人士透露,新版GMP硬件部分参照欧盟有关标准,软件内容参照美国,堪称史上最严,如果实施到位,大多数中小企业将被灭掉,行业大洗牌在所难免。
强调与国际接轨
据介绍,1998年修订的GMP存在着内容原则化、条款化,指导性和可操作性不足,企业对软件标准重视不够,个别标准与政策的关联性存在差异等问题。颜江瑛在谈到GMP修订实施时表示,公布实施之前做了大量工作,包括新版GMP实施在哪些方面要解决老版GMP的不足,比如对软件的管理,对企业人员能力、资质管理制度和管理措施方面详尽提出了要求,而且加大这方面条款的制定,加强企业的软件管理。在新版GMP修订过程中,也根据我们国家经济社会发展水平和中国企业的特点,更多地要求新版的GMP使我们国家的药品生产企业在生产的质量方面和生产的质量管理方面能跟国际更好接轨。
这个与国际接轨体现在,新标准,结合我国实际情况形成的,涵盖了欧盟、美国FDA、WHO对GMP的基本要求,丽珠医药集团副总裁陶德胜向记者介绍,其中硬件内容参照欧盟,软件参照美国,其严格程度在世界上看都处前列。
违规记录操作难度大增
深圳康泰生物制品股份有限公司有关人员介绍,新修订的GMP细化了软件要求,注重软件水平的提高,强化了GMP与药品注册和上市后监管的联系,对药物生产实施更严格、更细化地管理。
新版GMP采用基本要求加附录的框架,涉及基本要求以及无菌药品、中药制剂、原料药、生物制品和血液制品五个附录。原98版GMP中的非无菌药品附录要求合并到基本要求中,中药饮片、放射性药品、医用气体等附录继续使用,暂不修订,与新版GMP不适应的则依从新版。如此下来,供企业执行的药品GMP将有1个基本要求、5个新附录和3个旧附录。
新标对主要文件(如质量标准、生产工艺规程、批生产和批包装记录等)分门别类具体提出了编写的要求,大大增加了违规记录、不规范记录的操作难度。吸纳了国际GMP先进标准,增加了诸如质量风险管理、供应商的审计和批准、变更控制、偏差处理等章节,以期强化国内企业对于相关环节的控制和管理等。
1/3企业受冲击明显
其实原98版GMP并非不严格,有企业负责人表示,坦率说根本问题主要是执行未能真正到位,腐败滋生,审批混乱,以致时任国家药监局局长的郑筱萸连命也给搭上了。陶德胜也告诉记者,新GMP更加严格,如果能执行到位,将有力促进洗牌整合,提升行业集中度。
目前国内有大约4000-5000家医药企业,这其中或将有1/3的企业在新GMP执行中被淘汰。还有媒体报道,国家药监局药品安全监管司官员有言论称,通过GMP将砍掉500家左右,虽然公开的说法是500家,但药监局会有更多的预期,可能关停规模达到上一轮的水平。基础好的企业反应当然不强烈,但对大部分中小企业来说,冲击很大。
-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件