免疫治疗里程碑!真实世界数据为TMB背书 治疗获益率80.7%
免疫治疗火不火?火。
免疫治疗怎么用?现在官方认定的PD-L1似乎并不总是靠谱,NCCN则“钦点”了肿瘤突变负荷(TMB)作为预测免疫治疗效果的生物标志物。
这下该没问题了吧,岂知又有人问,这都是基于临床试验数据得出的结论,入组条件控制得那么好,谁知道真上了临床能不能行?
好,要真实世界数据是吧,求锤得锤,如你所愿。
本周JAMA发表了一项最新研究[1],结合真实世界患者的电子病历(EHR)和Foundation Medicince的全面基因组测序分析(CGP)数据得出结论,以20 mutations/Mb为界,高TMB晚期非小细胞肺癌患者经PD-1/L1治疗中位总生存期(OS)达16.8个月,接近低TMB患者的的两倍(vs 8.5个月)!同时,高TMB患者的治疗持续时间更长,治疗获益率达到80.6%。
此外,研究者还分析了其他非小细胞肺癌常见的致癌突变,结合NCCN的治疗推荐,进行了相应靶向治疗的晚期患者大幅度延长生存期(18.6个月vs 11.4个月),可见精准治疗这条路正把患者带向更好的未来。

(图源:pixabay.com)
还记得上学的时候,药理学老师就常常说,别看药物开发只需要做1/2/3期临床试验,实际上市之后很长一段时间,都是在进行隐形的“4期临床”。
确实是这样,大多数药物信息来源于少数的临床研究和医学机构,但是美国85%的癌症患者是在社区诊所就医[2]。患者永远不会照着教科书生病,不同的个体特征疾病特征远比临床研究纳入的被试要“丰富多彩”,临床试验的漂亮数据是否能够在所有患者群体中复制呢?
这就有了“真实世界数据(RWD)”。
本次研究使用的电子病历(EHR)来自著名EHR公司Flatiron Health,全面基因组测序分析(CGP)数据则来自我们曾介绍过的Foundation Medicine(FMI),二者结合构建的临床-基因组数据库(CGDB)一共包括了来自275个机构、38个癌种、近30000名患者的数据。

(图源:FMI官方网站)
经过条件筛选,共纳入了4064名非小细胞肺癌(NSCLC)患者,其中位年龄66岁,女性占51.9%,78.3%患者有吸烟史,77.6%为鳞癌,21.4%患者具有EGFR、ALK、ROS1等NSCLC常见致癌突变,分布比例也接近癌症基因图谱的数据。
值得一提的是,这些患者中非白种人达到了20.6%,包括3.6%的亚洲人,高于一般临床研究的比例,这就是真实世界数据的意义所在了。

患者特征(局部)[1]
考虑到晚期患者的基因组景观更典型,数据分析主要局限于晚期NSCLC患者(n=3522),中位总生存期为10.3个月,5年生存率3.8%,各亚组的临床结果特征也与之前的临床研究基本一致。
那么现在就来看看关键的PD-L1和TMB吧。
所有患者中,共有1235名做过PD-L1检测,其中482人做过免疫治疗,但是他们的临床结果却显示,PD-L1水平与生存期、持续治疗时间都是无关的。
估计大家也预想到了,不论PD-L1阴性阳性,TMB水平是没有差异的,都是6.95 mutations/Mb,这和之前临床研究的结果也是基本一致的[3]。

PD-L1水平与TMB,没关系[1]
以20 mutations/Mb为界,从接受免疫治疗开始计算生存期,高TMB患者中位生存期达到16.8个月,而低TMB患者仅有8.5个月;同时,前者的治疗持续时间达到了7.8个月,治疗获益率80.7%,后者则分别仅有3.3个月和56.7%。
另外,在那些没有接受免疫治疗的患者中,TMB的高低和患者的生存期似乎并没有什么关系。有吸烟史的患者TMB水平更高,存在致癌突变的患者TMB则更低。

以20为界,生存差异显著[1]
研究者还分析了其他一些NCCN指南有相应治疗推荐的致癌突变靶点,比如EGFR、ALK和ROS1,共有1260名患者具有这些突变,但是其中只有48.3%选择了相应的靶向治疗。药物选择的影响因素很多,这里不讨论了,就且看看对预后的影响吧。
很显然,遵循NCCN指南推荐很有利于患者生存,采纳相应靶向治疗方案的患者中位总生存期达到18.6个月,没有用靶向治疗的患者则仅有11.4个月。

靶向治疗有益生存[1]
以最常见的EGFR突变为例,采取靶向治疗的患者生存期达21个月,治疗持续时间10.3个月,临床获益率86.1%;没做靶向治疗的患者三项数据分别为13.3个月、2.8个月和50.9%。
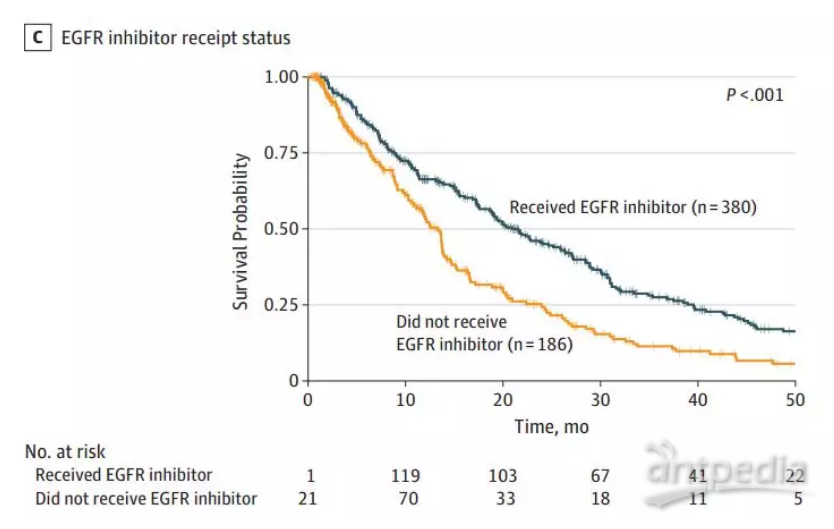
EGFR靶向治疗获益[1]
总的来说,真实世界数据基本重现了临床研究中描述的患者基因组特征、致癌突变特征、靶向治疗的反应、以及TMB与免疫治疗反应之间的关系,一方面扩大了临床结果的使用,一方面也说明真实世界数据库大有可为。中美肺癌患者致癌突变差异还是比较大的,如果国内开展类似的研究,应该也能够为中国的肺癌治疗提供新的信息。
在JAMA同期配发的评论[4]中,专家提到真实世界数据有三个重要的意义:
第一,扩大对治疗结果的认识。真实世界数据涵盖了更加多样化的患者,对于药物长期毒性和并发症也有更深的了解,这是单单凭借临床研究无法实现的。
第二,正确衡量医疗创新的成效。从研究走向真正的临床,新药/新治疗方案的应用、质量、有效性都需要真实世界数据来确认。
第三,指导临床研究的设计。在真正的应用场景下,真正要解决的问题是什么,目标的患者是什么群体,这是理论无法得出结果,只有真实世界数据才能够体现的。
同时专家也提出了担忧。包括FDA提出的“突破认定”在内,现在新药研发的大趋势就是降成本、加速度,真实世界数据的使用很可能会把研究导向新的综合控制方法,使药物研发脱离经典的随机化分析。没有可靠的对照组,药物的治疗效果可能没法客观衡量。

本文作者也在论文中讨论了相关的局限。由于临床上对患者资料的收集程度受机构规定、主治医师习惯等等因素影响,电子病历并不能保证资料齐备且100%“真实”。但不得不说的是,这还是一个相对来说较为年轻的领域,这些问题都可以通过标准化的方案来解决。
话再说回免疫治疗。关于TMB到底多大适合作为治疗推荐,目前NCCN还没有给出明确的数字。前段时间召开的AACR2019年年会上[5],一项最新公布的数据或许可以给我们一个参考答案。
在一项PD-L1抗体治疗晚期/转移NSCLC的2期临床中,研究者利用FoundationOne®Liquid检测了患者的血浆TMB(bTMB),分析结果显示,bTMB≥16 mutations/Mb的患者或许是理想的受益群体。数据显示,以20为界,高bTMB患者客观缓解率(ORR)达36.8%,低bTMB患者则仅有5%;如果以16为界,二者数据则分别为28.6%和4.4%。
由于检测bTMB有一定条件,对于那些血浆ctDNA较少无法检测TMB的患者来说,其实也能够从免疫治疗获益。
眼看着以基因检测为基础的各种精准治疗越来越好,感觉也是蛮欣慰的,希望咱们老去的那一天癌症都能束手就擒吧。
参考资料:
[1]https://jamanetwork.com/journals/c/article-abstract/2730114
[2]Consortium APG; AACR Project GENIE Consortium. AACR Project GENIE. Cancer Discov.2017;7(8):818-831.
[3]Carbone DP, Reck M, Paz-Ares L, et al; CheckMate 026 Investigators. First-line nivolumab in stage IV or recurrent non-small-cell lung cancer. N Engl J Med. 2017;376(25):2415-2426.
[4]https://jamanetwork.com/journals/jama/article-abstract/2730097
[5]https://www.aacr.org/Meetings/Pages/MeetingDetail.aspx?EventItemID=174