西安交大Science子刊发表神经学研究新成果
来自西安交通大学、多伦多大学等机构的研究人员在新研究中揭示了神经性疼痛的分子根源,证实其是由于大脑岛叶皮质(Insular Cortex)中突触NMDA受体增加所导致。从而为推动开发出有潜力的靶向治疗指明了新方向。研究论文发表在5月14日的《科学信号》(Science Signaling)杂志上。
西安交通大学的招明高(Ming-gao Zhao)教授和卓敏(Min Zhuo)教授是这篇论文的共同通讯作者。前者主要从事中枢神经系统突触可塑性、学习记忆和情感障碍的分子机制研究,在SCI杂志上发表论文38篇。后者现为加拿大皇家科学院院士, 多伦多大学生理系终身正教授。主要研究方向有为中枢学习记忆机制, 痛觉传递的中枢可塑性及其突触分子机制, 焦虑和其他精神病机制。在Nature,Science,Neuron等国际权威杂志上发表论文200余篇。
神经性疼痛是一种神经系统原发损害或功能障碍引起的慢性疼痛疾病,多种不同的损伤,如外伤、神经损伤或感染都可引起神经性疼痛。神经性疼痛一直是困扰医学界的难题,由于其发病机理不清楚,阿片类药物治疗效果不佳,患者非常痛苦。因此深入地了解神经性疼痛的复杂病理机制,将有助于为治疗提供新的思路和方法。
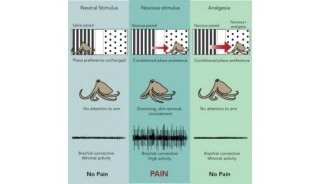
在这篇文章中,研究人员利用小鼠模型证实周围神经损伤可导致神经性疼痛发生,岛叶皮质突触可塑性发生改变,其与突触N- 甲基-D- 天氡氨酸受体(N-methyl-D-aspartate receptors ,NMDARs)数量长期升高有关,但与突触外NMDARs数量无关。他们发现,激活环腺苷酸(cAMP)依赖性信号通路,可以提高急性分离岛叶皮质切片中的突触 NMDARs数量,促进培养皮质神经元中NMDARs细胞表面定位。研究人员证实,通过AC1(腺苷酸环化酶亚型1)/ PKA(蛋白激酶A)/ SFK(Src家族激酶)信号通路磷酸化NMDAR亚基GluN2B,其是NMDARs数量增高的必要条件。当他们将NMDAR或GluN2B特异性拮抗剂注入到岛叶皮质中时,证实可以降低神经性疼痛小鼠模型对于正常非伤害性(nonnoxious)刺激的行为反应。
这些结果表明,神经损伤可引起岛叶皮质突触NMDA受体增加,导致出现活动依赖性可塑性(activity-dependent plasticity),从而引发了神经性疼痛发生。抑制NMDAR功能将有助于预防或治疗神经性疼痛。
-
精英视角

-
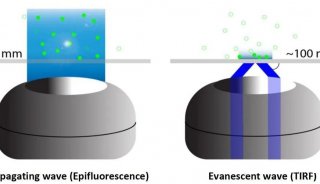
技术原理