最新的分子间相互作用分析技术---微量热泳动仪(MST)
微量热泳动仪-microscale thermophoresis (MST)是由总部设在慕尼黑的德国高科技公司NanoTemper技术有限公司发明的设备。2010年底的一篇Nautre的文章《Protein-binding assays in biological liquids using microscale thermophoresis》最先报道了NanoTemper公司创始人Dr. Stefan和 Dr. Philipp使用MST测量生物溶液中蛋白-蛋白之间的相互作用,引起了很多科研人员的极大兴趣。随后这个产品正式投入市场,在2011年就有很多客户购买试用,2012年就有130个国外的实验室购买使用。而且在短短的一年多的时间内,相关数据已经发表到nature,cell,PNAS等期刊,大大受到用户们的欢迎。
MST背景技术介绍
微量热泳动是粒子在微观的温度梯度中的定向运动。通过测量水化层的变化(通常是由生物分子结构/构象的变化引起的)而导致的微量热泳动的变化来确定亲和力。甚至像蛋白质磷酸化或小分子结合到靶标上这些微小的变化都可以被测量到。MST也允许直接在溶液中测量分子间相互作用,而不需要一个固定的表面(无需固定)。MST是由总部设在慕尼黑的德国高科技公司NanoTemper技术有限公司发展出来的。
微尺度热泳(MST)是一种新的方法,可以定量分析溶液中微升的分子间的相互作用。MST是基于微量热泳动效应,即沿温度梯度定向的分子运动。一个空间的温度差ΔT导致分子浓度在温度升高的地区的变化,用Soret系数ST定义为:C热/C冷= EXP(-STΔT)。
热泳动取决于分子和溶剂之间的界面。在恒定的缓冲条件下,热泳动反映出分子大小,电荷和溶剂化熵。 一个荧光标记分子A的热泳动由于大小、电荷和溶剂化熵的差异通常明显不同于分子A和靶标T形成的复合物AT。这种热泳动的区别可以用来通过梯度滴定实验,在一定缓冲条件下,测量计算出分子间的结合常数。
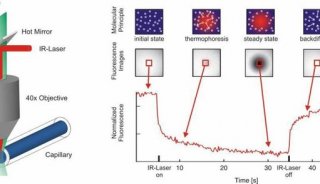
测量荧光标记分子的热泳运动是通过监测毛细管内的荧光分布F。红外激光产生微观的温度梯度。溶液在激光光斑处的温度升高ΔT= 5 K,之前的红外激光是在同质化的荧光分布F是毛细管内观察到的冷切换。当红外激光打开后,两方面因素影响荧光的分布(热弛豫时间和荧光标记分子的热泳动),但是由于其时间尺度分离(热弛豫时间很短和荧光标记分子的热泳动时间较长),有利于我们测量荧光分布F热。在较慢的热泳动时间内(10秒),分子运动从局部加热区域移往四周的低温地区,中心区域的分子浓度降低,由于质量扩散效应的反作用,最后分子的分布直到达到一个稳定态。
虽然质量扩散D的决定消耗的动力学,S、T确定的稳态浓度比例下温度上升Chot/Ccold=exp(-ST ΔT) ≈ 1-STΔT。归一化荧光Fnorm= F热/ F冷主要是这个浓度比,除了温度跳跃∂F /∂T的线性近似,我们发现:Fnorm= 1 +(∂F /∂TST)的温差。由于荧光强度的线性和热泳枯竭,Fnorm(A)未结合的分子归荧光和约束复杂的Fnorm(AT)线性叠加。 表示x的绑定到目标分子的一小部分,在目标T滴定的荧光信号不断变化的计算公式如下:Fnorm=(1-x) Fnorm(A)+x Fnorm(AT)。
定量绑定参数获得通过的约束力基板的连续稀释。通过绘制F规范对系列稀释的不同浓度的对数,获得一个S形的结合曲线。这种结合曲线,可以直接安装质量作用定律的非线性解与解离常数K ð,作为结果。微量热泳(MST)是一种分析生物分子的技术。微尺度热泳是粒子在微观的温度梯度中的定向运动。


实验流程
很简单的实验方法,使用便宜的毛细吸管作为耗材,避免了昂贵的样品消耗和繁琐的制备过程。相对于其他的已有的测量分子间相互作用的技术,MST结合毛细管使用大大降低所需的实验成本,并且可以测量天然状态环境中的生物分子间的相互作用。
荧光分子的浓度的保持不变而结合物分子的浓度梯度增加。将6ul的样品量被填充在MST毛细血管,然后使用制造一个局部温度梯度。由于标记分子在玻璃毛细管中的运动导致的区域荧光强度变化就会被观测到。既可用标记的荧光染料/融合表达的荧光蛋白来发光(NT.115系统),也可以用色氨酸自发荧光来检测(NT.LabelFree系统)。通过检测不同浓度的结合物分子对荧光分子热泳动平衡态的分布的影响,从而获得这两个分子间相互作用的各种参数。
荧光分子最初是自由均匀分布的。在红外激光照射下,分子受到热泳动的作用力,从加热区域向低温区域移动,同时分子又受到浓度梯度和质量扩散力的作用,最后分子在热泳动作用力和质量扩散作用力下达到平衡,形成稳定态。在关闭红外激光后,分子扩散重建均匀分布状态。下图显示了该过程。



主要特点
样品处理方面:
☆ 不需要固定,在生物溶液中测量,无需纯化
☆ 无需标记测量
☆ 使用荧光染料/荧光蛋白具有良好的选择性
☆ 极低的样品消耗量
☆ 直接在脂质体或者去污剂中研究膜蛋白
☆ 研快速简单的实验准备
测量数据方面:
☆ 10分钟之内测量任何(生物)分子间亲和力(KD, 解离常数)
☆ 测量sub-nM到mM 级的解离常数
☆ 可以选择特定温度下完成测量
☆ 研究各种不同大小的分子:离子、片段、核小体、脂质体
☆ 可以在各种不同的溶液环境中完成测量,包括研究膜蛋白所需的复杂的去污剂环境
☆ 广泛的样品兼容性:天然的环境中、生理学实验条件、血清、细胞裂解液
☆ 可以研究多组分反应:三元复合物、装配顺序、干扰因素、协同作用、类似物
☆ 可以区分靶标上不同的结合位点
☆ 可以测量生物分子的寡聚化
☆ 研究化学计量学并确定生物分子结合位点的数目
☆ 研究结合能量学ΔG (自由能 ),ΔH (焓) 和ΔS (熵)
☆ 研究蛋白的折叠和稳定性
实验操作方面:
☆ 非常简单易操作
☆ 实时获得数据
☆ 非常稳定的技术
维护费用方面:
☆ 非常低的运行成本
☆ 不需要日常的仪器维护
☆ 更快得到数据用于发表文章
☆ 仪器小型化设计,占用空间少