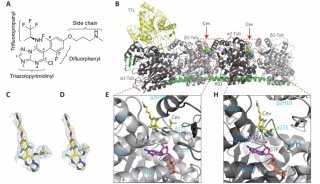
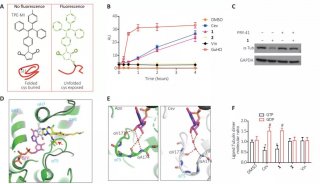
METTL16介导通过阻碍对剪接位点的识别从而抑制RNA剪接
RNA m6A修饰是目前RNA表观遗传领域研究的热点,对于m6A的甲基化酶和去甲基化酶,相信大家也是耳熟能详。事实上,大名鼎鼎的METTL3仅能结合约22%的m6A位点,这提示还有其他m6A甲基化酶。确实,在METTL3之后,METTL16也被鉴定为m6A甲基化酶,但是它的底物远不如METTL3的底物丰富,主要是U6 snRNA和S-腺苷甲硫氨酸(SAM)合成酶MAT2A。值得注意的是,SAM是细胞甲基化的甲基供体,包括m6A修饰的甲基也来自SAM。因此,MAT2A的表达量与SAM的稳态密切相关。有趣的是,METTL16具有保守的N端甲基转移酶结构和仅在脊椎动物中才有的C端无催化活性的VCR结构(vertebrate-conserved region)。已有研究证明METTL16的C端VCR对MAT2A的正确剪接很重要。那么,这就引出一个问题,在细菌到人中都保守的METTL16甲基转移酶结构的功能是什么?
近日,来自瑞士日内瓦大学的Ramesh S. Pillai和David Homolka在Cell发表研究
Splice site m6A methylation prevents binding of U2AF35 to inhibit RNA splicing,该研究发现METTL16介导的3’剪接位点AG的m6A修饰可以阻碍U2AF35对剪接位点的识别,从而抑制RNA剪接。

为了回答METTL16甲基转移酶结构的功能的问题,研究者利用线虫中METTL16的同源蛋白METT-10开展实验,因为METT-10不含VCR结构(图1)。通过在m6A-IP-seq,研究者在线虫中鉴定到了176个m6A位点(线虫不具有METTL3-METTL14复合体,所以m6A水平较低)。通过对比敲除METT-10后m6A的变化,研究者进一步确定了METT-10也调控U6和SAM合成酶SAMS-3,SAMS-4,SAMS-5的m6A水平,这与METTL16在哺乳动物中的功能一致。然而,METTL16介导SAM合成酶3’UTR的m6A修饰,而METT-10催化的m6A却是在SAM合成酶的2号内含子的3’剪接位点AG上。
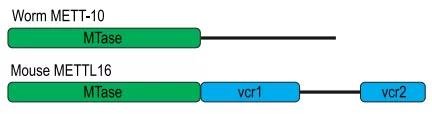
图1 线虫和小鼠中METTL16的结构对比
由此,研究者推测,METT-10催化的m6A可能与可变剪接相关。确实,通过in vivo和in vitro实验,研究者发现当3’剪接位点AG携带m6A修饰时,U2剪接辅助因子U2AF35无法正确识别这一位点,造成内含子的异常滞留。
以上实验都是将线虫培养在营养丰富的饮食条件下得到的,研究者意外的发现,当给予低营养条件时,METT-10调控SAM合成酶异常剪接的现象消失了。这提示了一种SAM的负反馈调节:即高营养时,细胞内SAM较丰富,METT-10通过介导SAM合成酶3’剪接位点的m6A修饰,抑制其正常的剪接,从而降低SAM的含量;而在低营养条件下,METT-10则不影响AM合成酶的剪接,从而保证SAM的产生(图2)。但是尚不清楚METT-10如何响应营养变化。
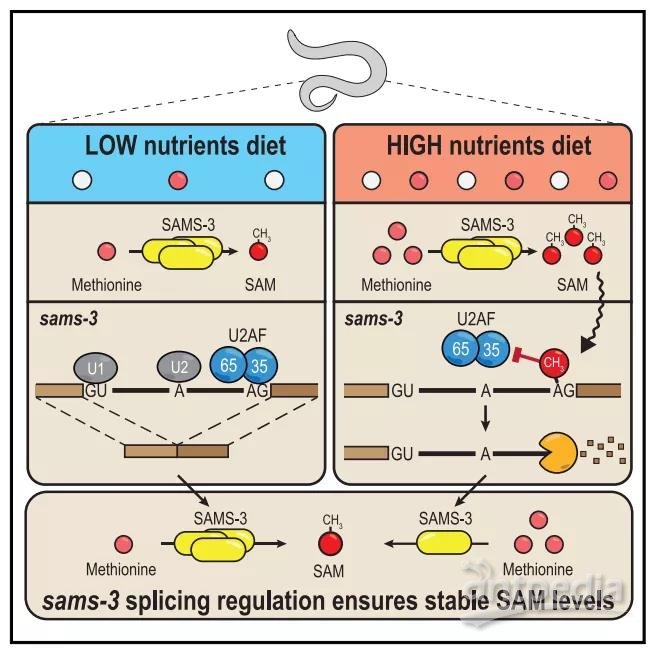
图2 不同营养条件下METT-10的功能
值得注意的是,线虫和哺乳动物在低SAM情况下对SAM的调节不同。面对SAM的缺乏,线虫是保证SAM合成酶的正常合成,一种听之任之一切随缘的态度;而哺乳动物却急不可耐的通过METTL16的VCR结构促进SAM合成酶的剪接,显示出对SAM含量的更高需求(图3)。这可能与哺乳动物的胚胎发育更依赖SAM有关,也因此,在小鼠中敲除METTL16会造成胚胎死亡,而线虫在缺失METT-10后仍能存活。

图3 线虫和小鼠中METTL16对SAM的响应
虽然哺乳动物的METTL16通过3’剪接位点调控SAM合成酶的剪接,但是研究者确实通过测序分析找到了一批在小鼠细胞中受METTL16调控的3’剪接位点,说明METTL16通过介导3’剪接位点AG的m6A甲基化,从而调控剪接的机制是保守的。但是对于小鼠和人中METTL16的靶基因还需更多的in vivo实验验证。
总的来说,该研究揭示了METTL16介导的m6A甲基化在可变剪接中的重要功能,并发现线虫利用这一机制响应饮食的变化和SAM稳态。有趣的是,除了本研究提到的m6A调控SAM稳态,SAM也可以调控m6A水平:在饮食中限制甲硫氨酸的摄入能降低METTL3介导的m6A,并有望成为多囊肾病的新的治疗思路。