质谱入门
今天我们继续了解学习有关质谱的其他问题,让我们共同学习,共同进步,希望对大家有所帮助。
常见的样品分离方法和样品递送方法
1.气相色谱(GC)
可能对很多人来说,第一次接触质谱是将其作为气相色谱的检测器。GC/MS联用仪类型的范围已大大扩展,超越早期仪器设计的范围,在使用中满足日渐严格的法规要求,像环境分析、食品安全筛查、代谢组学,以及包括法医学、毒理学和药物筛查的临床应用。在过去,两种类型的质谱主导着GC/MS分析:扇形磁场和单四极杆质谱仪。对于前者,可提供高分辨率和准确的质量分析,用于有极高灵敏度要求的分析中。后者适合目标化合物的常规分析。
2.液相色谱(LC)
这是一项革命性的技术,为大约80%不能采用GC分析的化学物质提供了分析途径,在近几十年来促进了质谱技术的显著提高。少数几个模型被挑出来,开始实现MS与LC联用。可以说LCMS联用开始于1970年代,在1990年代早期,我们今天所熟知的LCMS技术成熟起来。很多现在我们使用的装置和技术都直接来自那个时候。
在1900年代早期,俄国植物学家Mikhail S.Tswett定义了液相色谱技术。他的研究工作主要是分离从植物萃取的叶色素,在他的研究中,他用溶剂冲洗装填微粒的柱子。这是液相色谱最简单的形式,被测物溶解的溶液(流动相或浓缩相)与溶液流过的装填颗粒的床体(固定相)之间存在竞争作用,液相色谱就是依靠这种可预测、不断再现且具有很高精确性的相互作用实现分离。近年来,在色谱柱中装填各种功能性组分,以及能够准确传送流动相的溶剂输送系统的发展,使得LC成为很多分析行业的支柱。
首字母缩略词HPLC是由Csaba Horváth在1970年提出,表明对液相色谱填充柱需要施加高压,以引起液体流动。从那以后,液相色谱的效能不断提高,较小颗粒的填料和较高的选择性上都取得了发展,将首字母缩略词改为高效液相色谱。
2004年,仪器和色谱柱技术的进一步发展极大地提高了液相色谱的分离度,速度和灵敏度。具有较小颗粒(1.7微米)的色谱柱和旨在提供15,000 psi(1,000 bar)流动相的专门功能的仪器已被称为UPLC技术,代表了 “超高效液相色谱”。1970年代,诸如约翰·诺克斯(John Knox)这样的调查人员预言了当前技术中所包含的大部分内容。诺克斯预测最佳粒径为1-2μm,色谱法对摩擦热具有热敏感性。在开发可广泛使用的UPLC的过程中,必然遇到了能够开发出坚固,均匀的小颗粒的技术。
大气电离方法
1.电喷雾电离[ESI]
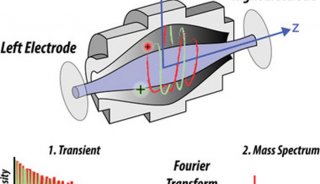
大气压电离(API)的最重要的技术是ESI,ESI为各个相关的技术提供了基础,这些相关技术能在大气压,而不是在真空下形成离子。样品溶解在极性溶剂中(一般比GC上使用的溶剂更难挥发),然后泵入不锈钢毛细管,不锈钢上施加2000到4000V的电压。当液体在大气压下,从毛细管流出时,液体被雾化,被雾化的液滴进一步去溶剂,释放出离子进入质谱仪。在静电吸引和真空联合效应下,诱导电离生成这些气态离子。如下图所示,位于前端的ESI探针,与MS离子入口垂直。当溶剂进入分析器的稀薄真空区域时,锥体或逆流气通常辅助液滴去溶剂化。
电势从液体转移到被分析物从而形成离子的机制仍然是个争论的主题。在1968年,Malcolm Dole提出电荷残留机制,在该机制中,他假定当液滴挥发时,液滴的电荷仍保持不变。液滴表面张力最终不能平衡电荷斥力,将小液滴炸裂成很多更小的液滴。持续发生这样的库仑力爆破,直到小液滴只含单一的被测物离子。当溶剂从最后形成的小液滴中挥发掉,即形成气态离子。在1976年,Iribarne和Thomson提出了一个不同的模型,即离子挥发机制,在该机制中,通过库仑裂解形成小液滴,这类似于Dole模型的形成方式。但是,按照离子挥发理论,在液滴表面的电场强度相当高,使溶剂化离子逸出液滴表面,并直接将其转移进入气相,形成气态离子。实际上,这两种机制可能协同起作用:对于大于3000Da的物质,电荷残留机制起主导作用,而对于较低质量的分子,离子挥发机制起主导作用(参见R.Cole,"关于电喷雾电离质谱的一些原则",质谱杂志)。
液相色谱的流出物,以电荷平衡状态进入ESI探针。因此当溶剂离开ESI探针,溶剂需携带有净电荷。为了确保ESI具有连续性,必须通过电化学反应给溶液充电,将电子转移到电极表面。在其它的效应中,该过程可能引起溶液pH值的变化。据推测,在阳离子模式时,带正电液滴离开喷雾器,电极(氧化作用)必定要吸收电子。(在阴离子模式下,则相反。)电活性电极的表面面积、电流大小和化学品种类及其电极电势的特性都将产生影应。
总的来说,ESI是一高效过程。不过,反应的活化量和能量差异对不同的物种是不同的。溶液流速和使用的电流对每个液滴形成也有限制。分子间的竞争以及目标被测物抑制效应也较为常见。离子形成之后,离子被"拖"过电势梯度(电场),到达计数板。如下图。
2.大气压化学电离[APCI]
虽然大气压化学电离(APCI)技术与ESI同时发布,但是在1985年Fenn的研究成果发布,ESI很快商业化,而直到此时,APCI也没有广泛被采用。在1973年,Horning首次提出APCI,采用包括HPLC在内的各种导入技术,分析挥发性组分。APCI的附加功能是,将ESI难以转化为气相离子的被测物,即那些极性很小且易挥发的被测物经浓缩相(或液体)导入质谱仪。不同于ESI,APCI通过在热的气流中蒸发引导液,将中性被测物转化为气相。化学电离依赖于电荷在反应离子和目标分子之间的转移,产生可被分析的目标离子。大多数情况下,以阳离子模式在目标分子与小的H+离子之间形成加合物,虽然与盐的加合物也比较常见。
3.生物分子电离方法
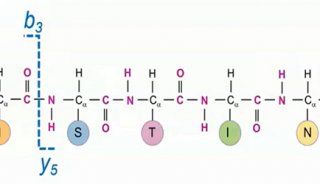
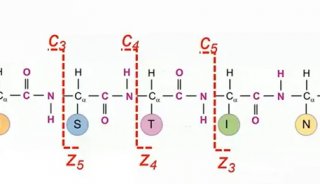
用于生物大分子鉴定的电离技术已经成熟,这类技术电离方式比较温和,不会将生物分子打碎。在生物分子分析和蛋白组学中公认有两个"能量沉积"过程,分别是电子捕获解离(ECD)和电子转移解离(ETD)。两种电离法都可以断裂邻近电子捕获位点的化学键,不同于其它裂解过程,比如碰撞诱导解离(CID),断裂的键在分子内不是最不稳定的。实测的断裂对肽序列的依赖性较低,因此在肽骨架中,大多数氨基酸之间的断裂往往不依赖于分子大小。在肽的ECD和ETD中,最主导的裂解形成c和z离子。ECD已证实,对不稳定的翻译后修饰分析有效,比如磷酸化作用和O-糖基化,以及完整蛋白的裂解分析。当结合酰胺氢/氘交换分析时,已表明ESI质谱法能进一步辅助阐明溶液中蛋白的结构细节。使用较少量样品,由电荷状况分布和ESI在蛋白质上形成的一系列多电荷离子,可以得到较大蛋白的溶液组成信息,而通过其它技术,比如紫外圆二色光谱(CD)和色氨酸荧光不容易实现(但是通常将这些和其它相关技术,比如核磁共振,联合使用)。其它技术只能测定溶液大量蛋白的平均属性,而采用MS的另外一个好处是能提供瞬间或折叠中间体的结构细节。
4.其他电离方法
纯净化合物可置于进样棒或固体探针的顶端,导入离子源。随着加热,样品升华或蒸发,进入气相。在大多数情况下,按此法接着发生电离。但是在一些情况下,电离与升华或蒸发同时发生。
4.1大气压光电离(APPI)
被测物直接或掺杂剂辅助光量子电离,电离电势低于10eV(主要由氪气灯的光量子能量输出)。LC通常使用的溶剂电离电势大于10eV。在实验室中,APPI是主要的API替代方法之一,因为APPI扩展了非极性被测物的电离范围,可以电离那些ESI和APCI有效电离的化合物。
4.2基质辅助激光解吸(MALDI)
是一种软电离技术,用于完整蛋白、肽和大多数其它生物分子(寡核苷酸、碳水化合物、天然产物和脂),以及异质样品的分析(复杂生物样品的分析,比如蛋白水解消化物)。高能的光量子与混入有机基质的样品之间的相互作用,通常具有低于皮克摩尔的灵敏度。
4.3快原子轰击(FAB)
软电离的早期方式,使用铯离子流,从溶解在甘油或类似基质的样品喷射出离子;等离子体解吸附(PD):核裂解片段与沉积在金属箔上的固体样品的相互作用;次级离子MS(SIMS):高速离子撞击沉积在金属板上薄层样品,或包含在液体基质的薄层样品(液体SIMS);解吸附电喷雾电离(DESI):像实时直接分析(DART )、大气压固体分析探针(ASAP)等紧密相关的技术,以及其它近来进入市场的技术,这些技术往往通过在一个表面的二次相互作用得到离子。在DESI中,带能液体流对准沉积在平面上的样品,在大气压下引起二次电离。
使用什么类型的质谱仪器?
在质谱分析中,对实验控制力是尤其重要的。一旦在周密的控制条件下得到离子,必须以适合的灵敏度将每个离子作为离散事件实施检测。极少量的气体载量使GC成为联用技术早期理想的选择,但仅仅适合20%的化合物分析。现今,我们在大多数情况下雾化LC洗脱液,将其作为质谱仪中导入被测物实施电离的方法,该技术要求确保真空环境。
任何质谱仪的一个重要设计元素是泵的容量。真空必须完全分布到仪器的所有稀薄大气区域,并且泵容量必须充足,以满足设计上的要求,比如离子入口的大小和需要去除蒸汽的量。
1. 分析器:质谱仪的心脏
分析器是分离或区分导入离子的仪器。在离子源可以形成正负离子,以及不带电的中性粒子。但是,在指定时刻仅能记录一种极性。现代的质谱仪能够在毫秒间转换极性,得到高保真记录,即使快速短暂事件,如典型的UPLC或GC分离中,峰仅仅大约1秒宽。
2. 四极杆和扇形磁场
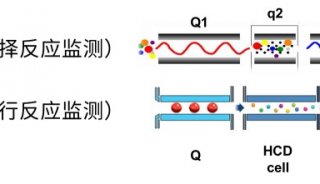
在1953年,西德物理科学家Wolfgang Paul和Helmut Steinwedel描述了四极杆质谱仪。在4根平行杆之间,叠加的射频(RF)和恒定的直流(DC)电势能够作为质谱分离器,或过滤器,仅限于特点质量范围的离子,以恒定振幅振荡,能够在分析器上收集。现代仪器制造商将四极杆瞄准到特定的应用中。单四极杆质谱仪要求基质干净,以避免无用离子的干扰,表现出非常好的灵敏度。
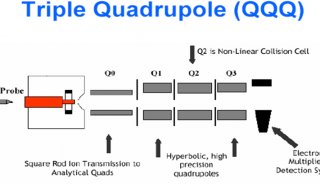
三重四极杆,或串联四极杆(参见四极杆),是将一个四极杆加到另一个附加的四极杆上,四级杆串联后能以各种方式发挥作用。一种途径是通过离子独有的质荷比(m/z)分离并检测复杂混合物中的目标离子。证实串联四极杆有效的另一途径是当与可控裂解分析联用时。这些分析通常将目标离子与其它分子(典型的气体,如氩)进行碰撞,母离子裂解成产物离子,MS/MS质谱仪通过其独特组成部分鉴别目标化合物。
当设置过滤某一特定离子,那么其它质量的离子则会以多种方式中丢失,比如撞击到四极杆上,或直接偏离去检测器的轨道。四级杆分析器由四根杆组成,通常平行排列,材质为金属,比如钼合金。如下图。
已投入了大量的技术和研究,设计开发四极杆。按照离子在DC和RF场中的运动,将质量分类。通过在软件上改变参数,系统可改变场强,在任何指定时间内,某一m/z值的离子被过滤掉,或通过四级杆到达检测器。相比于一些质谱仪的设计,比如飞行时间TOF质谱仪(Tof),四极杆分辨率较低。而四极杆相对简单,容易使用,是具有较高实用性的质谱仪,能以相对低的成本提供各种接口。
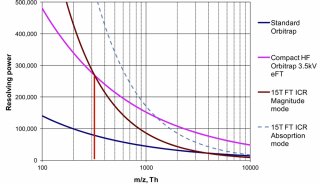
在比较和说明质谱仪的分析能力时,一些专业用语是必须的,例如:分辨力(通常缩写为"res"-质谱仪分离两种质量的能力),低分辨力的单位质量为1000;较高或中等分辨力为1000到10000;高分辨力为10000+;非常高的分辨力为高达3-5百万。