Epizyme递交EZH2抑制剂新药申请,治疗滤泡性淋巴瘤
昨日,FDA肿瘤学药物咨询委员会以11:0的投票结果,支持Epizyme公司开发的“first-in-class“EZH2抑制剂tazemetostat治疗转移性/局部晚期上皮样肉瘤患者。几个小时之后,Epizyme公司宣布,已经向美国FDA递交tazemetostat的新药申请(NDA),寻求加速批准这一创新疗法治疗复发或难治性滤泡性淋巴瘤(FL)患者。这些患者至少接受过两种前期系统性治疗。他们可能携带或不携带EZH2激活性突变。

FL是非霍奇金淋巴瘤的一种。大约20%的FL患者的EZH2基因携带功能获得性基因突变,导致EZH2的活性升高。而这会导致B细胞被“锁死”在生发状态(germinal state),从而促使它们癌变。Tazemetostat通过抑制EZH2的活性,能够让B细胞继续分化或者产生细胞凋亡,从而控制肿瘤的生长。
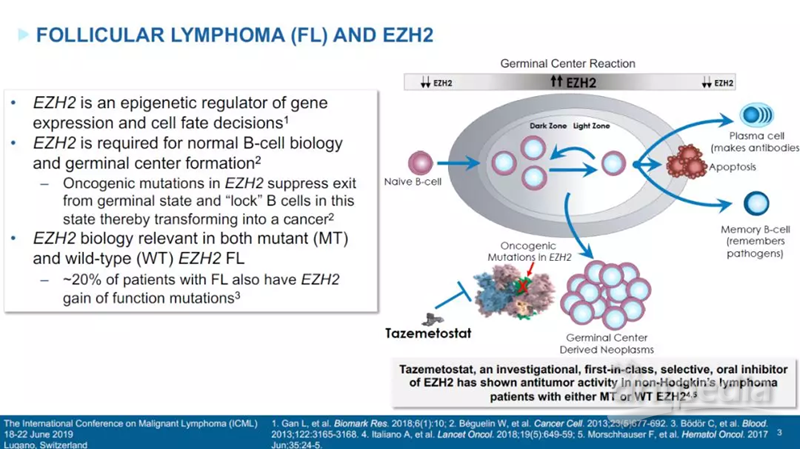
▲EZH2与FL(图片来源:参考资料[2])
这一申请是基于tazemetostat在一项2期临床试验的中期结果。在这项单臂试验中,携带野生型EZH2基因或突变型EZH2基因的FL患者接受了tazemetostat的单药治疗。试验结果表明,tazemetostat治疗携带EZH2突变的患者时达到69%的客观缓解率(ORR),治疗野生型EZH2患者时这一数值为35%。
突变型EZH2患者的中位无进展生存期(PFS)为14个月,野生型EZH2患者的PFS为11个月。这两个患者群的中位OS均尚未达到。

▲Tazemetostat的中期试验结果(图片来源:参考资料[3])
“我们非常高兴能够递交这一NDA,希望将tazemetostat带给FL患者和他们的医生们,”Epizyme公司首席医学官Shefali Agarwal博士说:“FL仍然是一种无法治愈的灾难性疾病。我们相信如果这款创新疗法获批,tazemetostat可能为这些患者的症状带来有意义的改善。”
参考资料:
[1] Epizyme Submits New Drug Application to the U.S. FDA for Tazemetostat for the Treatment of Patients with Follicular Lymphoma. Retrieved December 18, 2019, from https://www.businesswire.com/news/home/20191218005788/en/
[2] Interim Update From a Phase 2 Multicenter Study of Tazemetostat, an EZH2 Inhibitor, in Patients With Relapsed or Refractory Follicular Lymphoma. Retrieved December 18, 2019, from http://www.epizyme.com/wp-content/uploads/2019/11/ICML_2019_FL_Morschhauser_105_oral-presentation_FINAL06212019.pdf
[3] Epizyme Presents Updated Phase 2 Data at the 2019 ASH Annual Meeting Supporting Planned Tazemetostat NDA Submission for Follicular Lymphoma. Retrieved December 18, 2019, from https://www.businesswire.com/news/home/20191207005015/en/
-
焦点事件

-
焦点事件

-
产品技术

-
科技前沿












