QuEChERS结合高效液相色谱测定饲料中的18种β-兴奋剂
QuEChERS结合高效液相色谱-串联质谱法测定饲料中的18种β-兴奋剂
β -兴奋剂( β -agonist),俗称瘦肉精,在化学上属于苯乙胺类药物,一般具有含苯乙醇胺的母体结构。最早用于1988年,主要用于防治人、畜的支气管哮喘和支气管痉挛。这些药物高剂量添加在饲料中,可以选择性地作用于肾上腺素,导致动物体内的脂肪分解代谢增强,增加蛋白质的合成,显著提高胴体瘦肉率。但如果长期食用含有大量 β -兴奋剂残留的动物组织,会对人体健康造成很大伤害,包括中毒、引起恶性肿瘤,甚至致人死亡[1, 2]等。农业部于2002年2月发布的176号公告[3] 《禁止在饲料和动物饮用水中使用的药物品种目录》,其中就将克仑特罗、莱克多巴胺、西马特罗等列为违禁药物。之后,β -兴奋剂类药物一直是国家相关监管部门的重点监测项目之一。由于多年来对禁用药物的严厉监管,犯罪分子转而添加同类替代药物,比如:班布特罗、喷布特罗、苯乙醇胺A等。 β -兴奋剂的滥用严重威胁着人们的身体健康,农业部于2010年12月再次发文(农业部公告第1519号[4]),禁止在饲料和动物饮水中使用班布特罗、齐帕特罗、氯丙那林、马布特罗、阿福特罗、溴布特罗、喷布特罗、苯乙醇胺A等物质。因此,建立多组分的同时测定方法,在实际监督和执法工作中对饲料进行实时监测具有重要的意义。
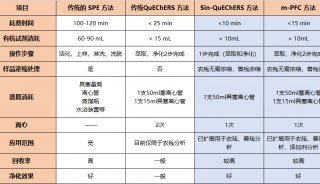
QuEChERS方法[5, 6]利用吸附剂填料与基质中的杂质相互作用吸附杂质,从而达到除杂、净化的目的。因具有快速(quick)、简单(easy)、廉价(cheap)、有效(effective)、可靠(rugged)和安全(safe)的特点而得名。此方法一经问世就受到各国农药残留分析者的普遍关注,发展十分迅速,现已成功地用于多种食品中多种农药残留的分析[7, 8, 9, 10, 11, 12]。QuEChERS方法很灵活,可根据分析物、基质、仪器和分析者的偏好对净化剂、盐量、水含量和吸附剂等做改进,改进的方法也适用于含中等或高脂的食物。因此,近年来该技术也开始应用于兽药残留检测领域[13, 14, 15]。
有关 β -兴奋剂的分析测定方法涉及液相色谱法[16]、(气相、液相)色谱-质谱法[17, 18, 19]、酶联免疫吸附法[20]等。实际工作中,多采用液相色谱-质谱联用法进行确证,因为此法可以同时满足高灵敏度、高选择性的定性定量要求。但在已报道的液相色谱-串联质谱测定方法中,前处理方法多为固相萃取方法,鲜有QuEChERS方法在饲料中 β -兴奋剂类违禁药物检测中的应用报道。目前已发布的饲料中 β -兴奋剂类违禁药物的国家标准[21, 22]及报道的测定方法[23]使用的也是固相萃取法。本文建立了QuEChERS结合HPLC-MS/MS同时测定饲料中18种 β -兴奋剂的方法,为饲料中 β -兴奋剂类违禁药物的监控提供了又一个快速、有效的方法,有利于提升对 β -兴奋剂类违禁药物的监控水平。
1 实验部分跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
1.1 仪器与试剂跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
液相色谱-串联质谱仪:Agilent 1200 RRLC+Agilent 6410B质谱仪,配电喷雾离子源(ESI)(美国安捷伦科技有限公司);高速离心机:Sigma3-18k(德国Sigma公司);振荡器:YAMATO SA300(日本Yamato Scientific Co. Ltd.);超纯水器:Milli-Q Reference(美国Millipore公司)
克仑特罗(clenbuterol)、班布特罗(bambuterol)、马布特罗(mabuterol)、克仑丙罗(clenproperol)等标准物质纯度均大于98% ,喷布特罗(penbutolol)纯度96% ,莱克多巴胺(ractopamine)纯度97% ,购自Dr. Ehrenstorfer GmbH;西马特罗(cimaterol)、西布特罗(cimbuterol)、氯丙那林(clorprenaline)、溴布特罗(brombuterol)、马贲特罗(mapenterol)、溴代克伦特罗(bromchlorbuterol)等纯度均为99% ,购自WITEGA Laboratorien Berlin-Adlershof GmbH;苯乙醇胺A(phenylethanolamine A)、妥布特罗(tulobuterol)、利托君(ritodrine)等纯度均为98% ,齐帕特罗(zilpaterol)纯度95% ,购自Toronto Research Chemicals Inc.;阿福特罗(arformoterol)纯度99.9% ,购自International Laboratory USA;苯氧丙酚胺(isoxsuprine)纯度99.5% ,购自U. S. Pharmacopeia。
C18、PSA粉末(40~63 μ m,CNW公司);甲醇、乙腈、甲酸(色谱纯);无水硫酸钠、氯化钠(分析纯);水为Milli-Q超纯水。
1.2 标准溶液的配制跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
称取各标准品10.0 mg,用甲醇溶解并定容至100 mL棕色容量瓶中,配成浓度为100 mg/L 的标准储备液,在-18 ℃保存。使用时根据需要用相应的空白样品基质提取液配制适当浓度的标准工作液。
1.3 样品处理跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
称取样品2 g(精确至0.01 g),加水10 mL,涡旋30 s,超声5 min。加入20 mL乙腈(含4% (v/v)氨水)、6 g无水硫酸钠、2 g氯化钠、涡旋混匀后振荡20 min,于4000 r/min 下离心10 min,取2 mL上层清液于净化管中(已加入25 mg C18和50 mg PSA),涡旋2 min,于10000 r/min 下离心10 min,取1 mL净化液于45 ℃氮气吹干,1 mL流动相(甲醇-0.1%甲酸水溶液(1 ∶ 9,v/v))溶解,LC-MS/MS测定。
1.4 HPLC-MS/MS条件跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
1.4.1 HPLC条件跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
色谱柱:ZORBAX Eclipse XDB-C18柱(50 mm×4.6 mm,1.8 μ m)。流动相:A为甲醇,B为0.1%甲酸水溶液。梯度程序:0~1 min,10%A; 1~3 min,10%A~40%A; 3~5 min,40%A~70%A; 5~7 min,70%A~90%A; 7~10 min,90%A; 10~11 min,90%A~10%A; 11~15 min,10%A。流速:0.4 mL/min;柱温:40 ℃;进样量:10 μ L。
1.4.2 质谱条件跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
离子源:ESI;扫描方式:正离子扫描;检测方式:多反应监测(MRM);毛细管电压: 4000 V;雾化气温度:350 ℃;雾化气流速:12 L/min;雾化气压力:310.05 kPa(45 psi)。MRM监测模式下的参数见表1。
2 结果与讨论跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
2.1 提取试剂的优化跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
应用QuEChERS方法进行兽药残留测定时,乙腈或酸化乙腈是常用的提取溶剂。文献[13]显示,添加4%氨水的乙腈能提高 β -兴奋剂的提取率,因此,本实验比较了乙腈、2%(v/v)氨水乙腈、4%(v/v)氨水乙腈、2%(v/v)乙酸乙腈、5%(v/v)乙酸乙腈的提取效果。结果显示,用4%(v/v)氨水乙腈提取,90%的目标化合物回收率在85% ~115%范围内,结果优于其他的提取试剂。部分待测物,如克仑特罗、马布特罗、溴代克仑特罗等,用以上几种试剂提取,回收率无明显差异;而西马特罗、西布特罗、利托君等,在碱性条件下提取,回收率明显高于中性及酸性条件。尤其是齐帕特罗,用4%氨水乙腈提取的回收率高于95% ,而在中性和酸性条件下提取的回收率不足50% 。原因可能是碱性条件能有效抑制这些化合物的离子化,从而增加其在有机相中的分配比例。因此本实验选择4%氨水乙腈为提取溶剂。
| 表1 18种分析物的MRM参数Table 1 MRM parameters of the 18 analytes |
2.2 净化吸附剂的优化跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
在QuEChERS净化方法中,PSA、C18及石墨化炭黑(GCB)是常用的吸附剂。PSA可去除提取液中的脂类和糖类物质,C18具有良好的除脂能力,GCB通常用于除去植物提取液中的色素成分,但对含苯环官能团的化合物有较强的吸附作用[16]。饲料中含有脂类、蛋白(在乙腈提取时已被沉淀)、糖类等干扰组分,而 β -兴奋剂类一般具有苯乙醇胺的母体结构,故本研究只选取PSA和C18作为净化吸附剂进行优化。在同一加标浓度的样品提取液中,
分别加入6个不同组合的PSA和C18(1: 25 mg C18; 2: 50 mg C18; 3: 75 mg C18; 4: 25 mg C18+50 mg PSA; 5: 25 mg C18+100 mg PSA; 6: 50 mg C18+50 mg PSA)吸附剂净化,结果如图1所示。由图1可以看出,各待测物在采用组合4(C18 25 mg+PSA 50 mg)净化时有较好的回收率,90%的目标化合物回收率在90% ~111%范围内。且实验发现,仅使用C18(组合1、2、3)净化时,样品溶液颜色仍较深,吹干后剩余残渣较多,进样检测后,离子源污染较严重。而组合4、5、6的净化效果均较好。其中采用组合4、6净化时,绝大部分待测物的回收率相当,但其中待测物喷布特罗在组合4的回收率明显高于组合6。比较6个组合的回收率可以看出,PSA和C18使用量的增加都会引起喷布特罗的回收率下降,因此,选择组合4(即25 mg C18+50 mg PSA)作为净化剂。
 | 图1 不同净化剂组合对18种待测物回收率的影响Fig.1 Effects of the usage amount of C18 and PSA on recoveries of the 18 compounds1: 25 mg C18; 2: 50 mg C18; 3: 75 mg C18; 4: 25 mg C18+50 mg PSA; 5: 25 mg C18+100 mg PSA; 6: 50 mg C18+50 mg PSA. |
2.3 净化方式及时间的选择跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件 1.4.2 质谱条件 2 结果与讨论 2.1 提取试剂的优化 2.2 净化吸附剂的优化 2.3 净化方式及时间的选择 2.4 基质效应评价及消除 2.5 质谱条件的优化与质谱定性 2.6 线性范围、检出限、定量限、回收率与精密度 2.7 实际样品测定 3 结论 参考文献
净化时采用的方式有两种,涡旋或振荡。实验比较了涡旋1、2 min和振荡5、10、20 min的净化效果。结果显示,不同振荡时间对回收率和净化效果无明显影响,且与涡旋2 min的结果相当。而涡旋1 min的样品,其响应均有不同程度的降低,50%的待测物响应降低20%以上。原因在于吸附时间过短,杂质吸附不完全。考虑到建立本实验方法是为了快速前处理,且在实验室也可实现批量样品同时涡旋,因此选择涡旋2 min为净化条件。
2.4 基质效应评价及消除跳转到:本文顶部 1 实验部分 1.1 仪器与试剂 1.2 标准溶液的配制 1.3 样品处理 1.4 HPLC-MS/MS条件 1.4.1 HPLC条件