分子检测定性项目的性能验证
为加强新冠病毒核酸检测能力建设,以更好满足新冠肺炎疫情常态化防控要求,去年至今各地新建和改扩建的PCR实验室数量快速增长。虽在每次举办的PCR培训班上我们都会重点讲解性能验证相关内容,但在实验室现场验收或督查过程中,仍发现不少实验室对性能验证相关知识并不是很清楚。今天就以新冠病毒核酸检测项目为例,和大家探讨一下分子检测定性项目性能验证的一些知识,希望能对大家有点帮助。
检验程序常规应用前。 任何严重影响检测系统分析性能的情况发生后(包括但不限于仪器主要部件故障、仪器搬迁、设施环境的严重失控等),应在检测系统重新启用前对受影响的性能进行部分性能验证。 实验室增加新的检测系统时,新的检测系统包含现用检测系统的任一要素(仪器、试剂等)变更,如试剂升级、仪器更新等。
PS:新增检测项目时需做性能验证,大部分实验室都很清楚这点。但有些实验室在新增/变更部分仪器/试剂的情况下,认为仅进行系统间比对即可,这并不符合相关要求,此种情况下也是需按照新系统进行性能验证。
操作人员应经过培训,熟悉所用方法原理与操作。 仪器经过校准,各项性能指标合格。 实验室设施及环境符合工作要求。 试剂满足要求。 性能验证人员应了解验证方案、制定验证计划并组织实施。
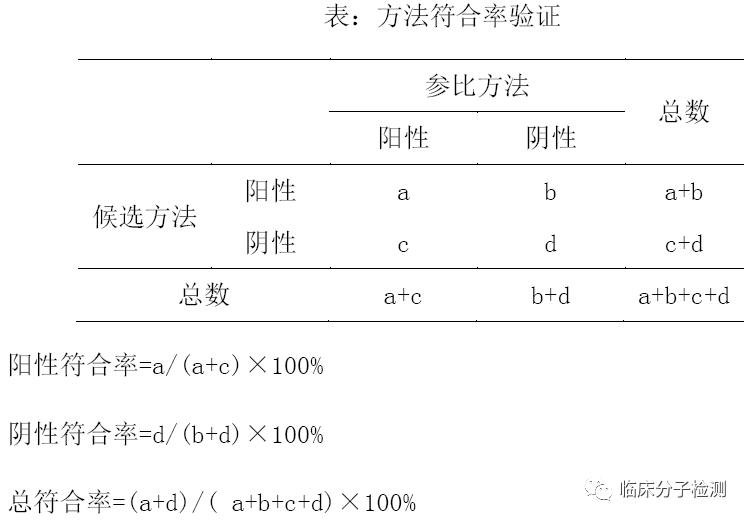
验证要求:通过与参比方法进行比较。参比方法:金标准方法、行业公认方法、经验证性能符合要求满足临床预期用途的方法(如:通过 ISO15189 认可实验室使用的相同检测方法)。 验证方案:
样本:新鲜或冻存的阴性和弱阳性样本各一份。对于无法获得足量临床阳性样本的项目,可对临床阳性样本进行稀释或使用人工制备样本(如假病毒颗粒、质粒等)。 验证方法:每天检测3-4次,连续检测5天,阴阳性样本符合率≥90%。如对新冠病毒核酸检测项目,其阴阳性样本的符合率应为100%,同时阳性样本重复检测Ct值的变异系数(CV)应<5%。
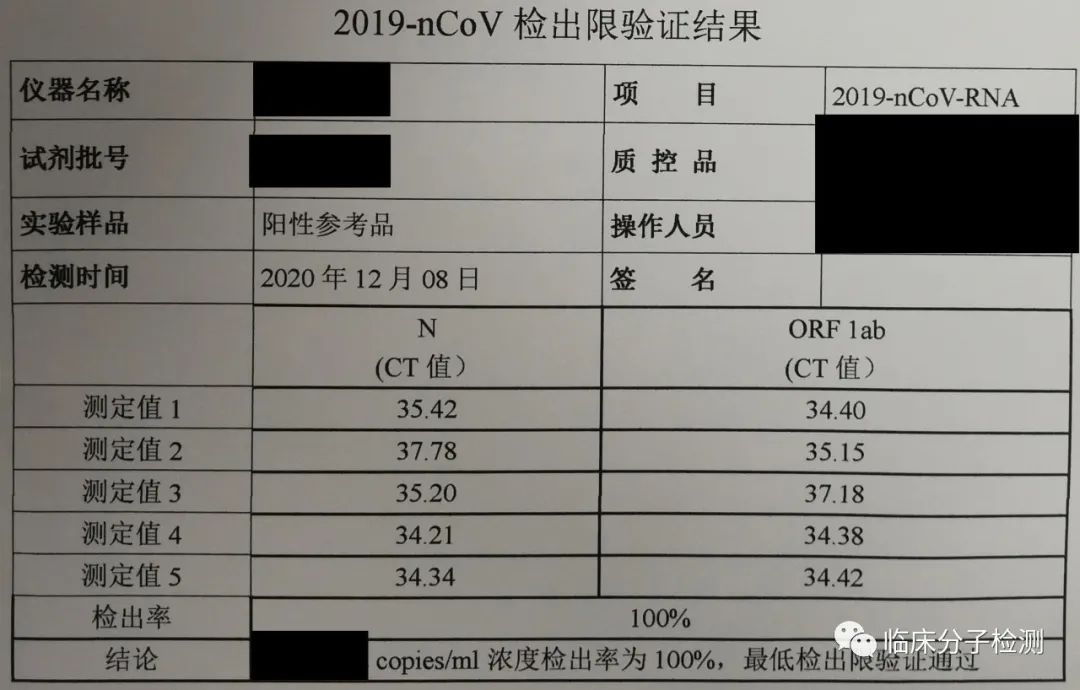
验证要求:所用检验程序在厂家试剂使用说明书等有声明检出限时,检测项目在有标准物质时,或以定量形式表达定性结果时,应进行检出限的验证。 样本要求:定值标准物质(如:国际参考品、国家参考品、厂家参考品)。对于报告具体基因型的方法,其选用的标准物质需包括所有的突变类型。对于检测对象同时含有不同比例的不同基因型时,应设置多个梯度,主要从扩增反应终体系总核酸浓度和突变序列所占比例两个方面进行评价。 验证方法:使用定值标准物质的样本梯度稀释至厂家声明的检出限浓度,可重复测定5次或在不同批内对该浓度样本进行20次重复测定(如测定5天,每天测定4份样本)。稀释液可根据情况选用厂家提供的稀释液或阴性血清,该阴性血清除被验证的目标物必须阴性外,所含干扰物质浓度必须在厂家声明的范围之内。如对于新冠病毒核酸检测项目,可选用有证的定值标准物质或定值质控品样本。 判断标准:如果是5次重复检测,必须100%检出靶核酸;如果是20次检测,必须检出至少18次靶核酸。
当然,除上述符合率、精密度和检出限等性能指标外,实验室也可根据自身情况对试剂说明书中的其他性能指标进行验证,如交叉反应和抗干扰能力等,不过这并不是强制要求的。
从定性结果来看,此浓度样本确实100%检出了。但如果仔细看下N基因和ORF1ab基因检测的Ct值,我想很多人应该会产生这样的疑问:这是同一浓度样本同批重复5次的检测结果?如果真的做成这样,那说明检测系统中某个环节必然存在大问题!而如果检测系统没有问题,那么只能说明这份报告并不真实。
因此,为保证实验室检测系统良好运行,请大家务必认真对待性能验证,严格按照相关要求进行性能验证,以最大限度地保证本实验室检测结果的准确可靠。
CNAS-CL02:2012《医学实验室质量和能力认可准则》
CNAS-GL039:2019《分子诊断检验程序性能验证指南》
CNAS-GL037:2019《临床化学定量检验程序性能验证指南》