用泡一杯方便面的时间读懂免疫细胞治疗
美国生物学家乔治戴利曾经说过,如果20世纪是药物治疗的时代,那么21世纪就是细胞治疗的时代。
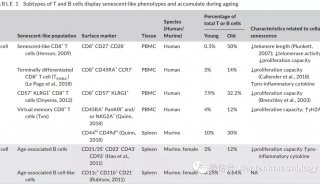
细胞治疗是指利用某些具有特定功能的细胞的特性,采用生物工程方法获取和/或通过体外扩增、特殊培养等处理后,使这些细胞具有增强免疫、杀死病原体和肿瘤细胞、促进组织器官再生和机体康复等治疗功效,从而达到治疗疾病的目的。免疫细胞治疗作为细胞治疗的一种,作为继手术,放、化疗之后的第四大肿瘤治疗技术,经过长足的发展,已经在多种肿瘤的治疗上发挥了很好的疗效,给人们带来了曙光。
免疫细胞治疗在多种肿瘤的治疗上可以达到两个目的,一是普遍改善肿瘤患者免疫状态,这是机体战胜肿瘤的基本保障;另一是特异或非特异地杀伤肿瘤细胞。
图片来源[2]
免疫细胞治疗分类
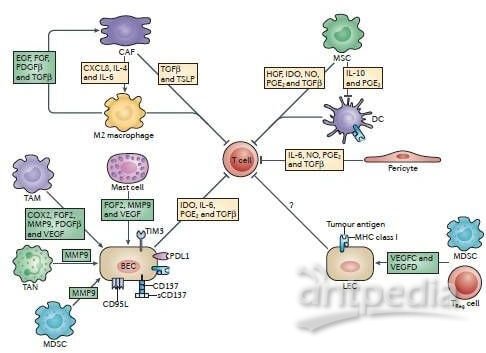
在杀伤肿瘤细胞过程中,无特定靶向作用靶点的淋巴因子激活的杀伤细胞(LAK)、细胞因子诱导的杀伤细胞(CIK)、树突状细胞(DC),以及有特定作用靶点的各种T淋巴细胞,如肿瘤浸润性T细胞(TIL)、T细胞受体嵌合型T细胞(TCR-T)、嵌合抗原受体T细胞(CAR-T) 等均发挥重要作用。
淋巴因子激活的杀伤细胞
淋巴因子激活的杀伤细胞 (lymphokine activatedkiller cells, LAK) 是最早的细胞免疫治疗方法。LAK疗法是将健康人外周血单核白细胞 (peripheral blood mononuclear leukocytes, PBL)在体外培养,经淋巴因子白介素2 (interleukin 2, IL-2)激活后扩增,回输至患者体内从而广谱地杀伤肿瘤细胞(杀伤对NK细胞不敏感的肿瘤细胞)的治疗方法。该疗法对转移性肾细胞癌、黑素瘤、结肠癌和非何杰金氏淋巴瘤患者的疗效较显著。
肿瘤浸润性T细胞
肿瘤浸润性淋巴细胞(tumor-infltrating lymphocytes, TIL) 疗法,即采集、分离患者肿瘤组织浸润淋巴细胞或引流淋巴结中的淋巴细胞,在体外扩增后回输给患者,用于抗肿瘤治疗。与LAK疗法相比,TIL疗法具有一定的肿瘤特异性,临床效果优于LAK治疗,黑色素瘤的治疗效果较为明显。TIL疗法主要治疗皮肤、肾、肺、头颈部、肝、卵巢部位的原发或继发肿瘤。
细胞因子诱导的杀伤细胞及链式激活的免疫细胞
细胞因子诱导的杀伤细胞(cytokine-induced killercells, CIK)是通过细胞因子IL-2、CD3单抗以及干扰素γ(interferon γ, IFN-γ) 共同诱导外周血单核细胞(peripheral blood mononuclear cells, PBMC)而获得。CIK是非主要组织相容性复合体(major histocompatibility complex, MHC)限制性的杀伤细胞,在血液系统肿瘤及肝癌、肺癌等实体肿瘤的治疗中有一定的疗效。链式激活的免疫细胞(cascade-primed immunecells, CAPRI) 是在CIK的基础上发展而来,CAPRI主要是利用患者自身的PBMC,加入CD3单抗和IL-2激活,并在体外将初始T细胞诱导为杀伤性效应细胞。CAPRI细胞治疗的临床效果优于CIK、LAK等细胞治疗,延长了转移性乳腺癌、非小细胞肺癌等多种肿瘤患者的生存时间。
树突状细胞
树突状细胞(dendritic cells, DC) 是主要的抗原提呈细胞,通过识别抗原呈递给淋巴细胞,是启动适应性免疫的关键细胞。DC疗法是将患者自身的单个核细胞提取出来,在体外增殖、培养、诱导生成DC细胞,让DC细胞负载相应的肿瘤抗原后回输患者体内,诱导机体产生特异性或非特异性的免疫应答,激活人体内的天然抗肿瘤系统,杀灭肿瘤细胞。临床试验显示,DC-CIK和肿瘤特异淋巴细胞过继性回输的方法可使部分患者的肿瘤得到缓解。
T细胞受体嵌合型T细胞
T细胞受体基因修饰T细胞(T-cell receptorengineered T cells,TCR-T) 技术是利用自身的外周血T细胞,通过基因修饰将针对肿瘤相关抗原的TCR序列转入T细胞中,成为肿瘤抗原特异性T细胞,这是针对不同患者肿瘤抗原的差异所进行的“个体化”治疗。TCR-T治疗方法最初应于黑色素瘤,此后多项研究证明滑膜细胞肉瘤、黑色素瘤以及多发性骨髓瘤患者在接受了NY-ESO-1 TCR-T后,肿瘤出现部分或完全消退,其中位生存时间明显延长。
嵌合抗原受体T细胞
另一种基因修饰T细胞的方法——嵌合抗原受体T细胞(chimeric antigen receptor-modifed T cell,CAR-T)则是通过基因工程技术,将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),将T细胞这个普通“战士”改造成“超级战士”,即CAR-T细胞,他利用其“定位导航装置”CAR,专门识别体内肿瘤细胞,并通过免疫作用释放大量的多种效应因子,它们能高效地杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。目前,靶向CD19的CAR-T细胞在血液肿瘤的治疗中已获得了令人振奋的抗肿瘤效果。到目前为止已经设计了五代CAR-T细胞,赋予了CAR-T细胞疗法无限的生机和未来。
研究中的细胞治疗类型数量占比[3]
免疫细胞治疗药物进展
目前,全球共有2个免疫细胞治疗类药物已经获得批准上市,分别是诺华(Novartis)开发的Kymriah(靶向CD19的CAR-T疗法)以及KitePharma公司开发的Yescarta/ciloleucel(靶向CD19的CAR-T疗法),分别在2017年8月和10月获得了美国 FDA 批准。
全球免疫细胞治疗类药物中已完成预注册的药物为韩国YooYoung Pharmaceuticals公司申请的新药YYB-103(靶向白细胞介素13受体α2( IL13Rα2) 的CAR-T疗法)。
此外,免疫细胞治疗类药物,如:Tabelecleucel( 曾用名: ATA129,是同种异体EB病毒特异性细胞毒性T淋巴细胞)、anti-CD19CART-cell therapy(CAR-T疗法)、eltrapuldencel-T ( 产品编号:NBS20,一种树状细胞治疗性疫苗)、Rexmyelocel-T ( 产品编号:REX-001,一种自体骨髓来源的成熟单核细胞(BMMNC) 治疗药物)等已经进入了临床Ⅲ期,其适应症涵盖了淋巴增生性疾病、肝癌、周围动脉闭塞性疾病、糖尿病并发症等, 有望为更多疾病提供治疗选择。
在免疫细胞治疗类药物中有多个产品已经进入了临床Ⅱ期研究例如,AUTO-3(一种可同时靶向CD19和CD22的 CAR-T疗法)、MG7-CAR(MG7靶向治疗的CAR-T疗法)、bb-2121(针对复发/难治性多发性骨髓瘤患者的靶向B细胞成熟抗原( BCMA)的CAR-T疗法药物)等。
免疫细胞治疗在肿瘤中研发趋势[4]
随着2017年底,FDA先后批准两个CAR-T药物上市这个里程碑事件,未来免疫细胞治疗行业将迎来高速发展时期,免疫细胞的能量将会不断被挖掘 ,更多的产品将进入Ⅱ/Ⅲ期临床试验甚至更后面阶段,更多的癌症患者有望迎来更多的选择。