蛋白质的纯化
实验概要
本实验介绍了用蛋白纯化试剂盒(HisTrap HP Kit)进行蛋白质纯化的过程。
主要试剂
高分子量蛋白Marker购自上海华舜生物工程有限公司
蛋白纯化所用的试剂盒(HisTrap HP Kit)购自Amersham Biosciences ( USA)公司
0.45 pm滤膜,磷酸缓冲液,咪唑,NaCl,EDTA,NaOH,NiSO4,0.025%考马斯亮兰R-250
主要设备
注射器,高速离心机,变性聚丙烯酞胺蛋白凝胶电泳装置
实验步骤
纯化的过程是在室温25℃的条件下进行的。纯化之前,按照HisTrap HP Kit说明书制备蛋白样品,然后用0.45 pm滤膜过滤,去除一些细胞碎片或其它杂质,以免阻塞镍柱,纯化时使用注射器上样。
1. 镍柱的准备
在第一次使用镍柱时,先用5 ml蒸馏水过柱,如有空气存在,应反复用水冲洗,直至空气消除;然后用5 ml binding buffer (1 x磷酸缓冲液,20 mM咪唑,pH 7.4)过柱和5 ml elution buffer(1 x磷酸缓冲液,40 mM咪唑)过柱,最后用10 ml binding buffer过柱。
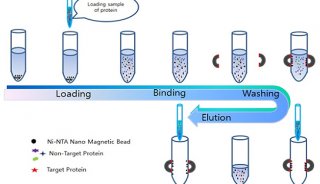
2. 样品过柱
用注射器吸取10 ml binding buffer过柱,平衡柱子(lx的磷酸buffer,20mM咪唑,pH7.4 );上样(含his-tags的融合蛋白样品),收集蛋白flow-through fraction;10 mlbinding buffer过柱,收集wash fraction;5 ml elution buffer (1 x磷酸缓冲液,40 mM咪唑)过柱,收集洗脱液,每毫升收集一管;依次使用更高咪哩浓度的缓冲液洗柱,并分别收集相应的洗脱液。
3. 镍柱再生
10 ml binding buffer (1 x磷酸缓冲液,20 mM咪唑,pH 7.4)过柱后镍柱即可再次使用,但为防止蛋白的交叉污染,每根柱子最好只用于同种蛋白的纯化。如果用于不同蛋白的纯化,必需进行柱子的清洗,并重新填充镍离子。在重新填柱或储存之前,要将柱子中的镍离子去除,用10 ml包含有20 mM磷酸钠,0.5 M NaCl,0.05 M EDTA,pH7.4的buffer清洗柱子,为了去除沉淀的蛋白,先去除镍离子后,用1M的NaOH充满柱子,然后将柱子浸泡在NaOH中2h,用10 ml蒸馏水和pH7.0的buffer洗出溶解的蛋白,直至流出液的pH约达到7.0。再用10 ml蒸馏水清洗一次,然后用0.5 ml 0.1 M NiSO4(用蒸馏水配制)填充柱子。最后,再先后用5 ml蒸馏水和5 ml binding buffer过一次柱子。现在的柱子就可以重新使用了。
4. 最佳洗脱浓度确定
收集的样品变性聚丙烯酞胺蛋白凝胶电泳((SDS-PAGE)观察,根据观察结果,确定融合蛋白的最佳洗脱缓冲液浓度,融合蛋白一般集中出现洗脱液的第二和第三管中。
5. His-tags融合蛋白的纯化
准备相应缓冲液(参见附录),控制pH值在7.4-7.6;根据镍柱准备的步骤进行洗柱;10 ml binding buffer(lx磷酸缓冲液,20 mM咪唑,pH 7.4)过柱;上样,收集flow-through fraction;分别用5 ml elution buffer(1 x磷酸缓冲液,20,40,60,300,500 mM咪唑)过柱,收集洗脱液,每毫升收集一管。
6. 融合蛋白的SDS-PAGE电泳
取样品液10ul与等体积的2xSDS加样缓冲液混合;沉淀用适当体积的1xSDS加样缓冲液悬浮;100℃沸水浴5 min,冷却后点样进行15% SDS-PAGE电泳(15%分离胶,5%浓缩胶),电泳结束,0.025%考马斯亮兰R-250染色。