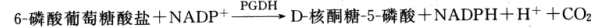由酶循环确定烟酰胺核苷酸实验——NADP(H) 的测定
烟酰胺核苷酸可以作为脱氢酶的底物被测定(特别是 LDH,ADH 作用于 NAD+ 和 G6PDH 作用于 NADP+),根据各自的吸收系数可以利用酶循环的方法在低浓度下被测定。
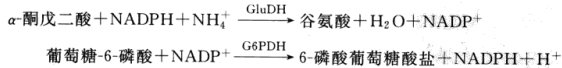
| 实验方法原理 | 为了测定 NADP(H),可以采用谷氨酸脱氢酶(GluDH)和葡萄糖-6-磷酸脱氢酶(G6PDH) 的偶联反应:
在指定的条件下,一个 NADP 分子可以催化生成 5000~10 000 个 6-磷酸葡萄糖酸盐。NADP的浓度为 10-9 mol/L(1 ul 含有 10~15 mol)时就可以检测到。ADP 作为 GluDH 的催化剂。 停止酶循环反应后,可以利用一个独立的 6-磷酸葡萄糖酸脱氢酶反应来测定 6-磷酸葡萄糖酸盐的生成量:
|
|---|---|
| 实验材料 | |
| 试剂、试剂盒 | Tris-HClα-酮戊二酸D-葡萄糖-6-磷酸盐ADP乙酸胺BSA谷氨酸脱氢酶葡萄糖 6-磷酸脱氢酶6-磷酸葡萄糖酸盐EDTA6-磷酸葡萄糖酸脱氢酶 |
| 仪器、耗材 | |
| 实验步骤 | 实验所需「试剂」具体见「其他」 1. NADP 或 NADPH 的测定 0.1 ml 循环混合物:
被测定的 x ul NADP 或 NADPH 溶液[x 为 1~20; 浓度为(3~50)×10-9 mol/L]。 (20~x)ul 0.1 mol/L Tris-HCl,pH 8.0 37 ℃ 培养 30 min 将样品转移到 100℃、2 min 来终止反应。 2. 6-磷酸葡萄糖酸盐的荧光测定
在发射 470 nm(激发 325 nm)处测定荧光、实验可以通过 6-磷酸葡萄糖酸盐标准曲线来定量。 展开 |
| 注意事项 | |
| 其他 | 试剂: 0.1 mol/L Tris-HCl,pH 8.0 0.1 mol/L α-酮戊二酸(二钠盐,Mr=190.1;190 mg 溶于 10 ml 水中) 0.1 mol/L D-葡萄糖-6-磷酸盐(二钠盐,氢氧化物,Mr=304.1;304 mg 溶于 10 ml 水中) 0.01 mol/L ADP(二钠盐,Mr=471.2;47.1 mg 溶于 10 ml 水中) 1.0 mol/L 乙酸胺(Mr=77.1;771 mg 溶于 10 ml 水中) BSA(20 mg/ml); 谷氨酸脱氢酶(来自于牛肝脏,40 U/mg,配制好的溶液:40 U/0.1 ml 0.1mol/L Tris-HCl,pH 8.0) 葡萄糖 6-磷酸脱氢酶(来自于酵母,300 U/mg,配制好的溶液: 60 U/0.1ml 0.1mol/L Tris-HCl,pH 8.0) 0.01 mol/L 6-磷酸葡萄糖酸盐(三钠盐,Mr=342.1;34 mg 溶于 10 ml 水中) 0.01 mol/L NADP(Mr=787.4;79 mg 溶于 10 ml 水中) 0.1 mol/L EDTA(Mr=292.2;292 mg溶于 10 ml 水中) 6-磷酸葡萄糖酸脱氢酶(来自于产朊假丝酵母,20 U/mg; 配制好的溶液:0.1 U/0.1 ml 0.1 mol/L Tris-HCl,pH 8.0) 展开 |