3月14日 Nature 杂志生物学精选
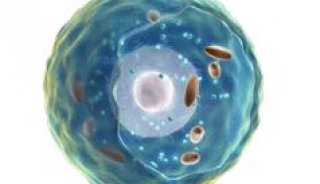
新兴的致病性冠状病毒hCoV- EMC(2012年9月首次被发现)对迄今被感染的少数人当中大约一半来说都是致命的。现在,Bart Haagmans及其同事识别出了该病毒用来感染细胞的受体。与相关病毒SARS-CoV(它所利用的是“血管紧缩素转化酶-2”)形成对比的是,hCoV-EMC的功能受体是“二肽基肽酶-4”(即DPP4,亦称为 CD26)——下呼吸道中无纤毛细胞上所发现的一种外肽酶。这种酶在各种不同物种中都是高度保守的,而且hCoV-EMC还能将蝙蝠的DPP4用作一个功能受体,这为这一新病毒的宿主范围及流行病史提供了一个可能的线索。这些发现对于干预策略的制定也可能是重要的。本期封面所示为原始细支气管上皮细胞培养中的“二肽基肽酶-4”(红色),即功能性冠状病毒-EMC受体,它在无纤毛细胞上,而不是在有纤毛细胞(黄色)上。
种群表观遗传多样性的模式
像自然遗传变异一样,自然外成变异(表观遗传变异)也是表现型多样性的一个来源。自然外成变异是指由DNA序列的改变以外的机制所引起的基因表达的可遗传改变。然而,对于外成变异体是怎样形成的以及遗传变异在种群层面上是怎样与外成变异联系在一起的却很少有研究。本文作者通过测定从整个北半球分离出的 “拟南芥”植物拥有超过150个新增成员的一个种群的基因组、甲基化组和转录组的序列,发布了第一个全基因组的、达到碱基分辨率的、种群层面的外成(表观遗传)分析结果。他们识别出了数以千计的DNA甲基化变异体,其中很多都与遗传变异体相关。这些分析结果还显示,由RNA引导的DNA甲基化作为目标的基因可能采用了这样一个机制:它使“转位子”沉默,以保持其在植物组织中的沉默状态,并确保在花粉、种子和生殖系发育中有正确的表达。
大脑怎样将时空联系起来
内侧颞叶(大脑中处理包括记忆在内的高级功能的区域)中的网格细胞以周期性的、像晶格一样的形式发射信号,来帮助导航,但目前仍不清楚这些网格一样的发射模式是怎样出现的。在这项研究中,David Tank及其同事对沿虚拟现实中的线性跑道奔跑的小鼠的这些细胞中的电压变化和细胞内动态进行了直接测定。他们发现,网格发射场是由缓慢的去极化产生的,网格细胞还表现出能影响它们尖峰时间的细胞内θ-振荡。这些数据与(假定)网格细胞来自“吸引子”(attractor)动态、θ-振荡控制网格细胞尖峰时间的模型最为一致。
PRC1在生殖细胞发育中所起作用
Polycomb group(PcG)蛋白参与胚胎干细胞中发育调控因子的转录抑制,在那里,它们在随后的发育过程中维持多能性和细胞身份。Antoine Peters及其同事研究了Polycomb repressive complex 1 (PRC1)在小鼠原始生殖细胞(PGCs)的发育中所发挥的功能。他们观察了PRC1在发育中的多种性别特异性作用。PRC1是维持转录因子Oct4 和Nanog的高水平表达所必需的。而且,通过抑制雌性生殖嵴的“体细胞腔”所提供的视黄酸信号作用,PRC1还确保诱导发生减数分裂的适当时机。
与卵巢癌相关的“干细胞龛”
最近发表的对卵巢癌所做的综合基因组分析,为这种致命疾病的分子异常提供了一个广泛的“目录”,但有关这种癌症起源于哪些上皮细胞的不确定性使这些分析结果的应用复杂化了。这项研究发现,小鼠卵巢门区域中一个干细胞群是由RB1 和TRP53肿瘤抑制因子的丢失所诱导的卵巢癌的起源——这两个抑制因子的通道在最具侵略性的、最常见的人上皮卵巢癌中经常被改变。